Содержание
- 2. Цель: научить вести расчеты по уравнению химической реакции, зная количество вещества, массу или объем одного из
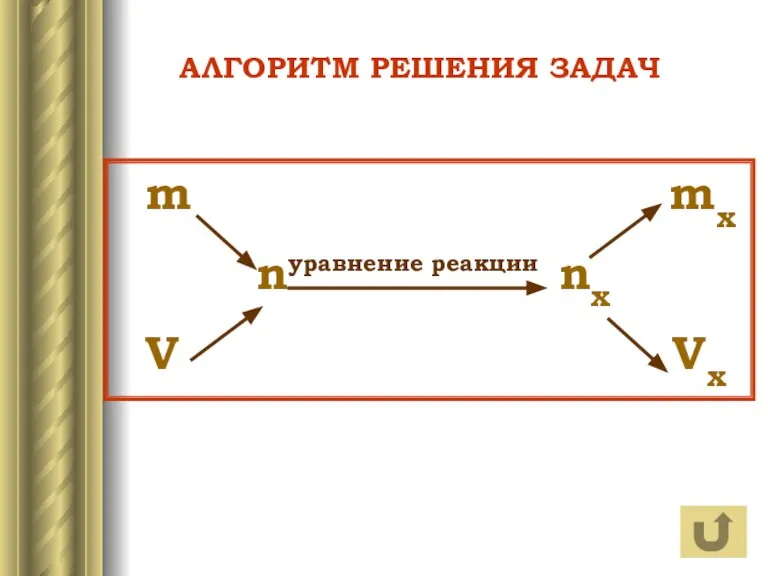
- 3. АЛГОРИТМ РЕШЕНИЯ ЗАДАЧ
- 4. Дано: n(H2) = 1,5 моль n(Al) – ? Решение: x моль 1,5 моль 2Al + 6HCl
- 5. Дано: n(Al2S3) =2,5 моль n(S) – ? Решение: x моль 2,5 моль 2Al + 3S =
- 6. Дано: m(Cu(OH)2)=14,7 г m(CuO) – ? M(Cu(OH)2) = 64+(16+1)·2 = 98г/моль M(CuO) = 64 +16 =
- 7. Дано: m(Zn)=13 г m(ZnCl2) – ? M(Zn) = 65 г/моль M(ZnCl2 =65 +35,5·2 = 136 г/моль
- 8. Дано: m(MgO) = 6 г V(O2) – ? M(MgO) = 24+16 = 40 г/моль Vm =
- 9. Дано: m(Cu)=32 г V(H2) – ? M(Cu) = 64 г/моль Vm = 22,4 л/моль Решение: x
- 10. САМОСТОЯТЕЛЬНАЯ РАБОТА: ВАРИАНТ 1: Вычислите массу меди, которая образуется при восстановлении избытком водорода 4 г оксида
- 11. ДОМАШНЕЕ ЗАДАНИЕ: Рассчитайте, какая масса кислорода образуется при разложении 108 г воды. Вычислите объем (н.у.) газа,
- 13. Скачать презентацию









 Эмульсия. Основные типы эмульсий
Эмульсия. Основные типы эмульсий Квантовая химия
Квантовая химия Алкены Бутен
Алкены Бутен Металлы
Металлы Химический диктант по органической химии. 9 класс
Химический диктант по органической химии. 9 класс Химические реакции. Классификация
Химические реакции. Классификация Знакомство с химией
Знакомство с химией Применение каучука
Применение каучука Неорганический мозговой штурм
Неорганический мозговой штурм Практическая работа: Очистка загрязнённой поваренной соли
Практическая работа: Очистка загрязнённой поваренной соли Буферные системы
Буферные системы Cеминар 6 -Алканы-2
Cеминар 6 -Алканы-2 Химические реакции
Химические реакции Электроосмос. Практическое применение электроосмоса
Электроосмос. Практическое применение электроосмоса Магматические горные породы
Магматические горные породы 1_
1_ Физические и химические свойства металлов
Физические и химические свойства металлов Строение электронных оболочек атома
Строение электронных оболочек атома Железо
Железо Производные салициловой, пара-аминобензойной кислот, применяемые в медицине
Производные салициловой, пара-аминобензойной кислот, применяемые в медицине коррозия металлов
коррозия металлов Индикаторная бумага
Индикаторная бумага Тренажер - Валентность. 8 класс
Тренажер - Валентность. 8 класс Потенциометрический анализ, титрование
Потенциометрический анализ, титрование Алкины
Алкины Лучший тест для подготовки к ЕГЭ по химии
Лучший тест для подготовки к ЕГЭ по химии Тривиальные названия веществ, наиболее часто встречаемых в ЕГЭ
Тривиальные названия веществ, наиболее часто встречаемых в ЕГЭ Блок колонн на установке замедленного коксования производительностью 730000 тонн/год гудрона (поз.к-1, кх-1)
Блок колонн на установке замедленного коксования производительностью 730000 тонн/год гудрона (поз.к-1, кх-1)