Содержание
- 2. Рідкі кристали Деякі органічні матеріали при переході з рідкого стану в твердий мають проміжну структуру. Речовина
- 3. Речовини, молекули яких за певних умов здатні утворювати рідкокристалічні фази, називаються мезогенами. Як правило, ці молекули
- 4. Рідкі кристали відкрив в 1888 р. австрійський ботанік Ф. Рейнитцер. Науковий доказ було надано професором університету
- 5. Рідкі кристали Ліотропні Термотропні
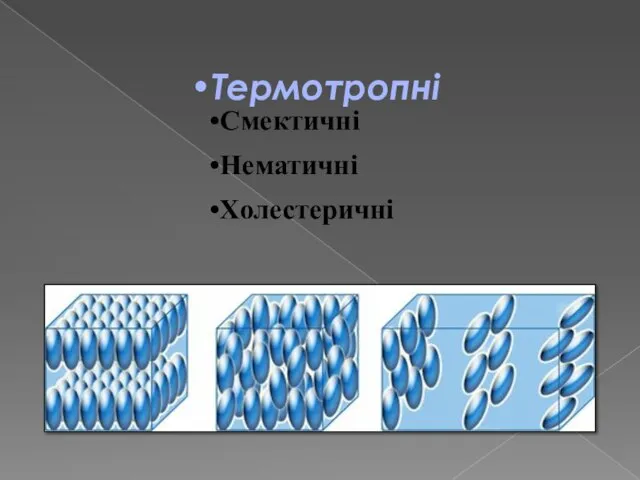
- 6. Термотропні Смектичні Нематичні Холестеричні
- 7. Нематичні кристали Найбільш простий різновид РК- нематики (від грец. «Нема» - нитка) - утворюють довгі ниткоподібні
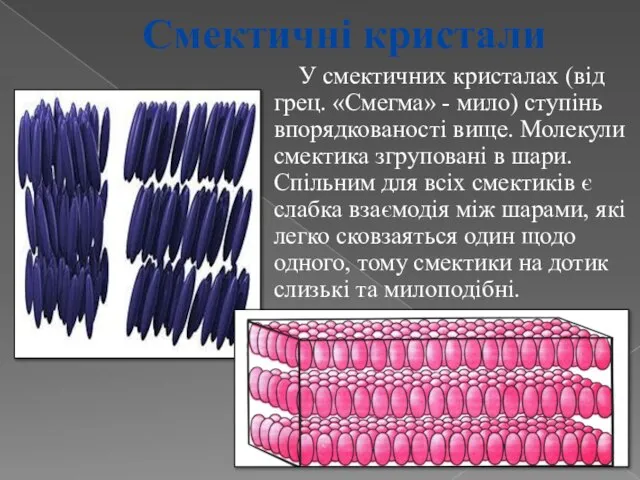
- 8. Смектичні кристали У смектичних кристалах (від грец. «Смегма» - мило) ступінь впорядкованості вище. Молекули смектика згруповані
- 9. Найбільш складно влаштовані молекули холестеричних рідких кристалів мають форму довгастих пластинок, розташованих паралельно один одному. Їх
- 10. Освітленні пучком поляризованого білого світла, холестеричні рідкі кристали мають райдужне забарвлення, яке залежить від природи речовини,
- 11. Загальна для всіх типів рідких кристалів властивість – подвійне заломлення світла, характерне для більшості твердих кристалів,
- 12. Перехід Фредеріка Явище переорієнтації молекул рідкого кристалу під дією електричного поля
- 13. Використання Одне з важливих напрямів використання рідких кристалів - термографія.
- 14. Рідкі кристали у вигляді плівки наносять на деталі електросхем. Несправні елементи - сильно нагріті або холодні,
- 15. Рідкі кристали також використовують у косметичних цілях для догляду за волоссям.
- 17. Скачать презентацию












 2.Химич. м-ды колич. ан-за
2.Химич. м-ды колич. ан-за Химия переходных элементов. Триада железа и металлы платиновой группы
Химия переходных элементов. Триада железа и металлы платиновой группы Бутадиен-стирольный каучук. 10 класс
Бутадиен-стирольный каучук. 10 класс Значение и применение спиртов
Значение и применение спиртов Теория валентных связей
Теория валентных связей Кислород. Применение и круговорот в природе. 8 класс
Кислород. Применение и круговорот в природе. 8 класс Сұрақтар
Сұрақтар Презентация по Химии "Анилин"
Презентация по Химии "Анилин" 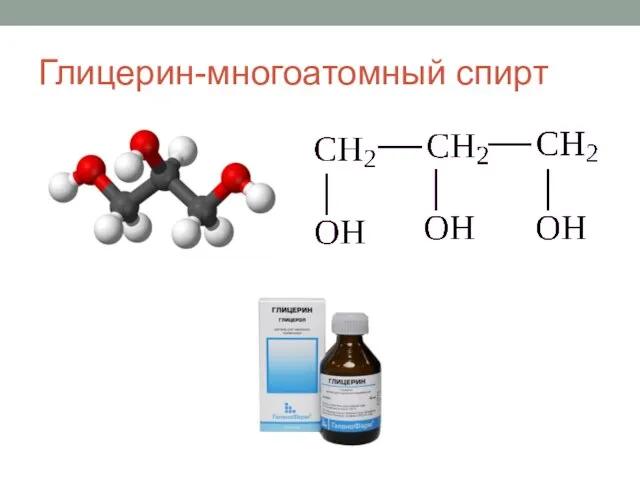 Жиры. Классификация жиров
Жиры. Классификация жиров Разработка математического описания расчета октанового числа бензинов каталитического риформинга с групповой кинетикой
Разработка математического описания расчета октанового числа бензинов каталитического риформинга с групповой кинетикой Сера
Сера Электролитическая диссоциация
Электролитическая диссоциация Структура периодической таблицы элементов
Структура периодической таблицы элементов d-элементы.Распространение в природе и основные материалы
d-элементы.Распространение в природе и основные материалы Альдегиды и кетоны. (Лекция 6.2)
Альдегиды и кетоны. (Лекция 6.2) Изменения, происходящие с веществами
Изменения, происходящие с веществами Элементы принадлежащие к VII группе периодической таблицы - галогены
Элементы принадлежащие к VII группе периодической таблицы - галогены Характеристика щелочных металлов (9 класс)
Характеристика щелочных металлов (9 класс) Аэрированный сшитый полимерный раствор (АСПР)
Аэрированный сшитый полимерный раствор (АСПР) Кислоты. Классификация. Номенклатура
Кислоты. Классификация. Номенклатура Виды нагрева и материалы резистивных нагревателей, их стойкость к температуре, ростовой атмосфере и расплаву
Виды нагрева и материалы резистивных нагревателей, их стойкость к температуре, ростовой атмосфере и расплаву Карбоновые кислоты
Карбоновые кислоты Термостабилизаторы. Доноры водорода
Термостабилизаторы. Доноры водорода Алмашу реакциясе
Алмашу реакциясе Алкадиены. Строение. Изомерия. Свойства
Алкадиены. Строение. Изомерия. Свойства Нахождение молекулярной формулы по данным о массовых долях элементов и относительной молекулярной массе (или молярной массе)
Нахождение молекулярной формулы по данным о массовых долях элементов и относительной молекулярной массе (или молярной массе) Свойства черных и цветных металлов
Свойства черных и цветных металлов Теория электролитической диссоциации
Теория электролитической диссоциации