Слайд 2Цель урока:
Изучение реакций ионного обмена и условий их протекания.
https://youtu.be/8vHOrE4AAlU

Слайд 3Эпиграф
Три пути ведут к познанию: путь размышления – самый благородный, путь подражания

– самый лёгкий, путь опыта – самый горький!
Слайд 4Ответьте на вопросы
1.Какие вещества называются электролитами? Приведите примеры.
2. Какие вещества называются неэлектролитами?

Приведите примеры.
3. В каком году и кто разработал теорию электролитической диссоциации?
Слайд 5Выполните задания
1.Перечисленные вещества разделите на 2 столбика: в один запишите электролиты, в

другой – неэлектролиты: р-р КОН, тв.КОН, крист. сахара, Н2SO4, спирт, дист.вода.
2. Запишите уравнение диссоциации следующих веществ: КNO3, Ba(OH)2, HCL, H2SO4
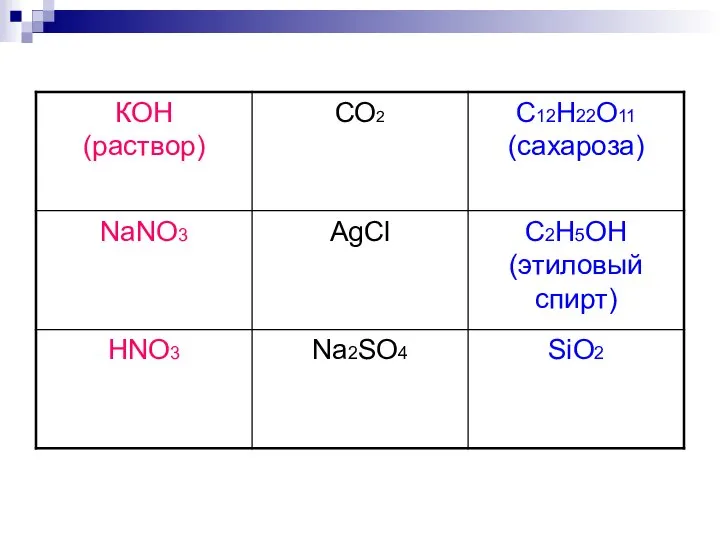
Слайд 7Выберите выигрышный путь, как в игре «крестики – нолики, где три вещества
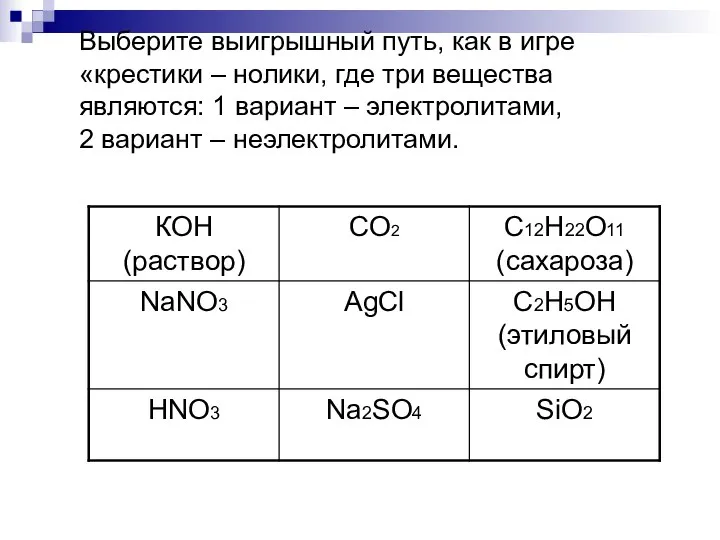
являются: 1 вариант – электролитами, 2 вариант – неэлектролитами.
Слайд 11Реакции между ионами называются ионными реакциями, а уравнения таких реакций – ионными

уравнениями.
Слайд 12 Реакции ионного обмена (РИО) протекают до конца в случае
Выпадения осадка
Выделения газа
Образования

малодиссоциирующего вещества(М), например вода.
Слайд 13Правила составления ионных уравнений
Простые вещества, оксиды, а также нерастворимые кислоты, основания, соли

не диссоциируют.
Для реакции берут растворы веществ, поэтому даже малорастворимые вещества находятся в растворах в виде ионов.
Если в результате реакции образовалось малорастворимое вещество, то при записи ионного уравнения его считают нерастворимым.
Слайд 14Алгоритм составления ионного уравнения
Записать молекулярное уравнение реакции.
С помощью таблицы растворимости определить растворимость

каждого вещества.
Составить полное ионное уравнение (найти одинаковые ионы и сократить их слева и справа)
Составить сокращенное ионное уравнение
Слайд 15Лабораторная работа
Тема: Реакции ионного обмена
Взаимодействие растворов NaOH и CuSO4
Взаимодействие растворов Na2CO3 и

HCl
Взаимодействие растворов NaOH и HCl
Слайд 16Взаимодействие растворов NaOH и CuSO4
вставьте ионы!!!!!!
2NaOH + CuSO4 Na2SO4 +Cu(OH)2
Уравнение в молекулярном
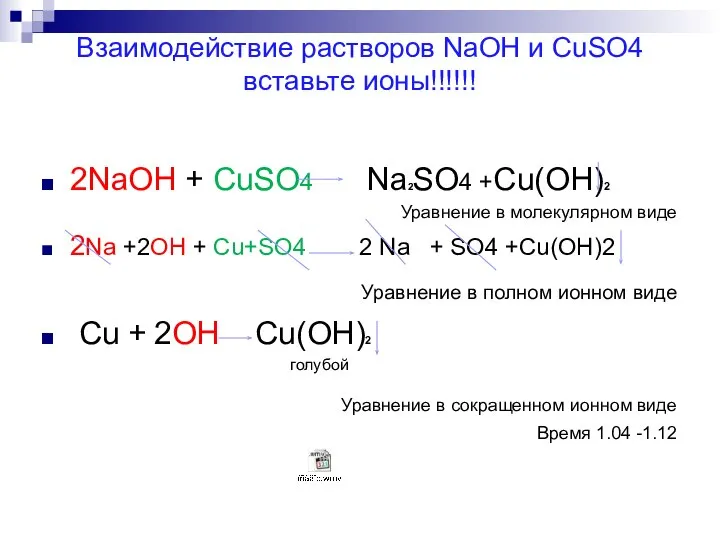
виде
2Na +2OH + Cu+SO4 2 Na + SO4 +Cu(OH)2
Уравнение в полном ионном виде
Cu + 2OH Cu(OH)2
голубой
Уравнение в сокращенном ионном виде
Время 1.04 -1.12
Слайд 17Взаимодействие растворов Na2CO3 и HCl
вставьте ионы!!!!!!
Na2CO3 + 2HCl 2NaCl +H2O + CO2

2Na + CO3 + 2H + 2Cl 2Na + 2Cl +H2O + CO2
CO3 + 2H H2O + CO2
бурное вскипание
Слайд 18
Взаимодействие растворов NaOH и HCl
(реакция нейтрализации)
NaOH + HCl NaCl + H2O
Фенолфт.
Na
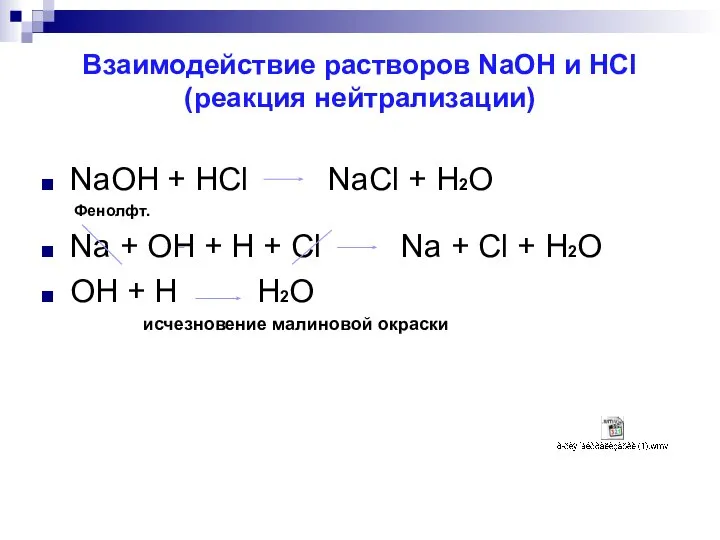
+ OH + H + Cl Na + Cl + H2O
OH + H H2O
исчезновение малиновой окраски
Слайд 23Оцените свою работу по направлениям
«Я» - как я себя чувствовал в процессе

урока, доволен ли я своей работой;
«Мы» - насколько комфортно и эффективно мне было работать в группе;
«Дело» - достиг ли я цели обучения, в чём испытал затруднения, как преодолеть проблемы.
Слайд 24Домашнее задание
§ 4, упр.1
https://youtu.be/0RCFox-oR_o
https://youtu.be/Sx0tldH9Grk
Соляная кислота + нитрат серебра HCl+ AgNO3 - HNO3

+ AgCl
H +Cl +Ag + NO3 - H + NO3 + AgCl
Cl +Ag - AgCl
белые хлопья
K2 SO4 + Ba(NO3)2 =
CaCO3 + H2SO3 = CaSO3 + H2O + CO2 ↑
CaCO3 + 2HNO3 = Ca(NO)2 + H2O + CO2 ↑
NaHCO3 + HCl = NaCl + H2O + CO2 ↑
2Na3PO4 + 3CaCl2 = Ca3(PO4)2 ↓ + 6 NaCl
NaHCO3+CH3COOH=CH3COONa+H2O+ CO2↑






















 Соли. Определение, состав, классификация, физические свойства, применение
Соли. Определение, состав, классификация, физические свойства, применение Синтетические душистые вещества
Синтетические душистые вещества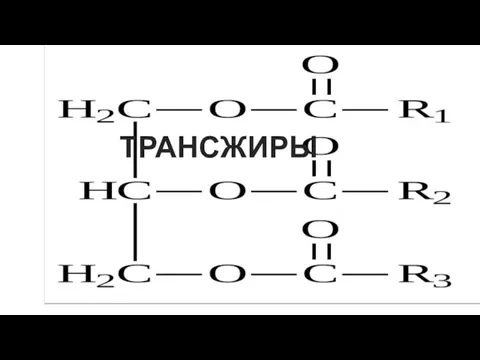 Трансжиры и их анализ
Трансжиры и их анализ Сероводород, сульфиды
Сероводород, сульфиды SHOT.шампуни. Состав. Компоненты
SHOT.шампуни. Состав. Компоненты Типы химических реакций. Реакции разложения, реакции соединения.8 класс
Типы химических реакций. Реакции разложения, реакции соединения.8 класс Стероиды. Дицетин-холестерин-ацилтрансферазная реакция
Стероиды. Дицетин-холестерин-ацилтрансферазная реакция Химический состав продуктов питания
Химический состав продуктов питания Агрегатное состояние вещества
Агрегатное состояние вещества Определение формул органических веществ. Задачи для самостоятельного решения
Определение формул органических веществ. Задачи для самостоятельного решения Презентация на тему Альдегиды и их свойства
Презентация на тему Альдегиды и их свойства  Кроссворд Интересные факты в химии
Кроссворд Интересные факты в химии Синтез и реакции пиридазина
Синтез и реакции пиридазина Ионная хроматография
Ионная хроматография Общая характеристика металлов
Общая характеристика металлов История гипса
История гипса Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Презентация на тему Ковалентная связь: полярная и неполярная
Презентация на тему Ковалентная связь: полярная и неполярная  Алкины и их свойства
Алкины и их свойства Металлы и неметаллы. Ознакомление с общими физическими свойствами металлов и неметаллов
Металлы и неметаллы. Ознакомление с общими физическими свойствами металлов и неметаллов Вторичная переработка нефти. Крекинг
Вторичная переработка нефти. Крекинг Переработка нефти. 10 класс
Переработка нефти. 10 класс Знатоки химии. Химия первопричина всех причин
Знатоки химии. Химия первопричина всех причин Типы химической связи и кристаллических решеток
Типы химической связи и кристаллических решеток Ренгеноструктурный и рентгеноспектральный анализы
Ренгеноструктурный и рентгеноспектральный анализы Оборудование и реактивы
Оборудование и реактивы Окситоцин. Сила любви и биология
Окситоцин. Сила любви и биология Относительная молекулярная масса
Относительная молекулярная масса