Содержание
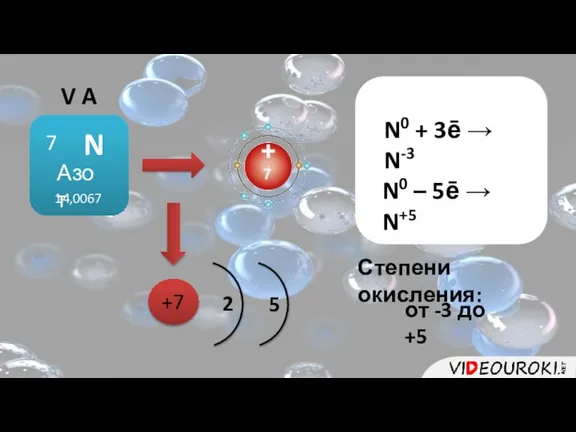
- 2. V A N0 + 3ē → N-3 N0 – 5ē → N+5 +7 2 5 Степени
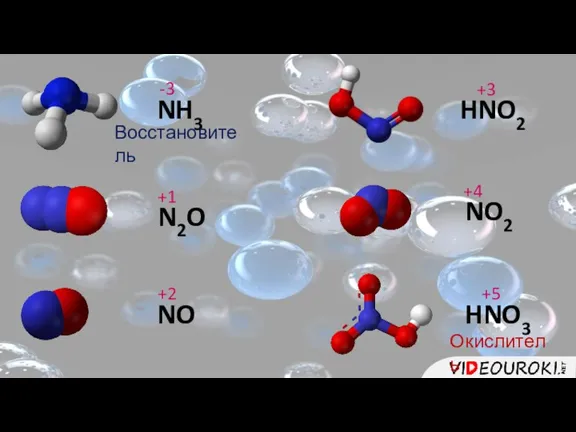
- 3. NH3 -3 N2O +1 NO +2 HNO2 +3 NO2 +4 HNO3 +5 Восстановитель Окислитель
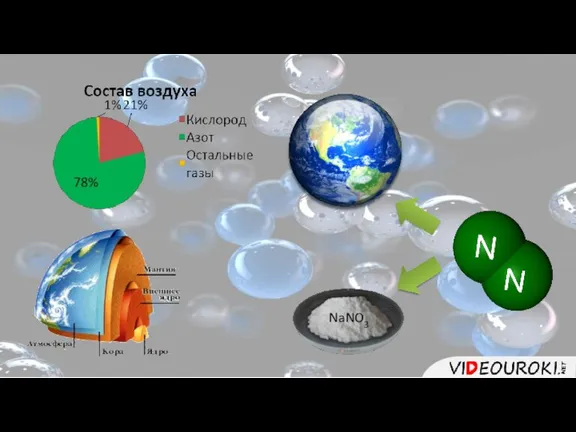
- 4. NaNO3
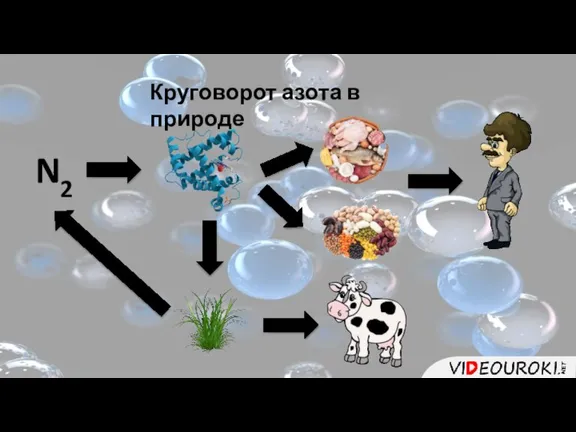
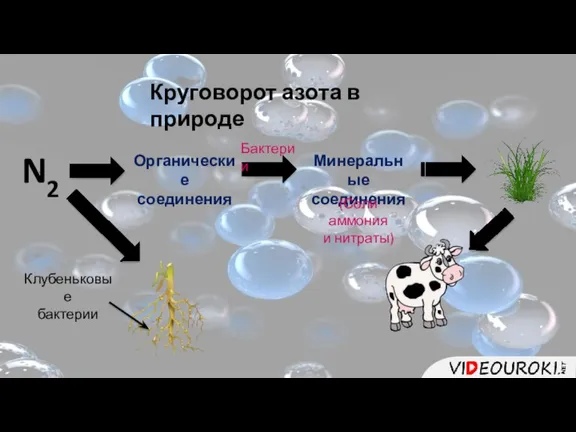
- 5. Круговорот азота в природе N2
- 6. Круговорот азота в природе N2 Органические соединения Минеральные соединения Бактерии (Соли аммония и нитраты) Клубеньковые бактерии
- 7. N2 + O2 ↔ 2NO 2NO + O2 ↔ 2NO2 4NO2 + O2 + 2H2O =
- 8. N2 Азот – малоактивное вещество. Азот является бесцветным газом, не имеет запаха и вкуса. Не сжижается
- 9. Химические свойства азота 1. Реакции с металлами 6Li + N2 = 2Li3N 0 0 +1 -3
- 10. 3. Реакция с кислородом Химические свойства азота 0 0 +2 -2 Восст-ль оксид азота (II) Ок-ль
- 11. Применение азота 1 1 - производство аммиака и азотной кислоты 2 2 - создание инертной среды
- 12. Д. Резерфорд В 1772 г. в экспериментах по сжиганию веществ обнаружили газ, не поддерживающий дыхание и
- 13. Определите массу соединения, которое образуется при нагревании металлического магния массой 7,2 г в азоте объёмом (н.у.)
- 15. Скачать презентацию






 Юные химики. Своя игра
Юные химики. Своя игра Оксидтер мен негіздердің реакциялары
Оксидтер мен негіздердің реакциялары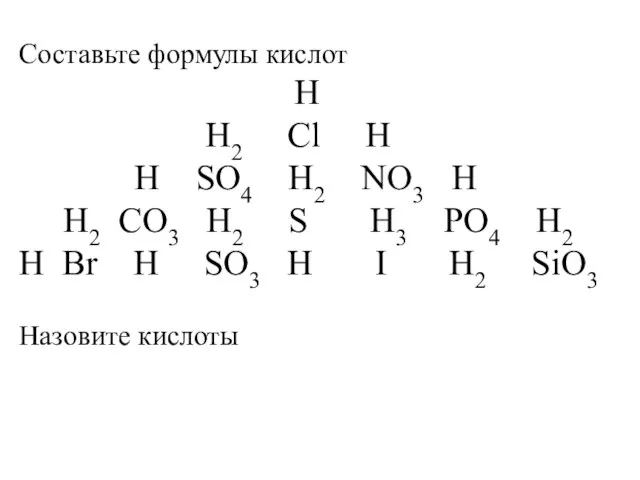 Составьте формулы кислот
Составьте формулы кислот Физико - химические основы получения лекарственных препаратов (лекция 4)
Физико - химические основы получения лекарственных препаратов (лекция 4) Гидрометаллургическое обескремнивание титанового сырья соединениями фтора
Гидрометаллургическое обескремнивание титанового сырья соединениями фтора Электролитическая диссоциация
Электролитическая диссоциация Углеводороды. Урок-игра
Углеводороды. Урок-игра Якісні реакції органічних речовин
Якісні реакції органічних речовин Липиды молока и молочных продуктов. Группы липидов
Липиды молока и молочных продуктов. Группы липидов Презентация на тему Природные источники углеводородов
Презентация на тему Природные источники углеводородов  Презентация по Химии "Белки как основа всего живого"
Презентация по Химии "Белки как основа всего живого"  Молярная масса вещества
Молярная масса вещества Буферные растворы
Буферные растворы Химия вокруг нас. 10 класс
Химия вокруг нас. 10 класс Получение и применение аренов
Получение и применение аренов Циклоалканы. Изомерия циклоалканов
Циклоалканы. Изомерия циклоалканов Расчеты по химическим уравнениям
Расчеты по химическим уравнениям Строение атома
Строение атома Оксид серы (VI)
Оксид серы (VI) Её величество – вода Интегрированный урок химии в 8 классе
Её величество – вода Интегрированный урок химии в 8 классе Красители vs пигменты
Красители vs пигменты Турнир Знатоков Химии
Турнир Знатоков Химии Производство аммиака
Производство аммиака Химический состав молока
Химический состав молока Классификация реакций и реагентов. Кислотные и основные свойства биомолекул
Классификация реакций и реагентов. Кислотные и основные свойства биомолекул Основания. Химические свойства.получение
Основания. Химические свойства.получение Введение. Тренажер
Введение. Тренажер Конкурс О, химия – ты муза вдохновения!
Конкурс О, химия – ты муза вдохновения!