Содержание
- 2. Элементы, входящие в состав клетки
- 3. Биогенные элементы O Кислород C Углерод H Водород N Азот S Сера P Фосфор
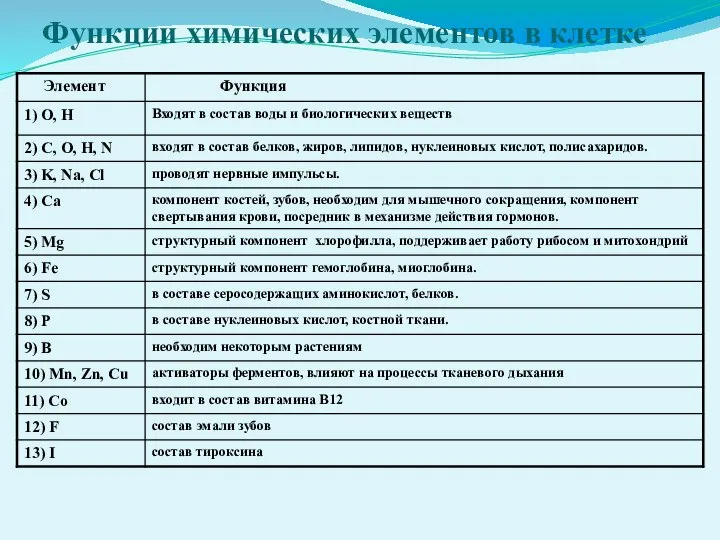
- 4. Функции химических элементов в клетке
- 5. Минеральные вещества Особенности строения минеральных солей а)в диссоциированном состоянии в виде катионов: К+, Na+, Ca2+, Mg
- 6. Функции минеральных солей Влияют на: Кислотно –щелочное равновесие (буферность) в организме Осмотическое давление, поступление воды в
- 7. Буферность – способность раствора сохранять определенную концентрацию водородных ионов (рН) Кислотность раствора определяется концентрацией в нем
- 8. Формы воды в клетке Свободная Межклеточные пространства Сосуды Вакуоли Полости органов Связанная Клеточные структуры Молекулы белка
- 9. Количество воды в клетке Первое место среди химических соединений В клетках развивающегося зародыша -90% В клетках
- 10. Количество воды в клетке В молодом организме человека и животного – 80 % от массы клетки;
- 11. Функции воды Обеспечивает тургор (упругость) клетки Участвует в терморегуляции Равномерно распределяет тепло по клетке (высокая теплопроводность)
- 12. Какова взаимосвязь строения и функции воды? Гидрофильные вещества – Гидрофобные вещества – Каков механизм растворения веществ
- 13. Свойства воды и ее биологическая роль
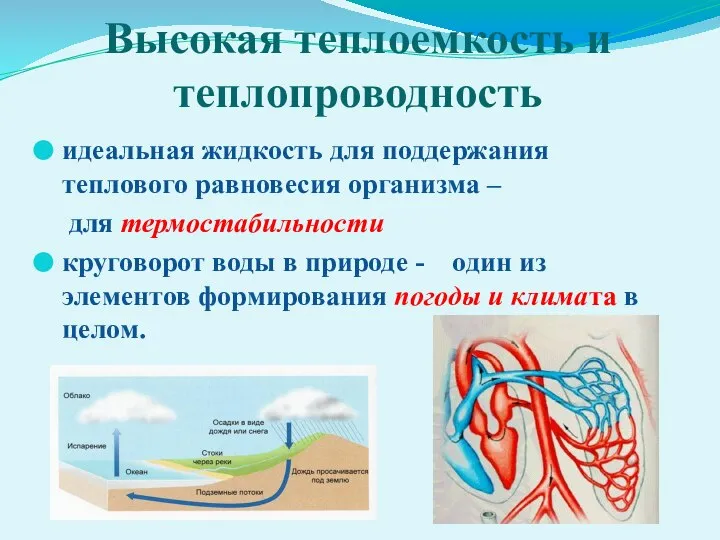
- 14. Высокая теплоемкость и теплопроводность идеальная жидкость для поддержания теплового равновесия организма – для термостабильности круговорот воды
- 15. Прозрачность в видимом участке спектра возможность фотосинтеза на небольшой глубине и, следовательно, возможность существования связанных с
- 16. Практическая полная несжимаемость благодаря силам межмолекулярного сцепления поддерживается форма организмов (тургорное давление, гидростатический скелет, амниотическая жидкость).
- 17. Подвижность молекул вследствие слабости водородных связей возможно проявление осмоса
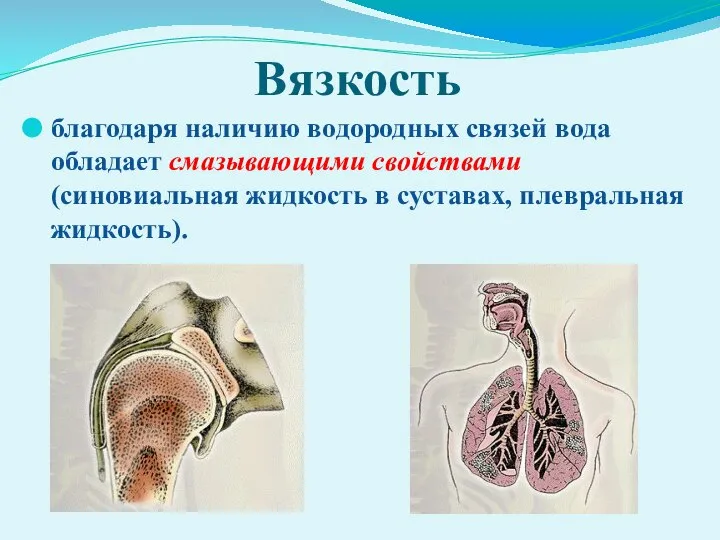
- 18. Вязкость благодаря наличию водородных связей вода обладает смазывающими свойствами (синовиальная жидкость в суставах, плевральная жидкость).
- 19. Благодаря полярности молекул: самый распространенный в природе растворитель среда протекания многих химических реакций в организме образует
- 20. Оптимальная для биосистем значение силы поверхностного натяжения водные растворы являются средством передвижения веществ в организме, которое
- 21. Расширение при замерзании лед легче воды, он образуется на поверхности водоемов и выполняет функцию теплоизоляции –
- 23. Скачать презентацию

















 Электролиз растворов и расплавов
Электролиз растворов и расплавов Состав атома
Состав атома Макро- и микромир
Макро- и микромир Аттестационная работа: Сравнение показателей качества меда разных производителей
Аттестационная работа: Сравнение показателей качества меда разных производителей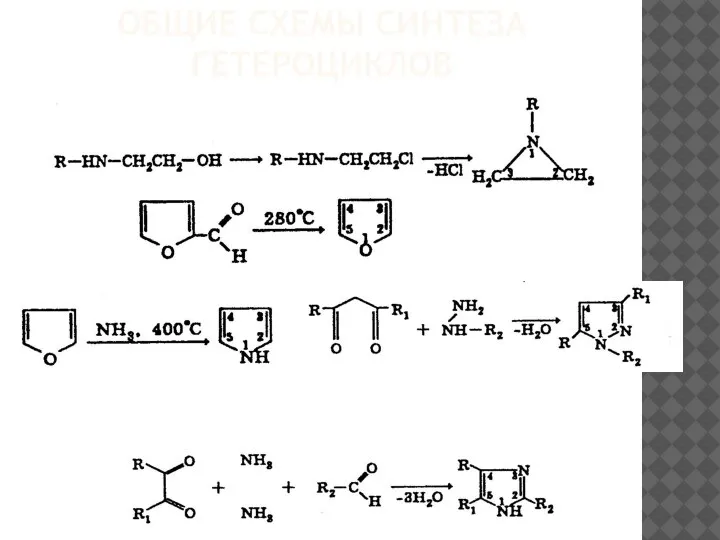 Общие схемы синтеза гетероциклов
Общие схемы синтеза гетероциклов Окислительно-восстановительные реакции. Степень окисления
Окислительно-восстановительные реакции. Степень окисления Презентация по Химии "Здоровьесберегающие технологии при изучении химии"
Презентация по Химии "Здоровьесберегающие технологии при изучении химии"  Презентация по Химии "Электрохимический ряд напряжений металлов. Общие химические свойства металлов"
Презентация по Химии "Электрохимический ряд напряжений металлов. Общие химические свойства металлов"  Гигиена воздуха
Гигиена воздуха Взаимодействие кислот с металлами. Кислоты-окислители
Взаимодействие кислот с металлами. Кислоты-окислители 9. Потомки светоносного элемента
9. Потомки светоносного элемента Химические средства защиты растений. Последствия применения пестицидов
Химические средства защиты растений. Последствия применения пестицидов Валентность
Валентность Альдегиды
Альдегиды Основные свойства и опасности нефти. Безопасность для танкеров
Основные свойства и опасности нефти. Безопасность для танкеров рН розчину
рН розчину Оксиды и гидроксиды металлов
Оксиды и гидроксиды металлов 42. Ионные уравнения
42. Ионные уравнения Понятие о предельных углеводородах. Алканы
Понятие о предельных углеводородах. Алканы Презентация на тему Научная химическая лаборатория Ломоносова
Презентация на тему Научная химическая лаборатория Ломоносова  Производство метанола
Производство метанола Rozcieńczanie i zatężanie roztworów
Rozcieńczanie i zatężanie roztworów Гетерофункциональные органические соединения
Гетерофункциональные органические соединения Применение алканов
Применение алканов Природные источники углеводородов. Нефть. Нахождение в природе,состав и физические свойства
Природные источники углеводородов. Нефть. Нахождение в природе,состав и физические свойства Мышьяк. История. Нахождение в природе
Мышьяк. История. Нахождение в природе Сравнительный анализ Фармакопейных статей для субстанций, представленных в мировых Фармакопеях
Сравнительный анализ Фармакопейных статей для субстанций, представленных в мировых Фармакопеях Моделирование строения химических соединений с использованием программного комплекса HyperChem 8.0
Моделирование строения химических соединений с использованием программного комплекса HyperChem 8.0