Содержание
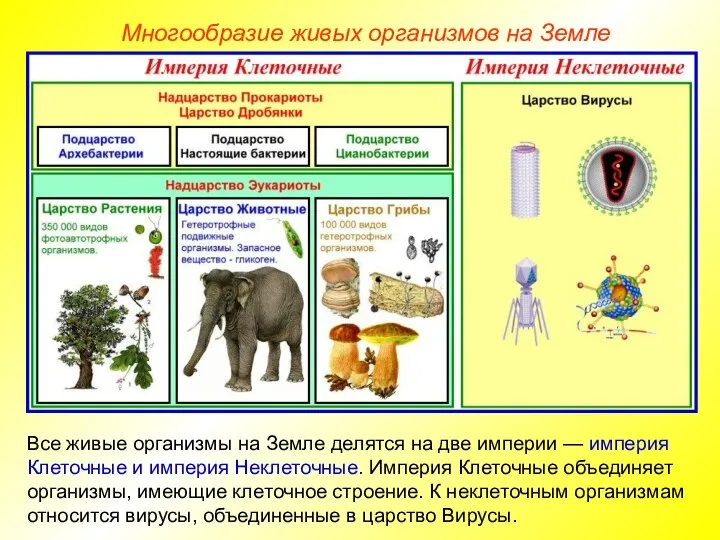
- 2. Многообразие живых организмов на Земле Все живые организмы на Земле делятся на две империи — империя
- 3. 1. Важнейший признак живого организма — способность к размножению, способность к передаче генетической информации следующему поколению.
- 4. 4. Пока организм жив, он воспринимает воздействия окружающей среды, под влиянием раздражителя происходит возбуждение и развивается
- 5. 1. Молекулярный, на котором изучаются органические и неорганические молекулы, их строение и функции в организме. 2.
- 6. 6. Организмы объединяются в популяции, популяции — в виды, формируется популяционно-видовой уровень, обеспечивающий сложные внутривидовые взаимоотношения.
- 7. Химический состав клетки
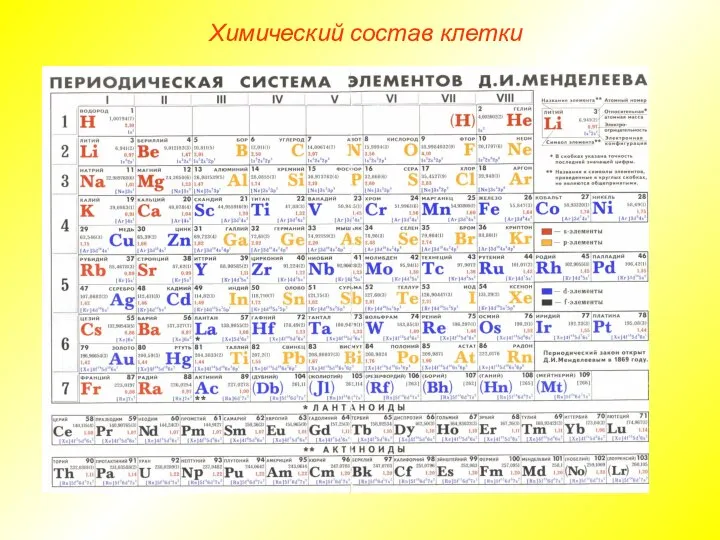
- 8. Химический состав клетки Все клетки, независимо от уровня организации, сходны по химическому составу. В живых организмах
- 9. Химический состав клетки
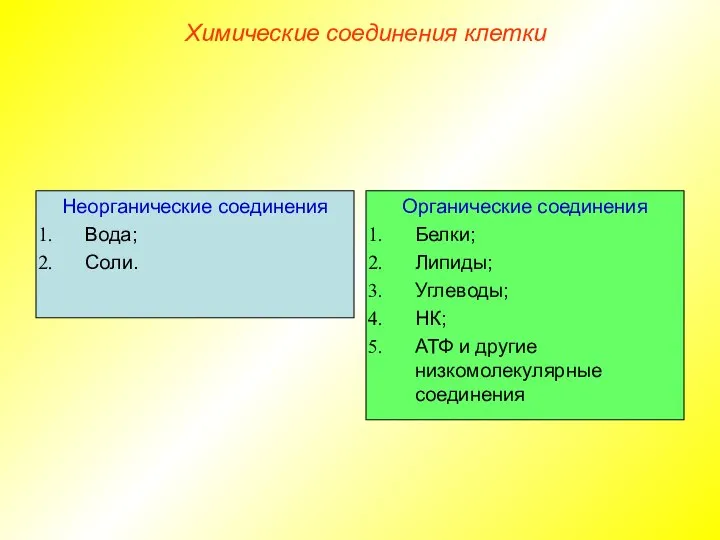
- 10. Неорганические соединения Вода; Соли. Органические соединения Белки; Липиды; Углеводы; НК; АТФ и другие низкомолекулярные соединения Химические
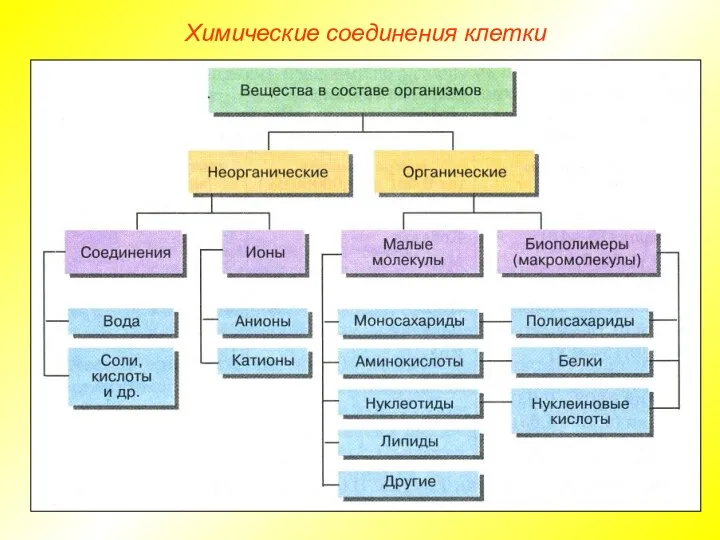
- 11. Химические соединения клетки
- 12. Химические соединения клетки Вода. Самое распространенное в живых организмах неорганическое соединение. Ее содержание колеблется в широких
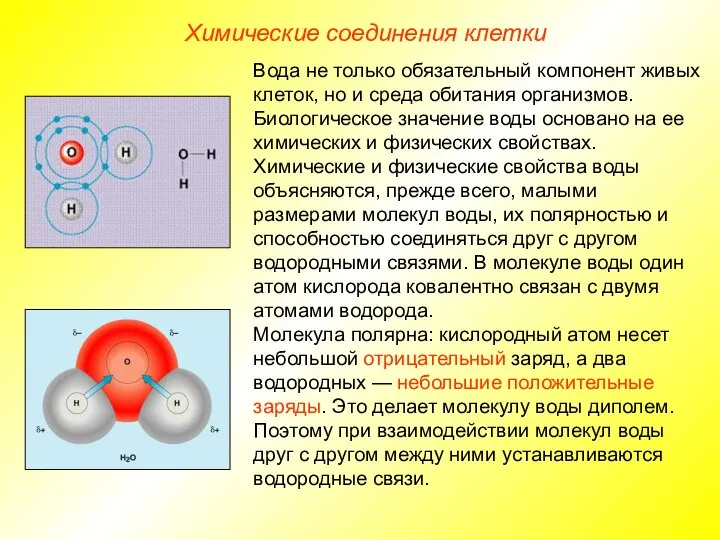
- 13. Химические соединения клетки Вода не только обязательный компонент живых клеток, но и среда обитания организмов. Биологическое
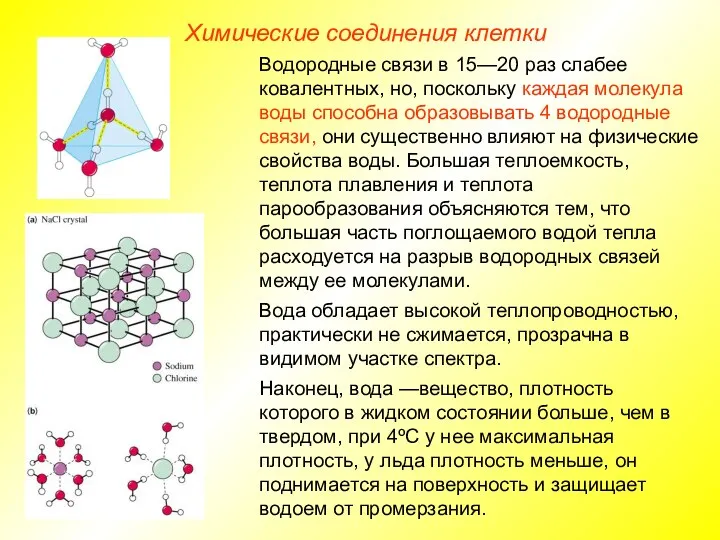
- 14. Химические соединения клетки Водородные связи в 15—20 раз слабее ковалентных, но, поскольку каждая молекула воды способна
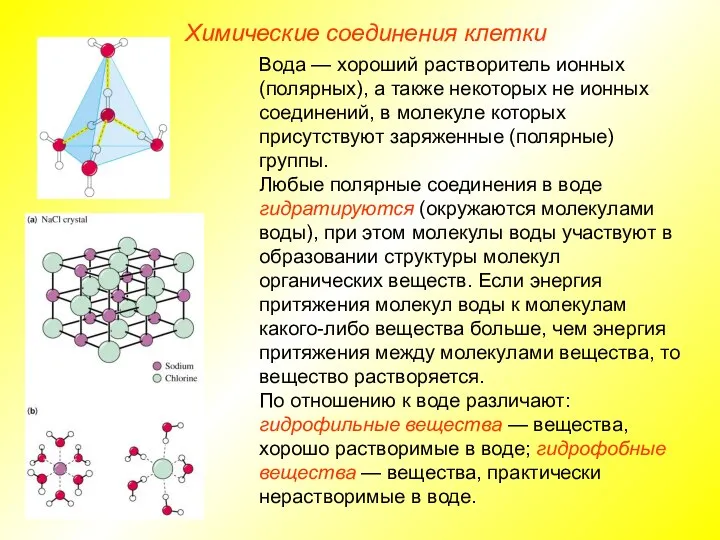
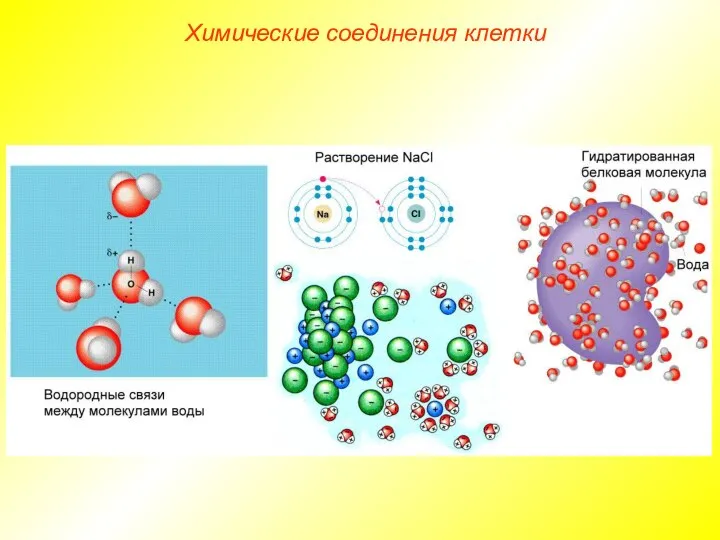
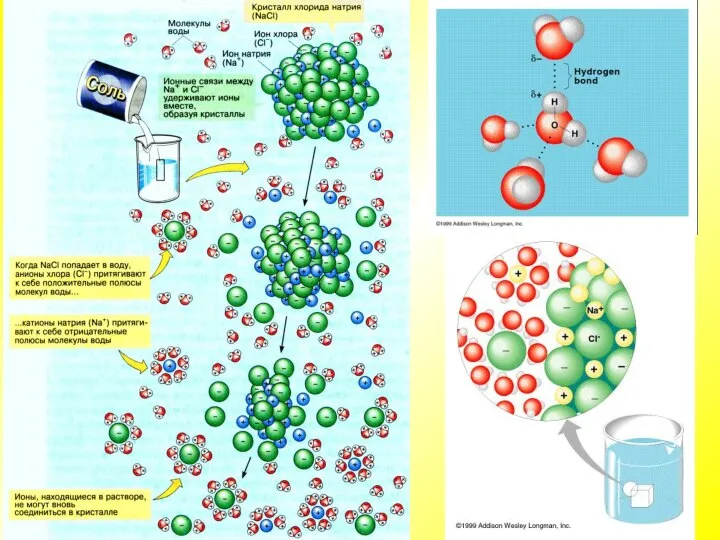
- 15. Химические соединения клетки Вода — хороший растворитель ионных (полярных), а также некоторых не ионных соединений, в
- 16. Химические соединения клетки
- 18. Химические соединения клетки Большинство биохимических реакций может идти только в водном растворе; многие вещества поступают в
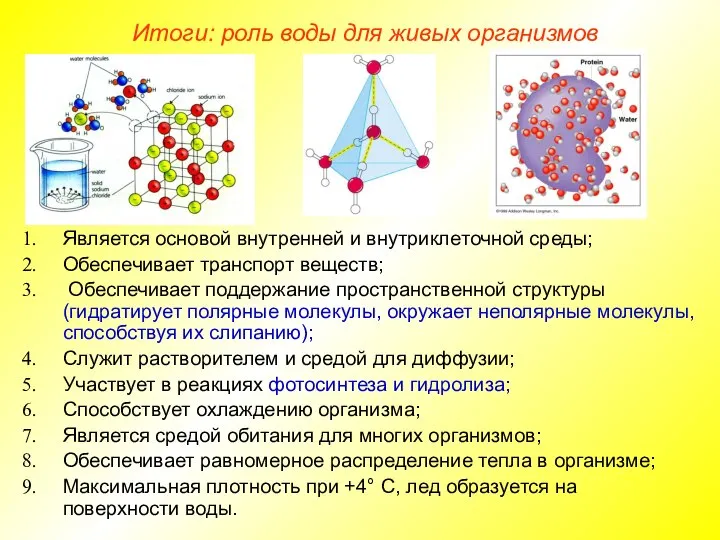
- 19. Является основой внутренней и внутриклеточной среды; Обеспечивает транспорт веществ; Обеспечивает поддержание пространственной структуры (гидратирует полярные молекулы,
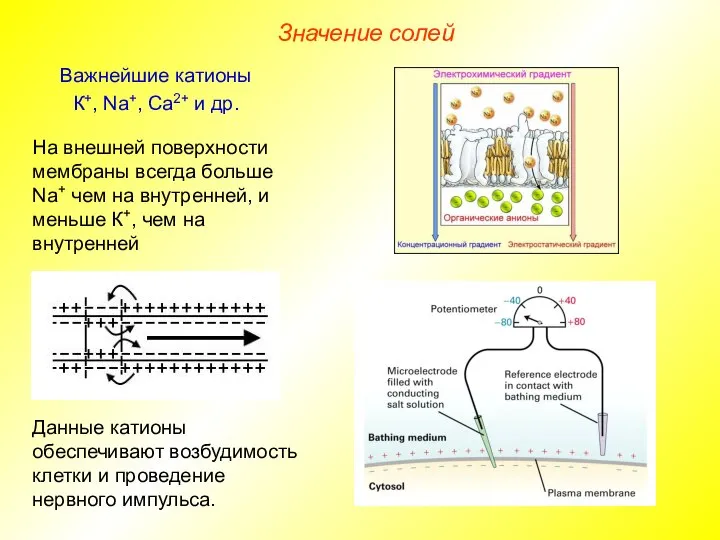
- 20. Значение солей Важнейшие катионы К+, Na+, Ca2+ и др. Данные катионы обеспечивают возбудимость клетки и проведение
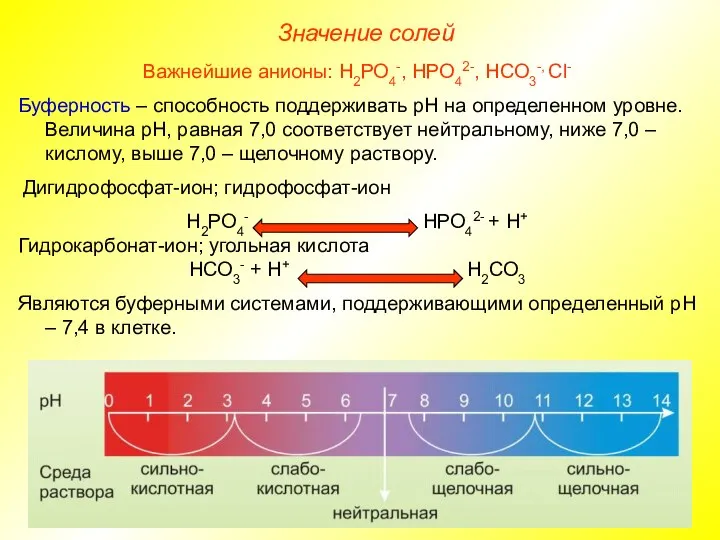
- 21. Значение солей Важнейшие анионы: Н2РО4-, НРО42-, НСО3-, Сl- Буферность – способность поддерживать рН на определенном уровне.
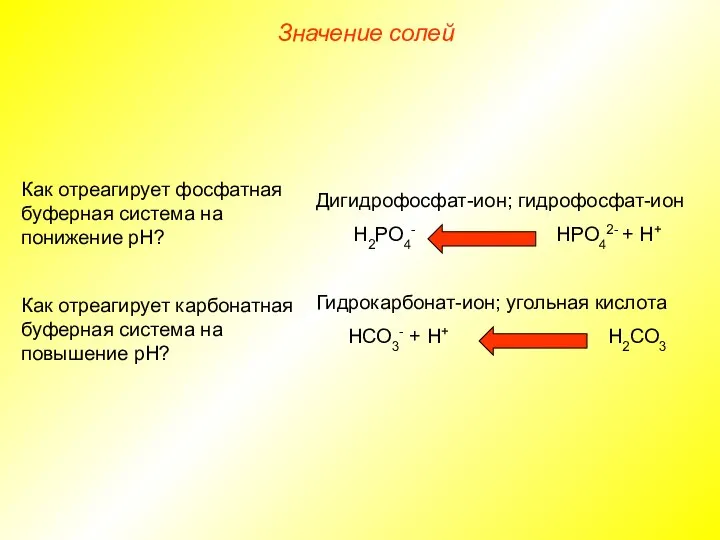
- 22. Дигидрофосфат-ион; гидрофосфат-ион Н2РО4- НРО42- + Н+ Гидрокарбонат-ион; угольная кислота НСО3- + Н+ Н2СО3 Как отреагирует фосфатная
- 23. Перечислите уровни организации живой материи. Какие четыре царства различают в империи Клеточные? Какие элементы называются биогенными?
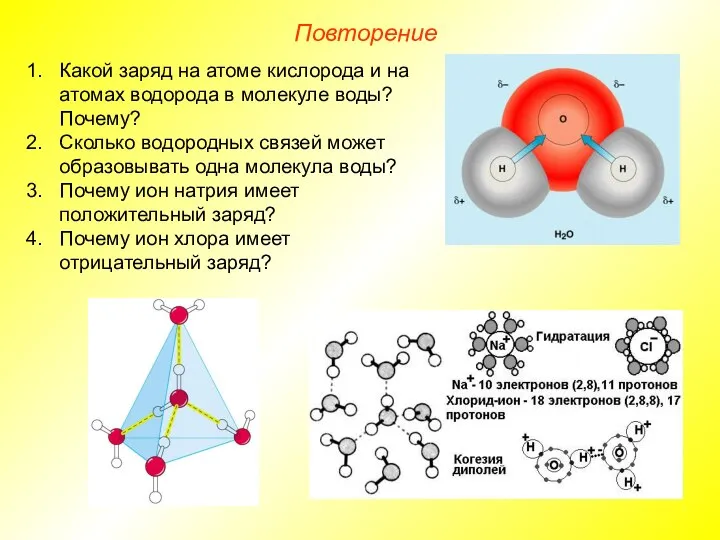
- 24. Повторение Какой заряд на атоме кислорода и на атомах водорода в молекуле воды? Почему? Сколько водородных
- 26. Скачать презентацию









 Химическая реакция
Химическая реакция Алотропия углерода
Алотропия углерода Химия и космос
Химия и космос Витамины и их роль в жизни людей
Витамины и их роль в жизни людей Химическое многоборье. 9 класс
Химическое многоборье. 9 класс Stroenie_atoma__1
Stroenie_atoma__1 Ароматические углеводороды - Арены
Ароматические углеводороды - Арены Чистые вещества и смеси
Чистые вещества и смеси Химический элемент Li
Химический элемент Li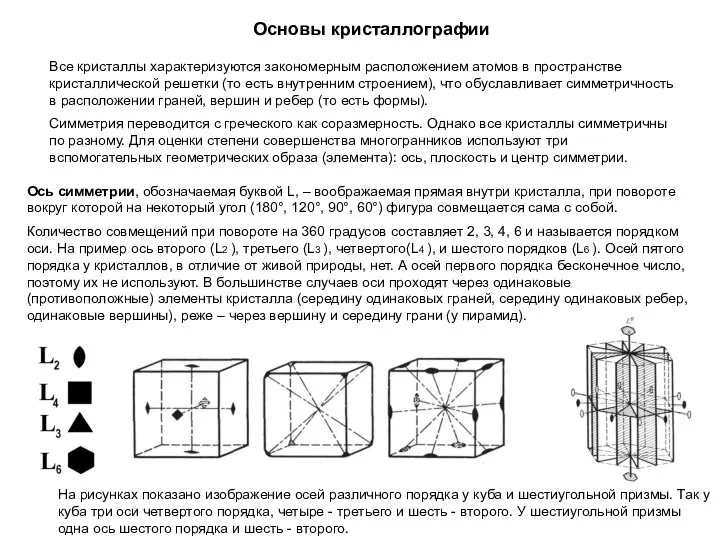 Основы кристаллографии
Основы кристаллографии Общая химическая технология. Определение размеров реакторов. Практическое занятие 8
Общая химическая технология. Определение размеров реакторов. Практическое занятие 8 Урок № 4
Урок № 4 Получение гидроген хлорида
Получение гидроген хлорида Презентация на тему Угарный газ
Презентация на тему Угарный газ  Диффузия в газах, жидкостях и твердых телах
Диффузия в газах, жидкостях и твердых телах Презентация на тему Оксид кремния
Презентация на тему Оксид кремния  Химическая связь и строение молекул
Химическая связь и строение молекул Аргументы к апелляции на ЕГЭ по химии 2021
Аргументы к апелляции на ЕГЭ по химии 2021 Обозначения групп симметрии по Шенфлису
Обозначения групп симметрии по Шенфлису Диэлектрики
Диэлектрики Алюминий. Из истории открытия
Алюминий. Из истории открытия Ковалентная неполярная связь
Ковалентная неполярная связь Минералы и их свойства
Минералы и их свойства 9 кл Урок 14 Ступінь дисоціації
9 кл Урок 14 Ступінь дисоціації Электромагнитное облучение. Радиоактивное загрязнение
Электромагнитное облучение. Радиоактивное загрязнение Полисахариды. Крахмал и целлюлоза
Полисахариды. Крахмал и целлюлоза Элемент протактиний
Элемент протактиний Хим_10_30_Производство_аммиака
Хим_10_30_Производство_аммиака