Содержание
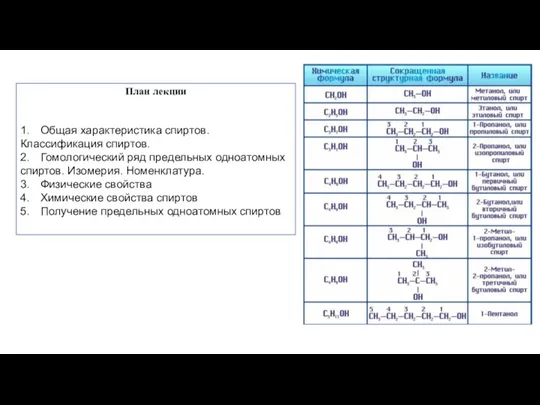
- 2. План лекции 1. Общая характеристика спиртов. Классификация спиртов. 2. Гомологический ряд предельных одноатомных спиртов. Изомерия. Номенклатура.
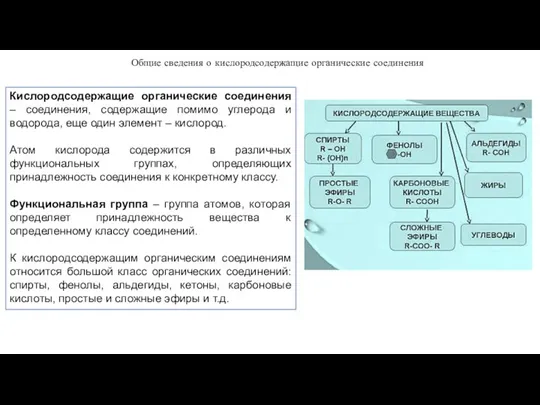
- 3. Кислородсодержащие органические соединения – соединения, содержащие помимо углерода и водорода, еще один элемент – кислород. Атом
- 4. Название этого класса происходит от латинского слова «дух вина». А с XVIII века наряду со словом
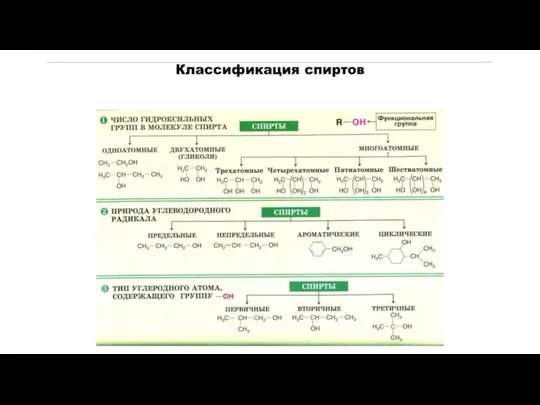
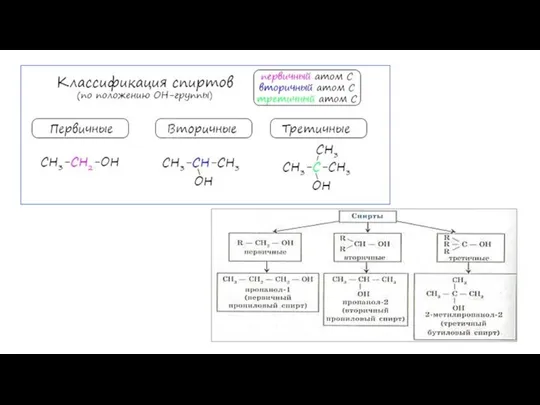
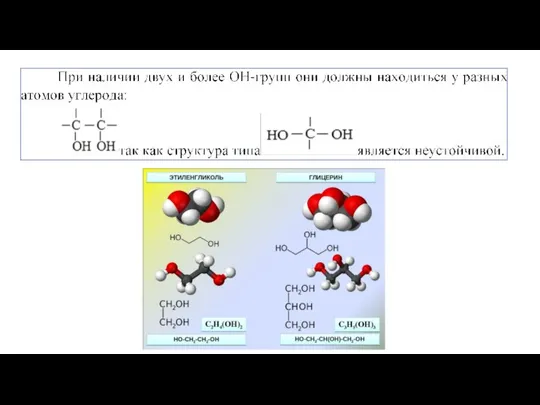
- 6. по числу гидроксильных групп (атомности) спирты
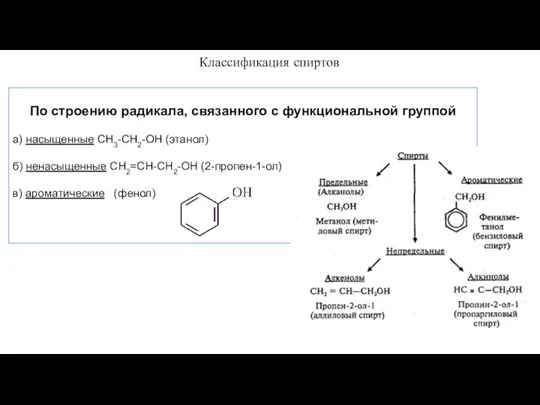
- 7. По строению радикала, связанного с функциональной группой а) насыщенные СН3-СН2-ОН (этанол) б) ненасыщенные СН2=СН-СН2-ОН (2-пропен-1-ол) в)
- 9. Общая формула – СnH2n+2O или CnH2n+1OH или R–OH, где R – углеводородный радикал . Предельные одноатомные
- 11. Гомологический ряд предельных одноатомных спиртов Первым членом гомологического ряда спиртов является метанол Н3С–ОН, каждый последующий член
- 12. изомерия
- 13. Номенклатура Название спиртов по заместительной номенклатуре ИЮПАК образуется от названия соответствующих алканов с добавлением суффикса -ол
- 15. В нумерации атомов углерода в главной цепи положение гидроксильной группы имеет приоритет перед положением кратных связей.
- 17. Низшие и средние члены ряда предельных одноатомных спиртов, содержащих от 1 до 11 атомов углерода, —
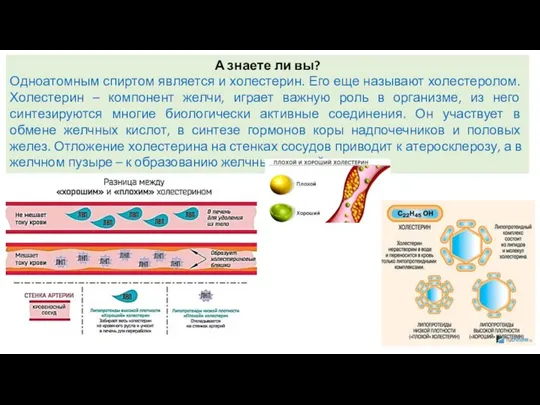
- 18. А знаете ли вы? Одноатомным спиртом является и холестерин. Его еще называют холестеролом. Холестерин – компонент
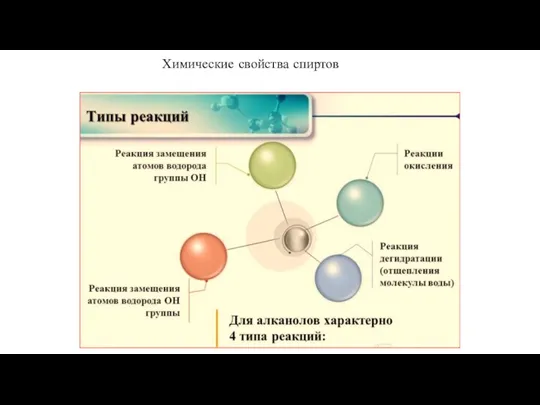
- 19. Химические свойства спиртов
- 20. Продукты замещения атома водорода гидроксильной группы спирта атомом металла называются алкоголятами.
- 21. Реакция с галогеноводородами Реакция с галогеноводородами протекают как реакции обмена: атом галогена замещает гидроксогруппу, образуется молекула
- 22. Реакции с кислотами В результате реакций спиртов с кислотами образуются различные эфиры.
- 23. Дегидратация спиртов Дегидратация спиртов (отщепление воды) идет при повышенной температуре в присутствии серной кислоты (водоотнимающего) компонента.
- 24. Окисление спиртов Качественной реакцией на спирты является взаимодействие с оксидом меди II. В ходе такой реакции
- 25. Вторичные и третичные спирты определяются другой качественной реакцией с хлоридом цинка II и соляной кислотой. В
- 26. Первичные спирты окисляются до альдегидов, а вторичные - до кетонов. Альдегиды могут быть окислены далее -
- 27. Кислотные свойства многоатомных спиртов Важным отличием многоатомных спиртов от одноатомных является их способность реагировать со щелочами
- 28. Получение предельных одноатомных спиртов В реакциях галогеналканов со спиртовым раствором щелочи получаются - алкены, а в
- 29. Гидратация алкенов Присоединения молекулы воды (HOH) протекает по правилу Марковникова. Атом водорода направляется к наиболее гидрированному
- 30. Восстановление карбонильных соединений В результате восстановления альдегидов и кетонов получаются соответственно первичные и вторичные спирты.
- 31. Получение этанола брожением глюкозы В ходе брожения глюкозы выделяется углекислый газ и образуется этанол.
- 33. Скачать презентацию






















 Химия и производство. Химическая промышленность
Химия и производство. Химическая промышленность Простые вещества в стране Химляндии. 8 класс
Простые вещества в стране Химляндии. 8 класс Двовимірний ямр. Основні принципи
Двовимірний ямр. Основні принципи (+)-Plumisclerin A. Плюмисклин А
(+)-Plumisclerin A. Плюмисклин А Гидролиз солей
Гидролиз солей Язык естествознания. Химия
Язык естествознания. Химия Презентация по Химии "Ароматы и чем они «пахнут»"
Презентация по Химии "Ароматы и чем они «пахнут»"  Углеводы: моно-, ди-, полисахариды
Углеводы: моно-, ди-, полисахариды Презентация на тему Растворы (11 класс)
Презентация на тему Растворы (11 класс)  Ионизирующее излучение и окружающая среда
Ионизирующее излучение и окружающая среда Дизайн молекулярных магнетиков
Дизайн молекулярных магнетиков Вода. Строение молекулы воды. Анализ и синтез воды
Вода. Строение молекулы воды. Анализ и синтез воды Кальций и его соединения. 9 класс
Кальций и его соединения. 9 класс Химические свойства и получение спиртов
Химические свойства и получение спиртов Презентация на тему Валентные состояния атома углерода
Презентация на тему Валентные состояния атома углерода  9 кл Урок 7 Розчинність речовин
9 кл Урок 7 Розчинність речовин Карбоновые кислоты
Карбоновые кислоты Простые и сложные вещества. Основные классы неорганических веществ
Простые и сложные вещества. Основные классы неорганических веществ Презентация на тему Атомы химических элементов
Презентация на тему Атомы химических элементов  Получение галогенов. Биологическое значение и применение галогенов и их соединений
Получение галогенов. Биологическое значение и применение галогенов и их соединений Силумины. Виды силуминов
Силумины. Виды силуминов Степень окисления
Степень окисления Амфотерность. Амфотерные соединения
Амфотерность. Амфотерные соединения Физическая и коллоидная химия
Физическая и коллоидная химия Жиры. Открытие жиров
Жиры. Открытие жиров khim
khim Органические вещества
Органические вещества Неметаллические материалы
Неметаллические материалы