Содержание
- 2. Решите цепочку превращений: 1). ZnS ← Zn →ZnCl2 →Zn(OH)2 → ZnO →ZnSO4 2). Li → Li2О
- 3. Решите задачу. Какую массу железа можно получить алюминотермическим методом из 100 г оксида железа (II), содержащего
- 4. Металлы в природе §36 1. Какой металл встречается в земной коре в чистом виде: а) калий,
- 5. Получение металлов §36 2. Какой процесс называют электрометаллургией: а) получение металлов из растворов солей, б) получение
- 6. Получение металлов §36 3. Какие восстановители используют для восстановления металлов из их оксидов: а) С, СО2,
- 7. Щелочные и щёлочно-земельные металлы §30-31 4. Какие металлы относятся к щелочным: а) Na, Mg, Al; б)
- 8. Изменение металлических свойств периодической системе 5. В каком ряду элементов радиус атомов уменьшается: а) Rb,Cs, Na
- 9. Сплавы металлов 13. Установите соответствие между компонентами сплава и названием сплава: 1. железо и углерод А)дюралюминий
- 10. Строение атомов металлов 11. Установите соответствие между элементом и его электронной формулой: 1. Вa А) 6s2
- 11. Восстановительные свойства металлов §29 6. У какого металла сильнее выражены восстановительные свойства: а) Au, б) Ba,
- 12. Химические свойства металлов §29 6'. Какой металл не реагирует с растворами солей: а) Fe, б) Сa,
- 13. Биологическая роль металлов §30,31,33,34 Состав гемоглобина Построение скелета Стимулятор обмена веществ Участие в свёртываемости крови Содержится
- 14. Химические свойства металлов §29,30,31,33,34 9. Определите коэффициент перед восстановителем в уравнении: Ва + HCl = ВaCl2
- 15. Применение металлов §30,31,33,34 Для получения других металлов Производство посуды Изготовление бенгальских огней Получение чугуна и стали
- 16. Соединения металлов §30,31,33,34 11. Установите соответствие между знаком элемента и его высшим оксидом: 1. Ra А)
- 17. Соединения металлов §30,31,33,34 12. Установите соответствие между формулой гидроксида и его характером: 1. LiОН А) кислотный
- 18. Соединения металлов §30,31,33,34 13. Установите соответствие меду формулой вещества и его названием: 1. Al2О3 А) сода
- 20. Скачать презентацию

















 Химия – это область чудес
Химия – это область чудес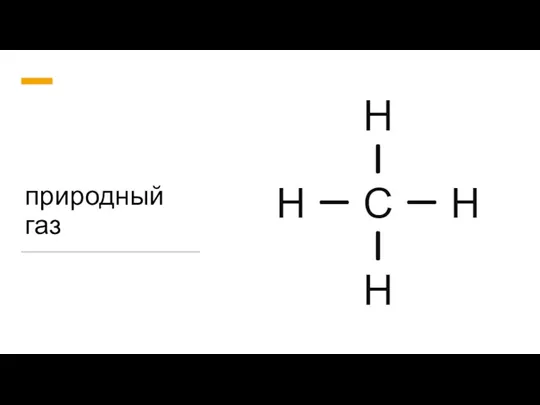 Природный газ
Природный газ Сера - химический элемент и простое вещество
Сера - химический элемент и простое вещество Реакции ионного обмена
Реакции ионного обмена Актиний. Нахождение в природе
Актиний. Нахождение в природе Алкины
Алкины Углерод и его аллотропные модификации. Органическая химия - химия углерода
Углерод и его аллотропные модификации. Органическая химия - химия углерода Выбор материала для изготовления зубчатых колес
Выбор материала для изготовления зубчатых колес Кристаллы. Виды
Кристаллы. Виды Аллотропия
Аллотропия Степень окисления. Составление формул бинарных соединений. 8 класс
Степень окисления. Составление формул бинарных соединений. 8 класс 3bc28ca0711047a6880d20a6763f17db
3bc28ca0711047a6880d20a6763f17db Ионная химическая связь
Ионная химическая связь Hydroxidy. Vlastnosti
Hydroxidy. Vlastnosti Валентные возможности атомов элементов
Валентные возможности атомов элементов Валентность
Валентность Экспериментальные методы изучения кинетики химических реакции
Экспериментальные методы изучения кинетики химических реакции Судың диссоциациясы
Судың диссоциациясы Кристаллизация и десублимация
Кристаллизация и десублимация Неоднородность по молекулярной массе. Полидисперсность. Содержание фракции
Неоднородность по молекулярной массе. Полидисперсность. Содержание фракции Закон постоянства состава веществ. Химические формулы. (8 класс)
Закон постоянства состава веществ. Химические формулы. (8 класс) Презентация на тему Решение задач "выход продукта от теоретически возможного"
Презентация на тему Решение задач "выход продукта от теоретически возможного"  Развитие ассоциативного мышления на уроках химии
Развитие ассоциативного мышления на уроках химии Химия элементов (IБ) группы
Химия элементов (IБ) группы alkany_stroenie_nomenklatura_izomeriya_10_klass (3)-1
alkany_stroenie_nomenklatura_izomeriya_10_klass (3)-1 Расчет по химическим уравнениям
Расчет по химическим уравнениям Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Основы теории сплавов. Типы сплавов (твердые растворы, сплавы-смеси, сплавы- химические соединения. Диаграммы
Основы теории сплавов. Типы сплавов (твердые растворы, сплавы-смеси, сплавы- химические соединения. Диаграммы