отдачи или принятия электрона.
Правила:
1. Степень окисления элемента в простом веществе равна 0.
H20 ; O20 ; F20 ; Cl20 ; Ca0.
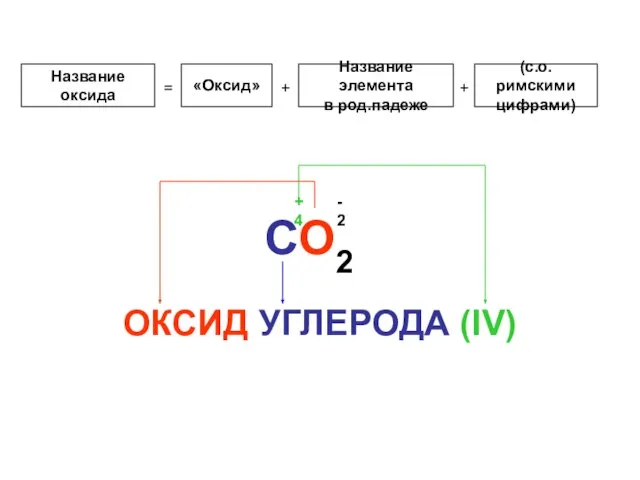
2. Степень окисления некоторых элементов в соединении:
- H+1
- О-2
степень окисления металлов IA, IIA группы и алюминия совпадает с номером группы:
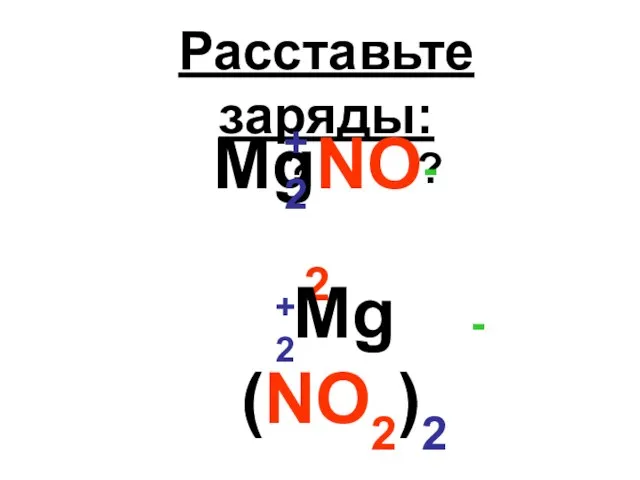
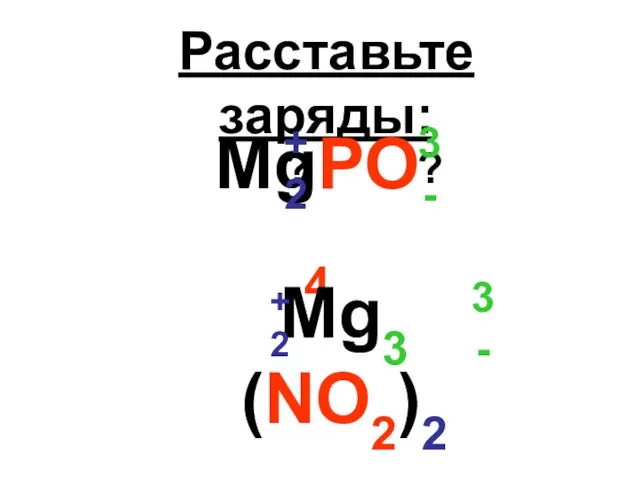
Na+1 ; K+1 ; Ca+2 ; Mg+2 ; Ba+2 ; Al+3 .
3. Сумма степеней окисления элементов в соединении, с учетом коэффициентов, равна 0.
H+1; О-2; Na+1 ; K+1 ; Ca+2 ; Mg+2 ; Ba+2 ; Al+3 .
H2СO3
Пример:
1. Расставляем степени окисления элементов, которые можем определить по правилу 2.
H ;
+1
О
-2
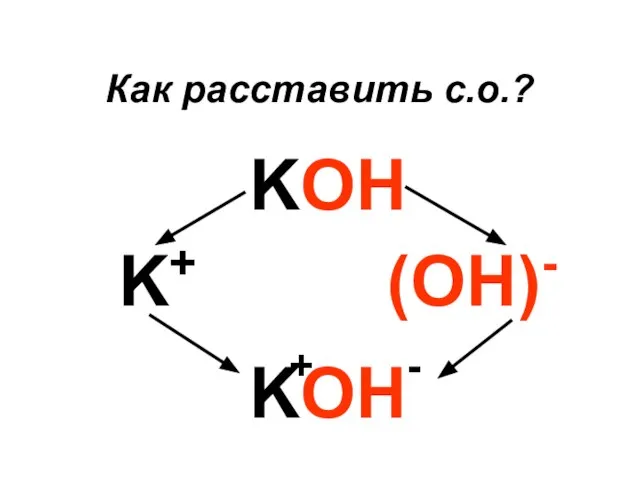
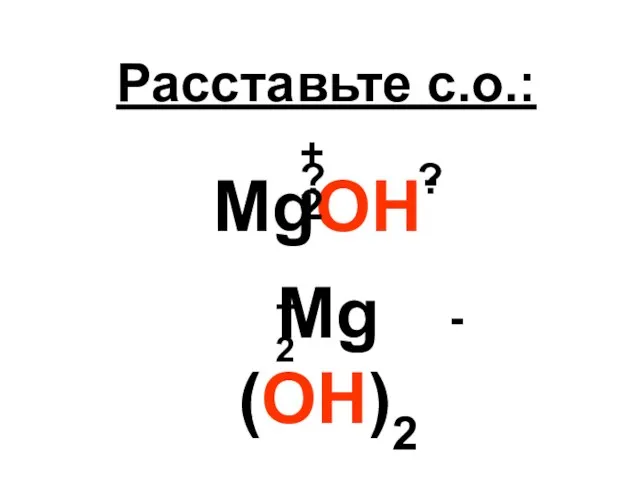
2. Степень окисления элемента, у которого пока ее не можем определить , обозначим за X
3. Составляем и решаем уравнение. Правило 3.
+1
-2
Х
2 . (+1) + Х + 3 . (-2) = 0
2 + Х - 6 = 0
Х = +4
+4
Тема: Степень окисления.



 Ацетиленовые углеводороды. Алкины
Ацетиленовые углеводороды. Алкины Металлы в организме человека
Металлы в организме человека Физические механизмы образования кристаллов
Физические механизмы образования кристаллов Физика полимеров Ч1
Физика полимеров Ч1 Минералы. Лекция 02
Минералы. Лекция 02 d-элементы.Распространение в природе и основные материалы
d-элементы.Распространение в природе и основные материалы Спирты и фенолы
Спирты и фенолы Органические соединения
Органические соединения Презентация на тему Неогранические соединения. Периодическая таблица
Презентация на тему Неогранические соединения. Периодическая таблица  Презентация на тему Полимеразная цепная реакция
Презентация на тему Полимеразная цепная реакция  Металлы. Повторение
Металлы. Повторение Периодическая система
Периодическая система Сравнительный анализ Фармакопейных статей для субстанций, представленных в мировых Фармакопеях
Сравнительный анализ Фармакопейных статей для субстанций, представленных в мировых Фармакопеях Фізика гірських порід і процесів. Хімічні зв'язки в мінералах. Іонний зв'язок
Фізика гірських порід і процесів. Хімічні зв'язки в мінералах. Іонний зв'язок Электролитическая диссоциация веществ Реакции ионного обмена и условия их протекания
Электролитическая диссоциация веществ Реакции ионного обмена и условия их протекания Взаимодействие цинка с разбавленной соляной кислотой. Лабораторный опыт. Шаблон
Взаимодействие цинка с разбавленной соляной кислотой. Лабораторный опыт. Шаблон Азот
Азот Почему амины считают органическими основаниями?
Почему амины считают органическими основаниями? Ferrum железо
Ferrum железо Презентация на тему Окислительно-восстановительные реакции: общие сведения
Презентация на тему Окислительно-восстановительные реакции: общие сведения  Трёхкомпонентные системы. Закон распределения. Экстракция. Свойства разбавленных растворов неэлектролитов
Трёхкомпонентные системы. Закон распределения. Экстракция. Свойства разбавленных растворов неэлектролитов Электрохимия. Предмет и задачи электрохимии. Теория растворов электролитов
Электрохимия. Предмет и задачи электрохимии. Теория растворов электролитов Чистые вещества и смеси. Использование химического анализа
Чистые вещества и смеси. Использование химического анализа Современные области применения изотопной продукции
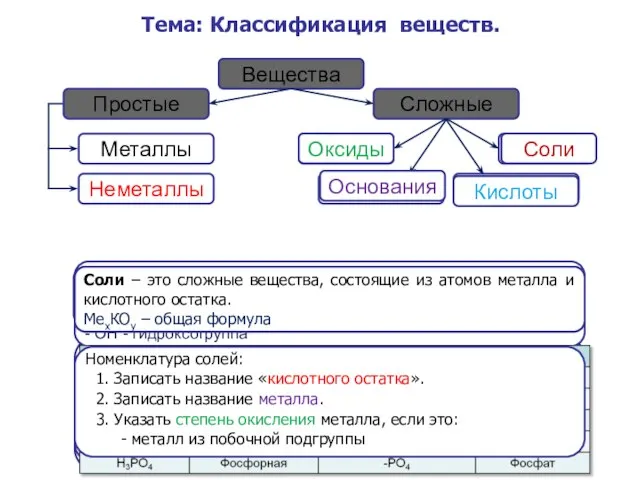
Современные области применения изотопной продукции Классы неорганических веществ
Классы неорганических веществ Кислоты 9 класс
Кислоты 9 класс ad8c00e7ea114b35a6fc29426ea31646 (1)
ad8c00e7ea114b35a6fc29426ea31646 (1) Kristālisku vielu uzbūve
Kristālisku vielu uzbūve