Содержание
- 2. Повторение пройденного:
- 3. Повторение пройденного
- 4. Самостоятельная работа Составить уравнения процессов электролиза раствора солей: Сульфата калия, сульфида натрия Нитрата цинка фторида серебра
- 5. Результат: прямые потери массы металла; косвенные потери - утрата важнейших свойств. Ежегодно в мире «теряется» до
- 6. Коррозия - самопроизвольное разрушение поверхности металлов (сплавов) под влиянием химического и электрохимического воздействия окружающей среды. окислительно-восстановительный
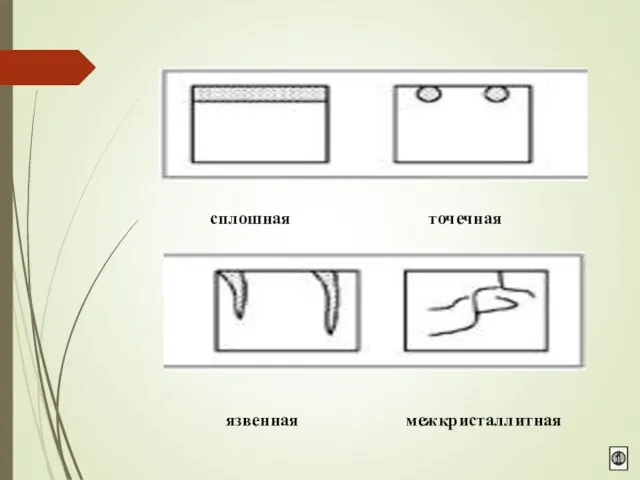
- 7. По характеру разрушения сплошная (общая): равномерная, неравномерная локальная(местная): точечная, пятнами, язвами, подповерхностная, сквозная и др. Виды
- 8. язвенная межкристаллитная сплошная точечная
- 9. Причины коррозии - химические и электрохимические процессы окисления, происходящие на поверхности металлических тел при их взаимодействии
- 10. Химическая коррозия металл разрушается в результате его химического взаимодействия с агрессивной средой (сухими газами, жидкостями-неэлектролитами). Образование
- 11. Коррозия металла на влажном воздухе Образующиеся на аноде ионы Fe2+ окисляются до Fe3+ : 4Fe2+ (водн.)
- 12. Электрохимическая коррозия - в среде электролита возникает электрический ток при контакте двух металлов (или на поверхности
- 13. Защита от коррозии Изоляция металла от среды Изменение состава металла (сплава) Изменение среды
- 14. Барьерная защита - механическая изоляция поверхности при использовании поверхностных защитных покрытий : неметаллических (лаки, краски, смазки,
- 15. Изменение состава металла (сплава) Протекторная защита добавление в материал покрытия порошковых металлов, создающих с металлом донорские
- 16. Пассивация поверхности Введение веществ, замедляющих коррозию (ингибиторов): для кислотной коррозии: азотсодержащие органические основания, альдегиды, белки, серосодержащие
- 18. Сплавы Сплавы – это системы из двух или нескольких металлов (или металлов и неметаллов), обладающие по
- 19. По способу образования различают: Химические соединения – близкие по строению металлы (AuZn, MgPb), Твердые растворы: –
- 20. Сталь – сплав железа с добавками углерода, кремния и других металлов и неметалов (до 2,5%)
- 21. Сталь используется в автомобильной промышленности
- 22. Инструментальная сталь
- 23. Сталь используется в строительной промышленности
- 24. Хирургические инструменты
- 25. Бронза – сплав меди и олова.
- 26. Дюралюминий – сплав алюминия с небольшими добавками меди, магния, марганца и кремния.
- 27. Золото используется в сплавах, обычно с серебром или медью.
- 28. Томпак – ”поддельное золото” – сплав меди и цинка, часто используемый для имитации золота
- 29. Сплав Вуда (висмут, свинец, олово, кадмий) используется при пайке
- 30. Монель-металл (медно-никелевый сплав) используется для изготовления химического оборудования, а также в промышленности, например в паровых турбинах
- 31. Белая латунь – сплав меди и цинка
- 33. Скачать презентацию





























 Химические формулы
Химические формулы 9-8 кислоты в свете ТЭД (1)
9-8 кислоты в свете ТЭД (1) Спирты
Спирты Адсорбционно-десорбционные взаимодействия фосфатов кальция и аминокислот
Адсорбционно-десорбционные взаимодействия фосфатов кальция и аминокислот Соли как производные кислот и оснований
Соли как производные кислот и оснований Интерактивная интеллектуальная игра Юный химик
Интерактивная интеллектуальная игра Юный химик Класс оксиды
Класс оксиды Обобщение знаний об углеводородах
Обобщение знаний об углеводородах ЕГЭ по химии: документы, регламентирующие структуру и содержание контрольных измерительных материалов
ЕГЭ по химии: документы, регламентирующие структуру и содержание контрольных измерительных материалов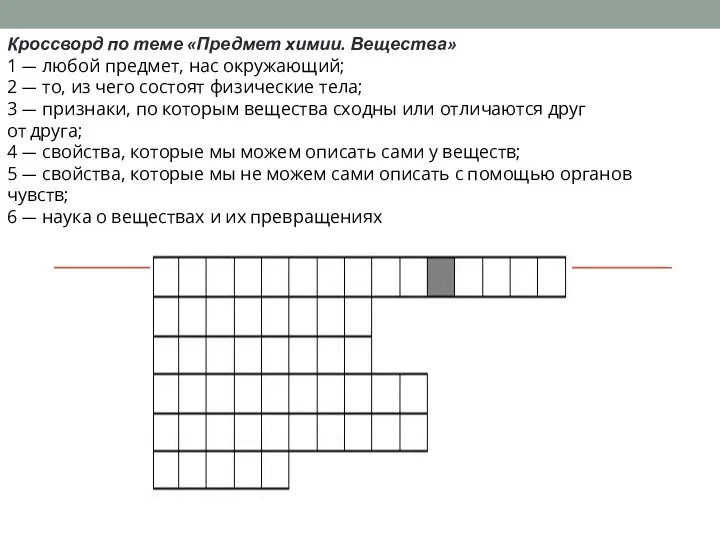 Предмет химии. Вещества
Предмет химии. Вещества 3bc28ca0711047a6880d20a6763f17db
3bc28ca0711047a6880d20a6763f17db Общая характеристика оксидов
Общая характеристика оксидов Золото
Золото Органическая химия. Ароматические углеводороды
Органическая химия. Ароматические углеводороды Методы получения нафтиридинов (всех изомеров)
Методы получения нафтиридинов (всех изомеров) Нефть и её переработка
Нефть и её переработка Оксид кремния
Оксид кремния Основания: номенклатура, классификация, применение, физические свойства
Основания: номенклатура, классификация, применение, физические свойства Алмаз. Свойства алмазов
Алмаз. Свойства алмазов Презентация на тему Соединения серы
Презентация на тему Соединения серы  Свойства солей, оксидов, оснований
Свойства солей, оксидов, оснований Модель химического образования на основе технологического подхода. Методическая система учителя химии
Модель химического образования на основе технологического подхода. Методическая система учителя химии Техника титрования и лабораторная посуда
Техника титрования и лабораторная посуда Уровень С1 в ГИА
Уровень С1 в ГИА Задачи. Периодическая система. Строение атома. Повторение
Задачи. Периодическая система. Строение атома. Повторение Азотсодержащие гетероциклические соединения пиррол
Азотсодержащие гетероциклические соединения пиррол Предельные углеводороды. Тест 19
Предельные углеводороды. Тест 19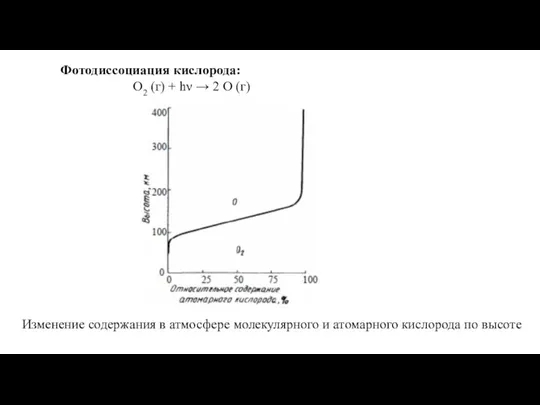 Фотодиссоциация кислорода
Фотодиссоциация кислорода