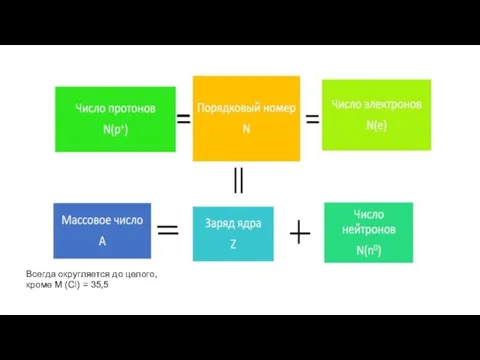
Слайд 2Всегда округляется до целого, кроме M (Cl) = 35,5
Слайд 5химические элементы
атомы с одинаковым зарядом ядра
Изотопы – атомы с одинаковым набором протонов

и электронов, но с другим количество нейтронов → изменяется массовое число
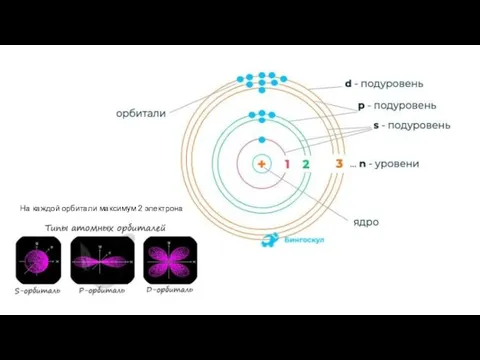
Слайд 6На каждой орбитали максимум 2 электрона
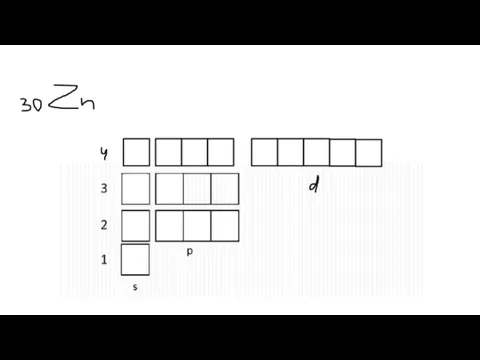
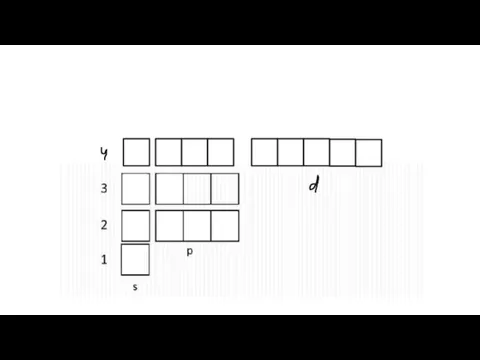
Слайд 7Электронная диаграмма
Электронная формула
Электронная конфигурация

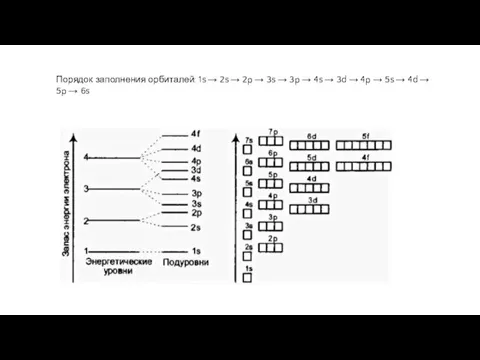
Слайд 8правила заполнения электронных орбиталей
Сперва следует заполнить орбитали с наименьшей энергией, и только

после переходить к энергетически более высоким
На орбитали (в одной "ячейке") не может располагаться более двух электронов
Орбитали заполняются электронами так: сначала в каждую ячейку помещают по одному электрону, после чего орбитали дополняются еще одним электроном с противоположным направлением
Порядок заполнения орбиталей: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s
Слайд 9максимальное число электронов на подуровнях
2 - максимальное число электронов на s-подуровне (1

орбиталь)
6 - максимальное число электронов на p-подуровне (3 орбитали)
10 - максимальное число электронов на d-подуровне (5 орбиталей)
14 - максимальное число электронов на f-подуровне (7 орбиталей)
Слайд 10как понять, сколько электронов и как они расположены
По таблице Менделеева
Порядковый номер –

суммарное число электронов в атоме
Номер периода – число уровней
Номер группы – число электронов на последнем (самом внешнем) уровне
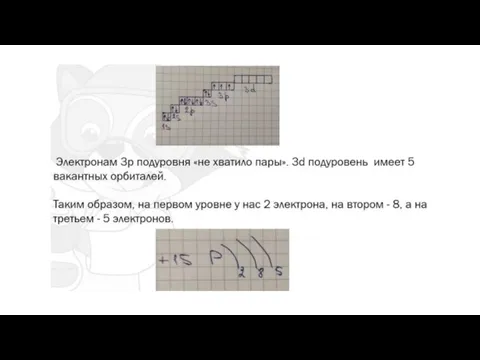
Слайд 18валентные электроны
— электроны в атоме, которые могут участвовать в образовании химической

связи («ищут пару»)
Слайд 20Порядок заполнения орбиталей: 1s → 2s → 2p → 3s → 3p
→ 4s → 3d → 4p → 5s → 4d → 5p → 6s
Слайд 23проскок/провал электрона
- переход электрона с внешнего, более высокого энергетического уровня, на предвнешний,

энергетически более низкий. Это связано с большей энергетической устойчивостью получающихся при этом электронных конфигураций (атом «тратит» меньше энергии, чтобы удерживать себя)
медь, хром, серебро, золото, молибден, платина, палладий
Слайд 24Электронно-графическая формула атома меди Cu

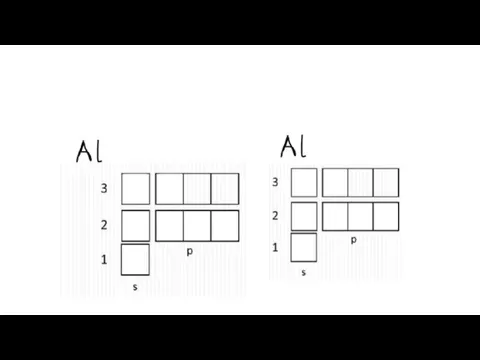
Слайд 26основное и возбужденное состояние атомов
Возбужденное состояние: все электроны на внешнем уровне распариваются

и занимают свободные ячейки (вакантные орбитали) по одному, становясь валентными (могут образовывать связи). Это состояние для атома нестабильно
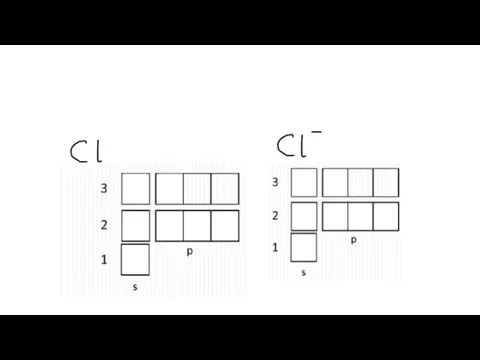
Слайд 27Электронная конфигурация ионов
Ионы – заряженные частицы
Отрицательный ион – анион – когда атом

получает электроны (минус – избыток электронов, недостаток протонов)
Положительный ион – катион – когда атом отдает электроны (плюс – недостаток электронов, избыток протонов)























 Неорганический мозговой штурм
Неорганический мозговой штурм Альдегиды и кетоны
Альдегиды и кетоны Проектная деятельность учащихся по химии
Проектная деятельность учащихся по химии Химия вокруг нас и для нас
Химия вокруг нас и для нас Уравнение материального баланса технологического процесса. (Лекция 3)
Уравнение материального баланса технологического процесса. (Лекция 3) Кинетическое лимитирование роста и жизненные стратегии микроорганизмов
Кинетическое лимитирование роста и жизненные стратегии микроорганизмов Алкадиены
Алкадиены Кинетика гомогенных реакций
Кинетика гомогенных реакций Презентация на тему Основные положения МКТ
Презентация на тему Основные положения МКТ 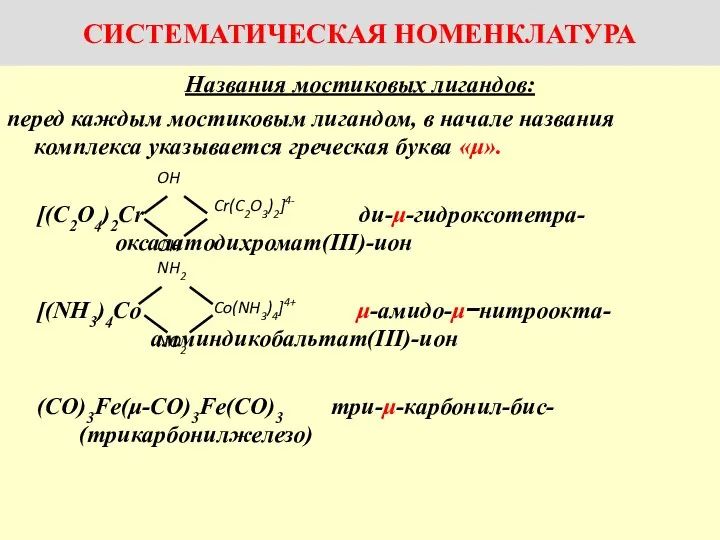 Названия комплексов с мостиковыми лигандами
Названия комплексов с мостиковыми лигандами Викторин. Диалог химии и медицины
Викторин. Диалог химии и медицины Урок изучения и первичного усвоения знаний с элементами исследования на тему: «Окислительно-восстановительные свойства соединен
Урок изучения и первичного усвоения знаний с элементами исследования на тему: «Окислительно-восстановительные свойства соединен Наноматериалы и нанотехнологии
Наноматериалы и нанотехнологии Растворы. Способы выражения концентрации растворенного вещества
Растворы. Способы выражения концентрации растворенного вещества Чистые вещества и смеси
Чистые вещества и смеси Строение вещества. Эксперименты
Строение вещества. Эксперименты Физико-химические основы получения лекарственных препаратов
Физико-химические основы получения лекарственных препаратов Спирты. Методы получения
Спирты. Методы получения Производственно-торговая компания ООО СОЖ Синтез-Набережные Челны
Производственно-торговая компания ООО СОЖ Синтез-Набережные Челны Строение атома
Строение атома Рівноваги у розчинах електролітів
Рівноваги у розчинах електролітів Менделеев Дмитрий Иванович
Менделеев Дмитрий Иванович Химическая картина мира
Химическая картина мира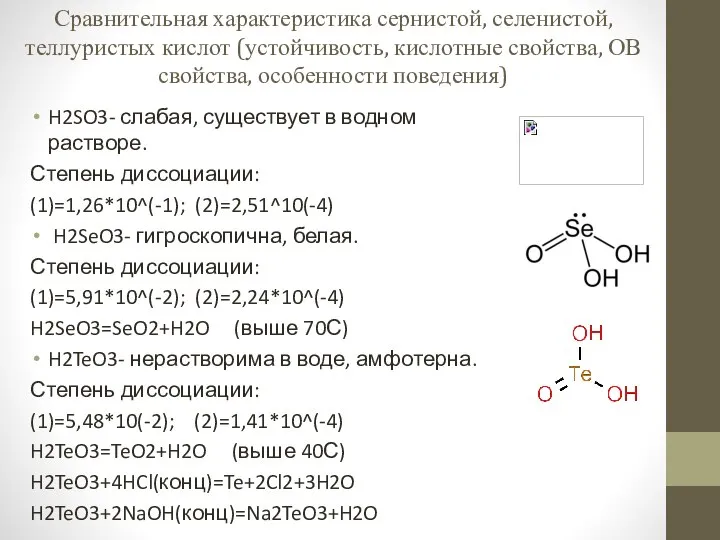 Сравнительная характеристика сернистой, селенистой, теллуристых кислот
Сравнительная характеристика сернистой, селенистой, теллуристых кислот Валентность. Определение валентности по формулам
Валентность. Определение валентности по формулам Биологическое окисление
Биологическое окисление Презентация на тему Минеральные удобрения
Презентация на тему Минеральные удобрения  Художественная обработка металла
Художественная обработка металла