Содержание
- 2. Равновесие жидкость-пар подчиняется законам Коновалова, связывающими общее давление насыщенного пара с составом жидкой и газовой фаз:
- 3. Растворимость веществ. Основываясь на зависимости химического потенциала от молярной доли и температуры, для идеальных растворов получено
- 5. Криоскопии. Эбулиоскопия. Осмотическое давление
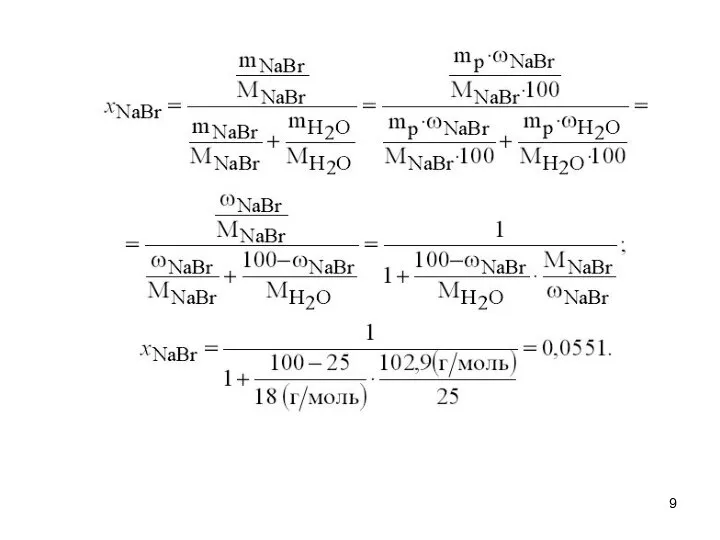
- 7. Примеры решения задач. Задача №1. Плотность 25%-го водного раствора NаВг равна 1.223 г/ см3. Выразить состав
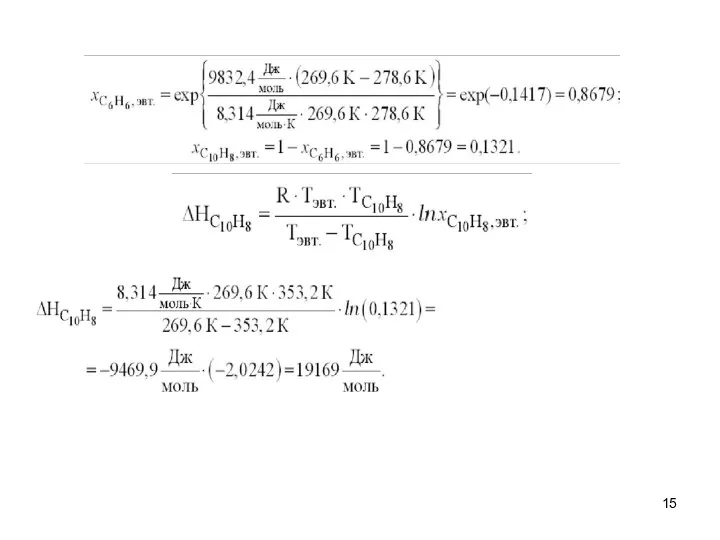
- 14. Графической интерпретацией этого выражения является кривая растворимости (кристаллизации) раствора на эвтектической диаграмме. Найдем координаты эвтектической точки,
- 18. Скачать презентацию













 Общая характеристика неметаллов подгруппы кислород
Общая характеристика неметаллов подгруппы кислород Характеристика азота как химического элемента и простого вещества
Характеристика азота как химического элемента и простого вещества Гидролиз солей
Гидролиз солей Понятие Эффективность. Принцип Ле-Шателье
Понятие Эффективность. Принцип Ле-Шателье Получение металлов
Получение металлов Коррозия металлов. Электрохимическая коррозия
Коррозия металлов. Электрохимическая коррозия Свойства воды
Свойства воды Металлы
Металлы Циклоалканы. Номенклатура и строение
Циклоалканы. Номенклатура и строение Нафта. Походження, переробка, використання
Нафта. Походження, переробка, використання Понятия и законы в химии. (Лекция 1)
Понятия и законы в химии. (Лекция 1) Электролитическая диссоциация
Электролитическая диссоциация Средства для мытья окон
Средства для мытья окон Строение и номенклатура карбонильных соединений
Строение и номенклатура карбонильных соединений Своя игра. Металлы и неметаллы
Своя игра. Металлы и неметаллы Презентация на тему Алкены. Строение. Изомерия. Химические свойства. Получение
Презентация на тему Алкены. Строение. Изомерия. Химические свойства. Получение  Проект Chemical 3D
Проект Chemical 3D Понятие о скорости химической реакции
Понятие о скорости химической реакции Оксиды
Оксиды Сокровища соляных дворцов
Сокровища соляных дворцов Сырье, продукты, параметры гидроочистки
Сырье, продукты, параметры гидроочистки Проверочный тест. Номенклатура алканов
Проверочный тест. Номенклатура алканов Электролиз
Электролиз Урок по теме Алюминий .Строение.Свойства. Учитель: Деревянко Н.Г.
Урок по теме Алюминий .Строение.Свойства. Учитель: Деревянко Н.Г. Альдегиды. Общая формула
Альдегиды. Общая формула Презентация на тему Стекло
Презентация на тему Стекло  Основания. Растворимые (гидроксиды щелочных и щелочноземельных металлов). Нерастворимые
Основания. Растворимые (гидроксиды щелочных и щелочноземельных металлов). Нерастворимые Своя игра. Химия и охрана почв
Своя игра. Химия и охрана почв