Содержание
- 2. МЕДИЦИНСКАЯ ХИМИЯ – объединяет закономерности всех разделов химии для изучения химической стороны физиологических процессов, лекарственной, гигиенической
- 3. Физическая химия изучает взаимосвязь химических и физических явлений. Химические реакции всегда связаны с разнообразными физическими процессами:
- 4. ТЕРМОДИНАМИКА изучает энергетику физических, физико-химических, химических процессов и отвечает на вопросы: возможен ли процесс и в
- 5. ОСНОВНЫЕ ПОНЯТИЯ И ЗАКОНЫ ТЕРМОДИНАМИКИ Предметом классической термодинамики является изучение законов взаимных превращений различных видов энергии,
- 6. В зависимости от характера взаимодействия с окружающей средой различают системы: ОТКРЫТЫЕ – обмениваются с окружающей средой
- 7. Термодинамическое РАВНОВЕСНОЕ состояние, которое характеризуется постоянством всех свойств во времени в любой точке системы и отсутствием
- 8. ИНТЕНСИВНЫЕ параметры или основные параметры состояния - параметры, которые поддаются непосредственному измерению, не зависят от числа
- 9. В зависимости от изменения параметров системы процессы разделяют на: изотермические Т=const, ∆T = 0 изохорические V=const
- 10. Термодинамический процесс вызывает энергетические изменения в системе, которые выражаются через изменение определенных величин: внутренней энергии, теплоты,
- 11. ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ. ТЕРМОХИМИЯ. Первый закон ТД – всеобщий закон природы, закон сохранения и превращения энергии.
- 12. 1. В изобарных условиях ( P = Const) Qp= ΔH Следствия из первого начала ТД 2.
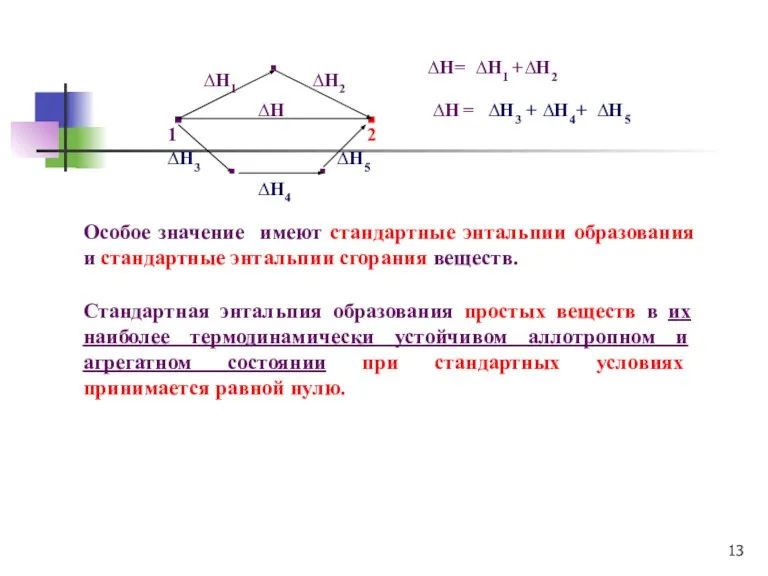
- 13. 1 ▪ ▪ ∆H 2 ▪ ∆H2 ∆H1 ▪ ▪ ∆H3 ∆H4 ∆H5 ∆H= ∆H3 +
- 14. Cледствия из закона Гесса. Стандартная энтальпия сгорания вещества равна энтальпии реакции сгорания 1 моль вещества при
- 15. 3. Энтальпия прямой реакции равна энтальпии обратной реакции, но с противоположным знаком
- 16. Калорийностью питательных веществ называется энергия, выделяемая при полном окислении 1 г питательных веществ. 1 калория =
- 18. Скачать презентацию














 Образование первичной структуры белка
Образование первичной структуры белка Железо
Железо Катаболизм пуриновых нуклеотидов
Катаболизм пуриновых нуклеотидов Кристаллическое строение металлов и сплавов. Аморфные и кристаллические тела
Кристаллическое строение металлов и сплавов. Аморфные и кристаллические тела Сплавы металлов (познавательная презентация)
Сплавы металлов (познавательная презентация) Предмет органической химии. Особенности органических веществ
Предмет органической химии. Особенности органических веществ Отжиг сталей (отжиг 2-го рода) Лекция 2
Отжиг сталей (отжиг 2-го рода) Лекция 2 Металлы II А подгруппы
Металлы II А подгруппы Презентация
Презентация Фосфор - светоносный
Фосфор - светоносный 1662922113131__olk9yp
1662922113131__olk9yp Соединения щелочных металлов
Соединения щелочных металлов Хлор. Химические свойства и применение. Лекция 5
Хлор. Химические свойства и применение. Лекция 5 Сложные неорганические вещества
Сложные неорганические вещества Презентация по Химии "Строение и физические свойства металлов"
Презентация по Химии "Строение и физические свойства металлов"  Основной закон радиоактивного распада и активность радионуклидов
Основной закон радиоактивного распада и активность радионуклидов Контроль качества лекарственных средств, производных аминокислот ароматического ряда. Лекция № 11
Контроль качества лекарственных средств, производных аминокислот ароматического ряда. Лекция № 11 Магматические породы
Магматические породы Строение металлов и их сплавов
Строение металлов и их сплавов Химическое равновесие и способы его смещения
Химическое равновесие и способы его смещения Материальный и тепловой балансы абсорбции
Материальный и тепловой балансы абсорбции Химия и сельское хозяйство
Химия и сельское хозяйство Характеристика 1-й аналитической группы анионов
Характеристика 1-й аналитической группы анионов Vielu īpašības
Vielu īpašības Обмен белков и аминокислот. Синтез заменимых аминокислот
Обмен белков и аминокислот. Синтез заменимых аминокислот Молярный объем газов. Закон Авогадро
Молярный объем газов. Закон Авогадро Сульфиты. Виды сульфидов
Сульфиты. Виды сульфидов Нафтены и арены
Нафтены и арены