Содержание
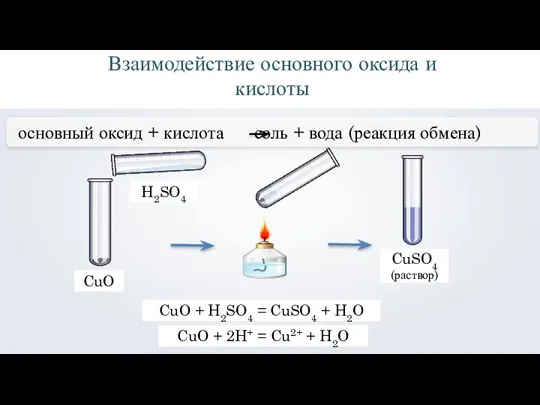
- 2. Взаимодействие основного оксида и кислоты основный оксид + кислота соль + вода (реакция обмена) CuO H2SO4
- 3. Взаимодействие основного оксида и кислотного оксида CuO + SO2 = CuSO3
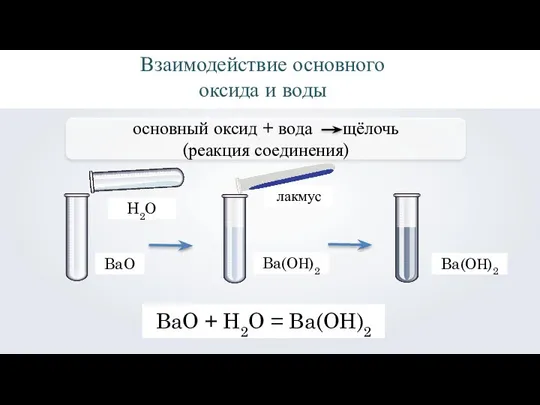
- 4. Взаимодействие основного оксида и воды BaO H2O Ba(OН)2 лакмус Ba(OН)2 BaO + H2O = Ba(OH)2
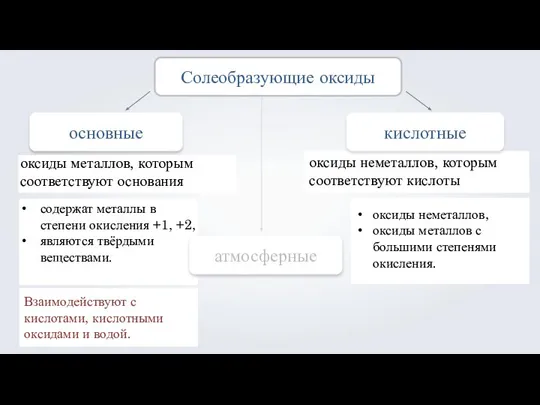
- 5. содержат металлы в степени окисления +1, +2, являются твёрдыми веществами. основные атмосферные оксиды металлов, которым соответствуют
- 6. Кислотные оксиды, состоящие из атомов неметаллов и кислорода SO2 оксид серы (IV) H2SO3 сернистая кислота —
- 7. Кислотные оксиды, состоящие из атомов металла и кислорода CrO3 оксид хрома (VI) H2CrO4 хромовая кислота —
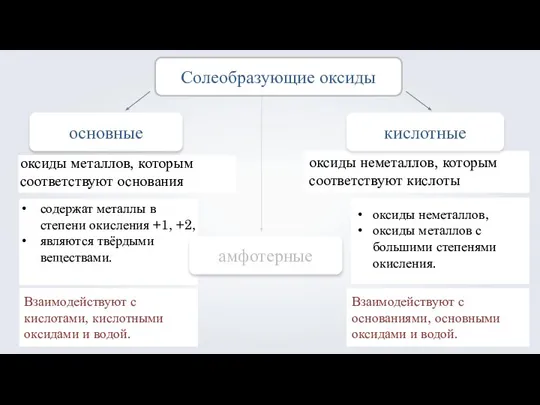
- 8. содержат металлы в степени окисления +1, +2, являются твёрдыми веществами. основные амфотерные оксиды металлов, которым соответствуют
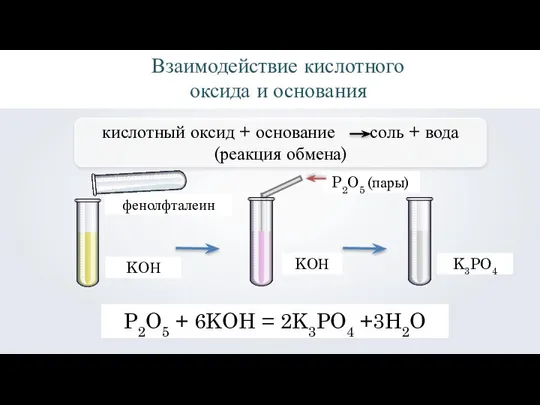
- 9. фенолфталеин Взаимодействие кислотного оксида и основания KOН KOН P2O5 (пары) K3PO4 P2O5 + 6KOH = 2K3PO4
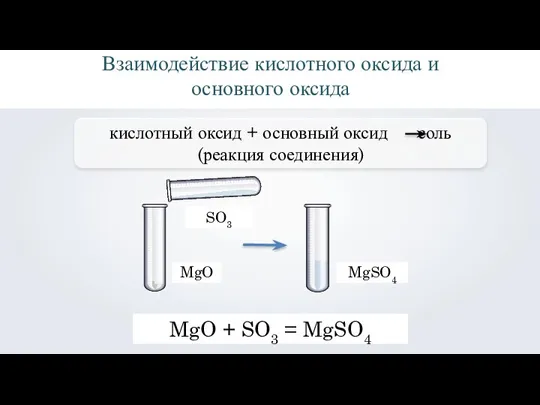
- 10. Взаимодействие кислотного оксида и основного оксида MgO SO3 MgO + SO3 = MgSO4 MgSO4
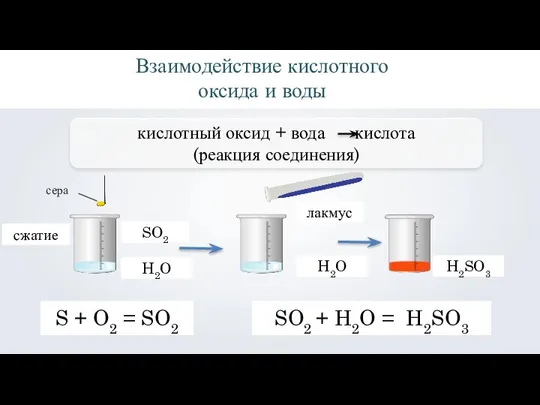
- 11. Взаимодействие кислотного оксида и воды SO2 H2O лакмус H2O H2SO3 S + O2 = SO2 SO2
- 13. Скачать презентацию



 Условия среды, вызывающие коррозию металла
Условия среды, вызывающие коррозию металла Комментарии к выполненным заданиям по темам Алканы и Алкены. 9 класс
Комментарии к выполненным заданиям по темам Алканы и Алкены. 9 класс ФБОУ- Раздольненская средняя общеобразовательная школа №19 Новосибирского района Новосибирской области
ФБОУ- Раздольненская средняя общеобразовательная школа №19 Новосибирского района Новосибирской области Характеристика химического элемента-неметалла на основании его положения в ПСХЭ Д.И.Менделеева. 9 класс
Характеристика химического элемента-неметалла на основании его положения в ПСХЭ Д.И.Менделеева. 9 класс Электролитическая диссоциация
Электролитическая диссоциация Классификация ХГ методов разделения
Классификация ХГ методов разделения Значение химии в медицине
Значение химии в медицине Рубидий (лат. Rubidium)
Рубидий (лат. Rubidium) Реакции соединения
Реакции соединения Кинетика химических реакций
Кинетика химических реакций Введение в органическую химию
Введение в органическую химию Пятая группа элементов
Пятая группа элементов Французский физик, химик, металловед 1850 - 1936
Французский физик, химик, металловед 1850 - 1936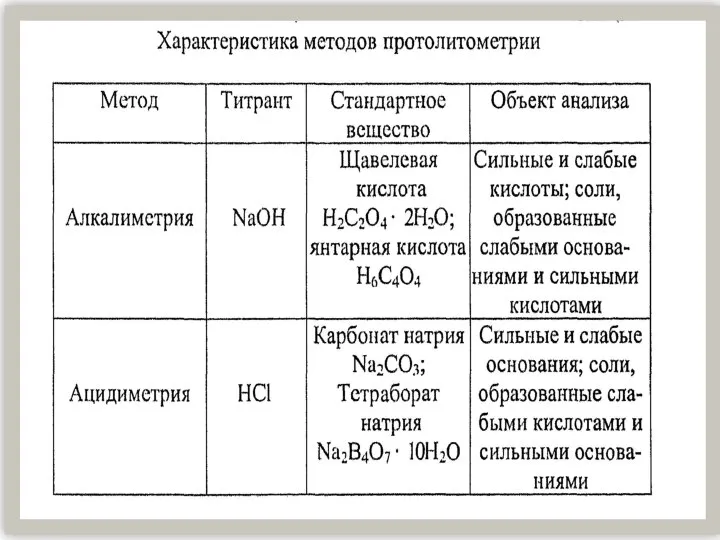 Характеристика методов протолитометрии
Характеристика методов протолитометрии Соединения серы
Соединения серы Движение молекул
Движение молекул Индиго-краситель
Индиго-краситель Селективность (реакторы)
Селективность (реакторы) Презентация на тему Алканолы
Презентация на тему Алканолы  Кинетика физико-химических процессов
Кинетика физико-химических процессов кремний и его соединения
кремний и его соединения Водород
Водород Закон сохранения массы
Закон сохранения массы Пиримидин (шестичленный гетероцикл с двумя атомами азота)
Пиримидин (шестичленный гетероцикл с двумя атомами азота) Типы загрязнений биосферы
Типы загрязнений биосферы Кислоты в свете теории электролитической диссоциации
Кислоты в свете теории электролитической диссоциации Поделочный камень родонит
Поделочный камень родонит Получение углекислого газа и изучение его свойств. Практическая работа
Получение углекислого газа и изучение его свойств. Практическая работа