Содержание
- 2. Только в «жестких» условиях реагирует с О2: N2 + O2 2NO – Q C Н2, только
- 3. Нитриды легко взаимодействуют с водой: Ca3N2 + 6H2O = 3Ca(OH)2 + 2NH3 И с кислотами: AlN
- 4. Получение: В лабораторных условиях: (NH4)2Cr2O7 = Cr2O3 + N2 + 4H2O NH4NO2 = N2 + 2H2O
- 5. Аммиак. NH3. В обычных условиях газ, с резким запахом. В жидком состоянии молекулы связан водородными связями.
- 7. Скачать презентацию




 Альдегиды, строение и свойства
Альдегиды, строение и свойства Кроссворд по теме Металлы
Кроссворд по теме Металлы Диаграмма состояния железо-цементит
Диаграмма состояния железо-цементит Отчёт по ПП 03.01. Лаборант химического анализа. Подготовка химической посуды, приборов и лабораторного оборудования
Отчёт по ПП 03.01. Лаборант химического анализа. Подготовка химической посуды, приборов и лабораторного оборудования Презентация на тему Свойства простых веществ
Презентация на тему Свойства простых веществ  Методы выделения и разделения радионуклидов
Методы выделения и разделения радионуклидов Презентация по Химии "Законы газового состояния вещества"
Презентация по Химии "Законы газового состояния вещества"  Производство серной кислоты
Производство серной кислоты Характеристика кислорода и серы
Характеристика кислорода и серы Растворы. Квалификации химических веществ:
Растворы. Квалификации химических веществ: Пуриновые основания
Пуриновые основания Стереоизомерия
Стереоизомерия Периодический закон Менделеева в действии
Периодический закон Менделеева в действии Презентация на тему Водород (8 класс)
Презентация на тему Водород (8 класс)  Щелочноземельные металлы
Щелочноземельные металлы Химическая связь
Химическая связь Углеводы. Общее понятие углеводов
Углеводы. Общее понятие углеводов Скорость химических реакций
Скорость химических реакций Строение сплавов, диаграммы состояний
Строение сплавов, диаграммы состояний Презентация на тему Классификация химических реакций
Презентация на тему Классификация химических реакций 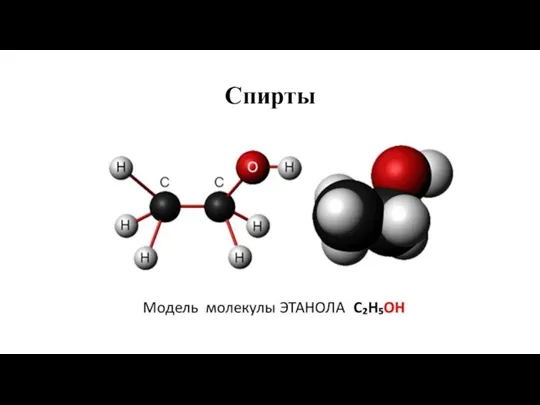 Спирты
Спирты Минеральные компоненты молока и молочных продуктов. Макроэлементы
Минеральные компоненты молока и молочных продуктов. Макроэлементы Алкены. Строение, номенклатура, изомерия, физические свойства
Алкены. Строение, номенклатура, изомерия, физические свойства Окислительно-восстновительные реакции
Окислительно-восстновительные реакции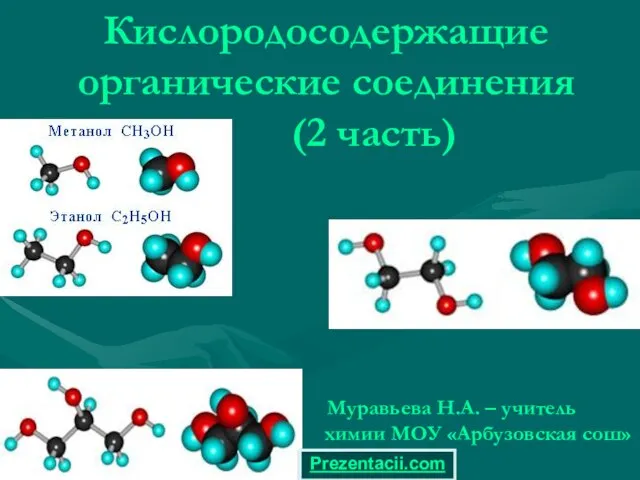 Презентация на тему Альдегиды и Кетоны
Презентация на тему Альдегиды и Кетоны  Кислотно-основное равновесие
Кислотно-основное равновесие Предельные углеводороды. Лекция 2
Предельные углеводороды. Лекция 2 Химические реакции
Химические реакции