Содержание
- 2. ПРАВИЛА НОМЕНКЛАТУРЫ МОСТИКОВЫХ СОЕДИНЕНИЙ Основой названия станет предельный углеводород, соответствующий полному числу атомов углерода, входящих в
- 3. Нумеруют полициклические соединения, начиная с первого узлового атома мостика, по самому длинному пути до второго узлового
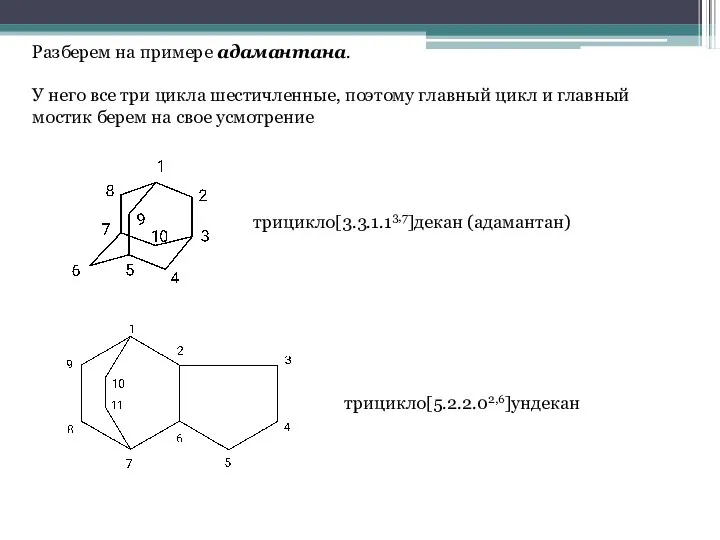
- 4. Разберем на примере адамантана. У него все три цикла шестичленные, поэтому главный цикл и главный мостик
- 5. Спироуглеводороды (спираны, спироцикланы) – циклические углеводороды, имеющие только один общий атом углерода (т.е. без мостика). Общий
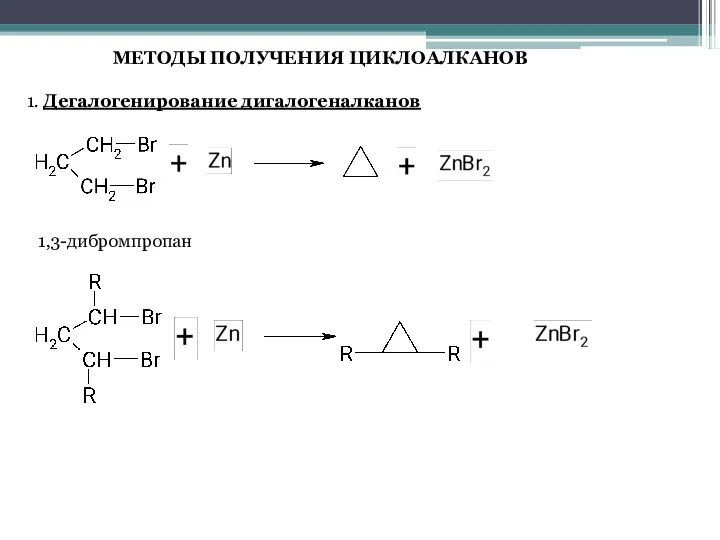
- 6. МЕТОДЫ ПОЛУЧЕНИЯ ЦИКЛОАЛКАНОВ 1. Дегалогенирование дигалогеналканов 1,3-дибромпропан
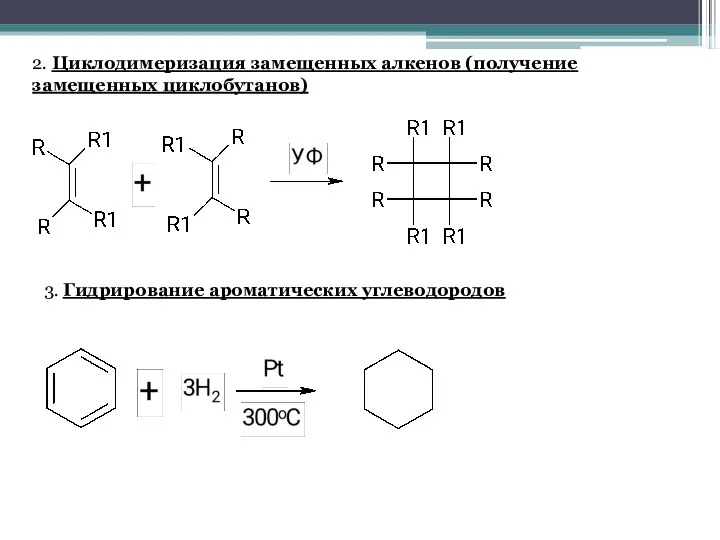
- 7. 2. Циклодимеризация замещенных алкенов (получение замещенных циклобутанов) 3. Гидрирование ароматических углеводородов
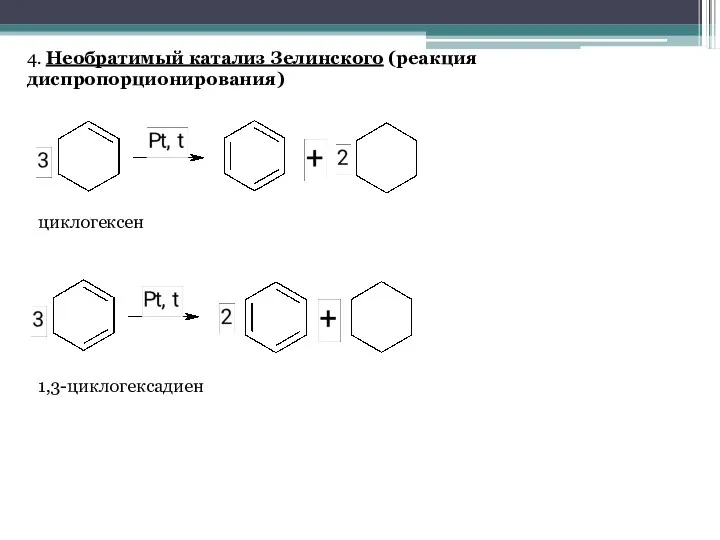
- 8. 4. Необратимый катализ Зелинского (реакция диспропорционирования) циклогексен 1,3-циклогексадиен
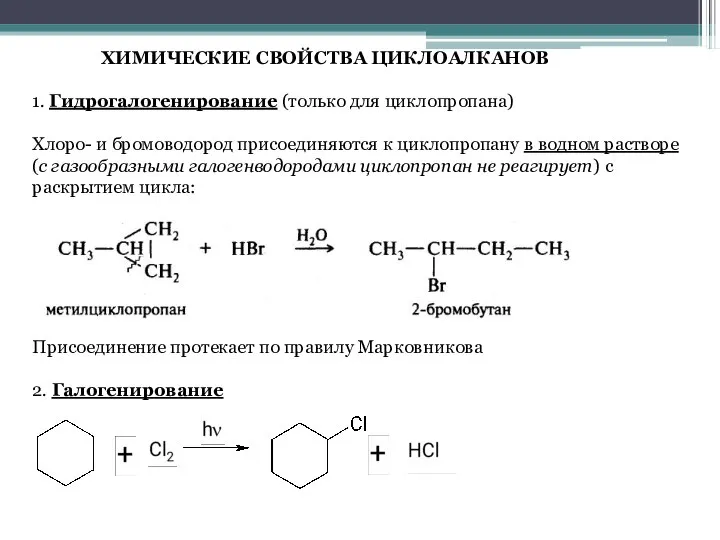
- 9. ХИМИЧЕСКИЕ СВОЙСТВА ЦИКЛОАЛКАНОВ 1. Гидрогалогенирование (только для циклопропана) Хлоро- и бромоводород присоединяются к циклопропану в водном
- 10. В малых циклоалканах такая реакция протекает только при комнатных температурах. При нагревании свыше 100° происходит раскрытие
- 11. 4. Окисление адипиновая кислота В качестве окислителя используется 50-70%-ная азотная кислота, при температуре 100-200°С и давлении
- 13. Скачать презентацию





 Сера. Немного истории
Сера. Немного истории тэд — без анимации(1)
тэд — без анимации(1) Распространение ПВО в приземном слое атмосферы
Распространение ПВО в приземном слое атмосферы Возможности пропедевтического курса химии
Возможности пропедевтического курса химии Амины
Амины Презентация на тему Оксиды. Основания. Кислоты
Презентация на тему Оксиды. Основания. Кислоты  Взаимодействие частиц конденсированной фазы, их срастание (коалесценция). Лекция 3
Взаимодействие частиц конденсированной фазы, их срастание (коалесценция). Лекция 3 Гидролиз солей
Гидролиз солей Неметаллы. Общая характеристика
Неметаллы. Общая характеристика Общие знания по курсу неорганической химии
Общие знания по курсу неорганической химии Предмет органической химии
Предмет органической химии Металлы тоже воевали… 8 класс
Металлы тоже воевали… 8 класс Переработка нефти
Переработка нефти Разбор заданий
Разбор заданий Составление химических формул методом нулевой суммы
Составление химических формул методом нулевой суммы Составление уравнений окислительно-восстановительных реакций
Составление уравнений окислительно-восстановительных реакций Алкадиены. Строение. Изомерия. Свойства
Алкадиены. Строение. Изомерия. Свойства Карбонильные соединения – альдегиды
Карбонильные соединения – альдегиды Закономерности процессов тепло- и газообмена на пожаре
Закономерности процессов тепло- и газообмена на пожаре Педагогические измерительные материалы ХИМИЯ Варганова Ирина Вячеславовна, и.о. зав. кафедрой естественно-математических дисцип
Педагогические измерительные материалы ХИМИЯ Варганова Ирина Вячеславовна, и.о. зав. кафедрой естественно-математических дисцип Характеристика переходного элемента на основании его положения в периодической системе Д.И. Менделеева
Характеристика переходного элемента на основании его положения в периодической системе Д.И. Менделеева Презентация на тему Угольная кислота и её соли (9 класс)
Презентация на тему Угольная кислота и её соли (9 класс)  Золото
Золото Смеси веществ
Смеси веществ Химический тренажер
Химический тренажер Вебинар. Задачи из домашек по 27-29 задачам
Вебинар. Задачи из домашек по 27-29 задачам Металлы
Металлы Окислительно-восстановительные реакции, 9 класс
Окислительно-восстановительные реакции, 9 класс