Содержание
- 2. Вода является растворителем для многих твердых, жидких и газообразных веществ. Со многими веществами она образует растворы.
- 3. Растворами называются однородные системы, состоящие из молекул растворителя и растворенного вещества, между которыми происходят физические и
- 4. Растворимость веществ в воде. Не все вещества одинаково хорошо растворяются в воде. Чтобы сравнить насколько одно
- 5. Растворимость-это отношение массы вещества, образующего насыщенный раствор при данной температуре, к объему растворителя. Единицы измерения растворимости-
- 6. Раствор, в котором данное вещество при данной температуре больше уже не растворяется, называется насыщенным, а раствор,
- 7. Если в 100г воды при комнатной температуре растворяется более 10г вещества, то оно называется хорошо растворимым
- 8. Если в 100г воды при комнатной температуре растворяется менее 1г вещества, то оно называется малорастворимым и
- 9. Если в 100г воды при комнатной температуре растворяется менее 0,01г вещества, то оно называется нерастворимым и
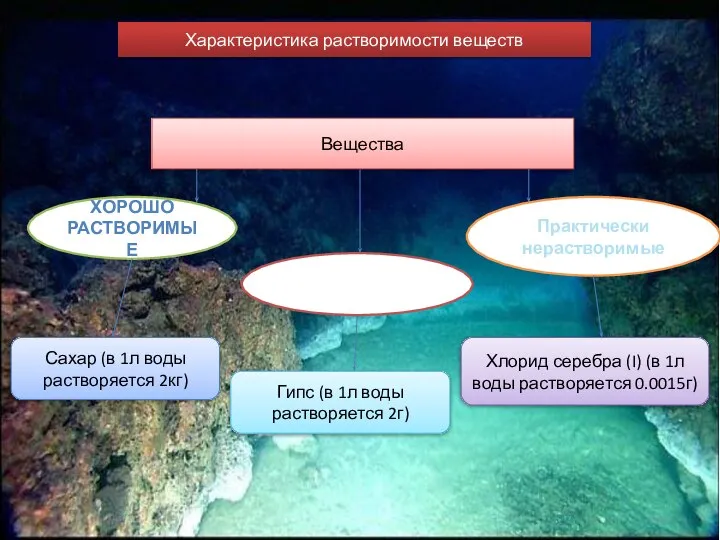
- 10. Вещества Характеристика растворимости веществ ХОРОШО РАСТВОРИМЫЕ Малорастворимые Практически нерастворимые Сахар (в 1л воды растворяется 2кг) Гипс
- 11. Растворимость большинства твердых веществ уменьшается с понижением температуры. Если горячий насыщенный раствор охладить, то некоторые твердые
- 12. Некоторые твердые вещества при понижении температуры не выделяются в виде кристаллов, а образуют перенасыщенные растворы.
- 13. Растворимость жидкостей и газов Жидкости и газы также могут растворяться в воде. Они, как и твердые
- 14. Многие газы, например водород, аргон, неон, очень плохо растворяются в воде, а хлороводород, аммиак, наоборот хорошо.
- 15. Вода- химически активное вещество. При растворении в воде газов, жидкостей и твердых веществ образуются однородные прозрачные
- 16. Вода- универсальный растворитель. Растворы- однородные системы, состоящие из системы молекул растворителя и растворного вещества
- 18. Скачать презентацию














 Исследование фазовых и структурных превращений в железе и его сплавах магнитным методом
Исследование фазовых и структурных превращений в железе и его сплавах магнитным методом Спирты. Классификация, изомерия
Спирты. Классификация, изомерия Нуклеирующие добавки
Нуклеирующие добавки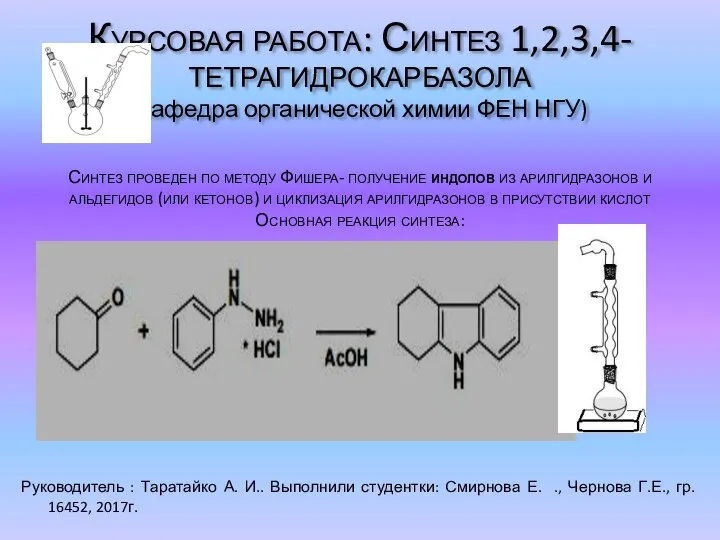 Синтез 1,2,3,4-тетрагидрокарбазола
Синтез 1,2,3,4-тетрагидрокарбазола Основные особенности процессов растворения твёрдых веществ
Основные особенности процессов растворения твёрдых веществ Реакции ионного обмена. Электролитическая диссоциация
Реакции ионного обмена. Электролитическая диссоциация Изменения, происходящие с веществами Урок химии 8 класс Учитель химии МОУ «СОШ №7» г. Балаково Саратовская обл.
Изменения, происходящие с веществами Урок химии 8 класс Учитель химии МОУ «СОШ №7» г. Балаково Саратовская обл. Презентация на тему Жидкий металл - ртуть
Презентация на тему Жидкий металл - ртуть 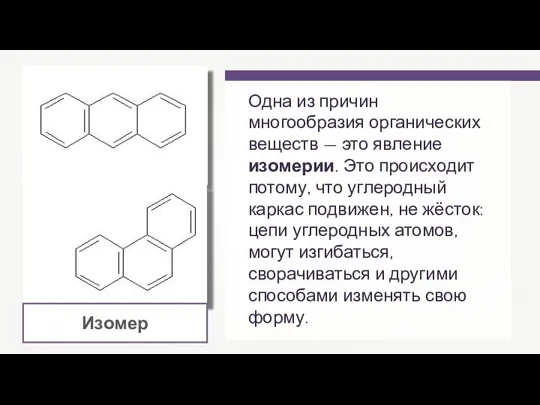 Номенклатура и изомерия алкенов
Номенклатура и изомерия алкенов Серная кислота. Свойства серной кислоты
Серная кислота. Свойства серной кислоты Химия и сельское хозяйство
Химия и сельское хозяйство prezentatsiya-po-fizike-7-klass-tri-agregatnyh-sostoyaniya-veshchestva
prezentatsiya-po-fizike-7-klass-tri-agregatnyh-sostoyaniya-veshchestva Презентация на тему Химические средства гигиены и косметика
Презентация на тему Химические средства гигиены и косметика  Общие вопросы материаловедения
Общие вопросы материаловедения Углеводы (Сахариды)
Углеводы (Сахариды)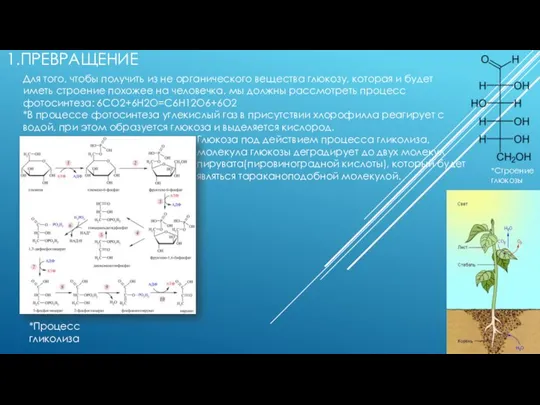 Превращение из не органического вещества в глюкозу
Превращение из не органического вещества в глюкозу Alkalické kovy
Alkalické kovy Многообразие органических веществ
Многообразие органических веществ Электрохимические процессы
Электрохимические процессы Силикатная промышленность
Силикатная промышленность Презентация на тему Органическая химия
Презентация на тему Органическая химия  Презентация на тему Научная химическая лаборатория Ломоносова
Презентация на тему Научная химическая лаборатория Ломоносова  Растворы электролитов
Растворы электролитов Вещества с атомной кристаллической решеткой
Вещества с атомной кристаллической решеткой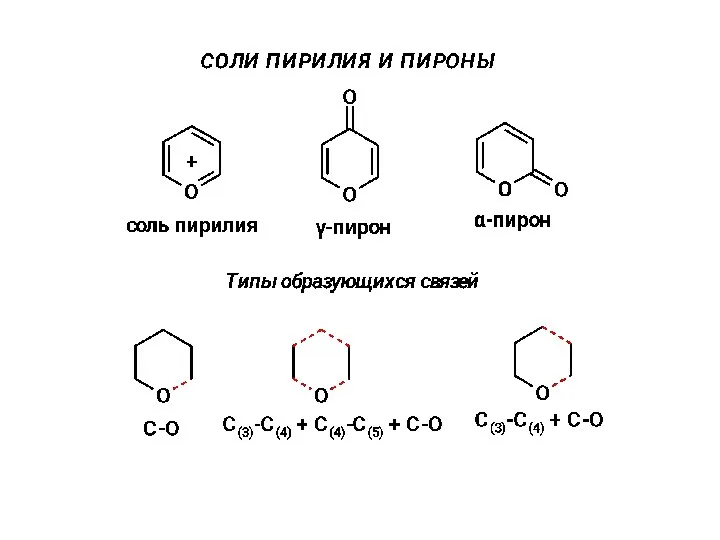 Соли пирилия и пироны
Соли пирилия и пироны Простые вещества - неметаллы
Простые вещества - неметаллы Соединения Ca и Mg, представителей элементов II группы главной подгруппы
Соединения Ca и Mg, представителей элементов II группы главной подгруппы Образовательные технологии, используемые на уроках химии для повышения мотивации обучения
Образовательные технологии, используемые на уроках химии для повышения мотивации обучения