Содержание
- 2. Цель проекта: Знакомство с водородом как элементом и веществом Рассматриваемые вопросы: История открытия элемента Строение атома
- 3. Рабочие группы: 1 группа – «Теоретики» 2 группа – «Исследователи» 3 группа – «Практики»
- 4. История открытия Впервые этот газ в чистом виде выделил 240 лет назад английский химик Генри Кавендиш.
- 5. Другой великий химик, француз Антуан-Лоран Лавуазье, уже в 1787 году доказал, что полученное Кавендишем вещество —
- 6. Водород в природе: Водород широко распространен в природе — содержится в воде, во всех органических соединениях,
- 7. Водород самый распространенный элемент во вселенной
- 8. Общая характеристика: Порядковый номер 1 1 малый период I группа главная подгруппа Ar=1 Электронная конфигурация 1S1
- 9. Молекула водорода Молекула водорода состоит из двух атомов - H2 Ковалентная неполярная связь Н:Н
- 10. Получение водорода в лаборатории Zn + 2HCl → ZnCl2 + H2↑ 2H2 + O2 = 2H2O
- 11. Физические свойства водорода Бесцветный газ Без запаха Почти нерастворим в воде В 14,5 раз легче воздуха
- 12. Промышленные способы получения водорода Водород получают конверсией водяных паров с углем или метаном H2O + C
- 13. Восстановительные свойства водорода Горит в кислороде 2H2 + O2 = 2H2O Реагирует с другими неметаллами N2
- 14. Взаимодействие водорода с оксидом меди (II)
- 15. Окислительные свойства водорода Реагируют со щелочными и щелочноземельными металлами с образованием гидридов 2Na + H2 =
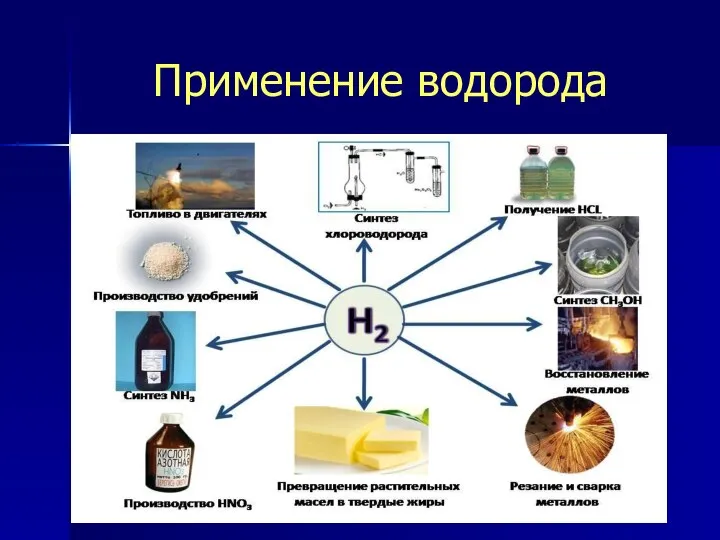
- 16. Применение водорода
- 17. Применение водорода Применение Свойства водорода Горит с выделением большого количества теплоты Реагирует с неметаллами Реагирует с
- 18. Применение Наработав в достаточном количестве этот легкий газ, люди сначала приспособили его для воздушных полетов. В
- 19. Водородная энергетика: миф или реальность? В недалёком будущем основным источником получения энергии станет реакция горения водорода,
- 20. Контрольные вопросы: Какой элемент характеризуется наибольшей распространенностью во Вселенной? Кто впервые выделил водород в чистом виде?
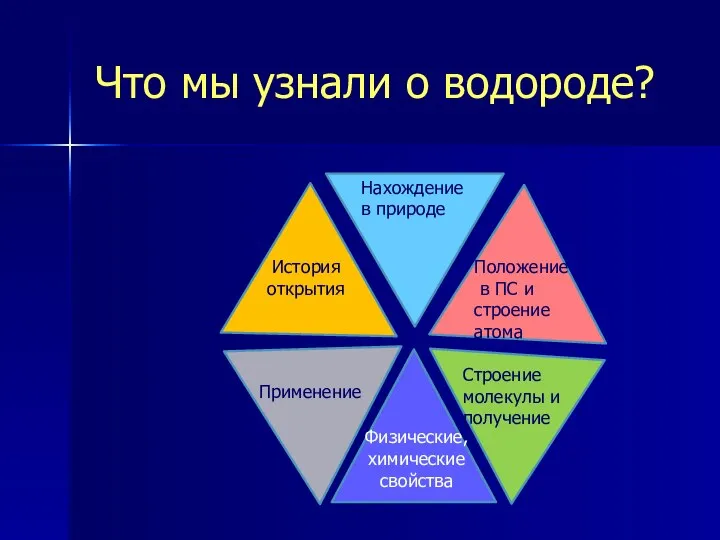
- 21. Что мы узнали о водороде? Положение в ПС и строение атома История открытия Нахождение в природе
- 23. Скачать презентацию


















 Презентация на тему Кристаллы
Презентация на тему Кристаллы  Классификация химических реакций по различным основаниям
Классификация химических реакций по различным основаниям Сера и ее соединения
Сера и ее соединения Презентация на тему Фолиевая кислота
Презентация на тему Фолиевая кислота  Химические свойства
Химические свойства Свойства кислорода. Оксиды
Свойства кислорода. Оксиды Термореактивные пластмассы (реактопласты)
Термореактивные пластмассы (реактопласты) Диссоциация. Уравнения диссоциации
Диссоциация. Уравнения диссоциации Бирюза. Характеристики минерала
Бирюза. Характеристики минерала Применение эфиров в производстве автомобильных бензинов
Применение эфиров в производстве автомобильных бензинов Презентация по Химии "Алканолы"
Презентация по Химии "Алканолы"  ОВР - метод полуреакции
ОВР - метод полуреакции 20170625_otkrytyy_integrirovannyy_urok_himiya-geografiya
20170625_otkrytyy_integrirovannyy_urok_himiya-geografiya 175 – летию со дня рождения Дмитрия Ивановича Менделеева посвящается… АВТОР ПРЕЗЕНТАЦИИ: учитель химии МОУ СОШ №2 города Ртищево Саратовской области ПОПКОВА Е.Г.
175 – летию со дня рождения Дмитрия Ивановича Менделеева посвящается… АВТОР ПРЕЗЕНТАЦИИ: учитель химии МОУ СОШ №2 города Ртищево Саратовской области ПОПКОВА Е.Г. Изомерия
Изомерия Сера и его соединения
Сера и его соединения Алкены-2 (электрофильные реакции)
Алкены-2 (электрофильные реакции) Застосування рідких кристалів
Застосування рідких кристалів Электролиз
Электролиз Астат. Свойства астата
Астат. Свойства астата Железо как химический элемент
Железо как химический элемент Золото (Au)
Золото (Au) Распределение электронов в атоме по энергетическим уровням
Распределение электронов в атоме по энергетическим уровням Трёхкомпонентные системы. Закон распределения. Экстракция. Свойства разбавленных растворов неэлектролитов
Трёхкомпонентные системы. Закон распределения. Экстракция. Свойства разбавленных растворов неэлектролитов Металлы. Своя игра
Металлы. Своя игра Научно-познавательное шоу Юный химик
Научно-познавательное шоу Юный химик Роль М.В. Ломоносова и Дж. Дальтона в создании атомно-молекулярного учения
Роль М.В. Ломоносова и Дж. Дальтона в создании атомно-молекулярного учения Bioenergetyka syntezy glutaminy
Bioenergetyka syntezy glutaminy