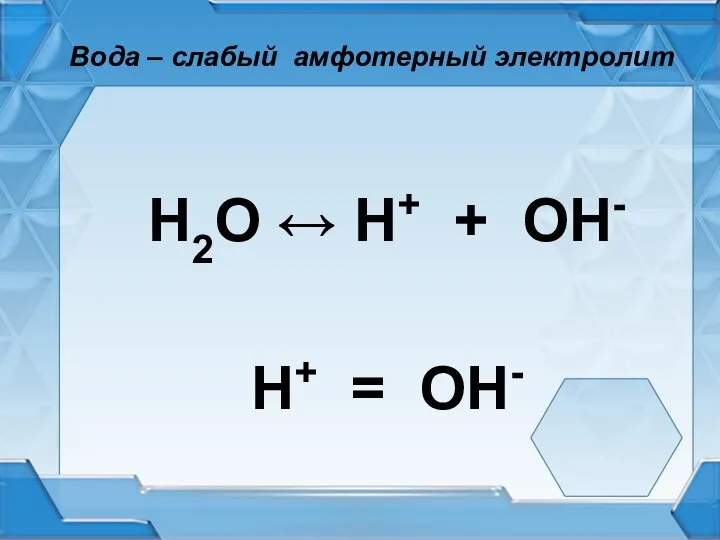
Слайд 4Вода – слабый амфотерный электролит
Н2О ↔ Н+ + ОН-
Н+ = ОН-
Слайд 5Водородный показатель (рН) – количественная характеристика кислотности среды

Слайд 6 Это понятие было введено в 1909 году датским химиком Сёренсеном. Показатель

называется pH, по первым буквам латинских слов potentia hydrogeni — сила водорода, или pondus hydrogenii — вес водорода.
Слайд 7
Зависимость среды раствора от концентрации ионов Н+ и ОН-

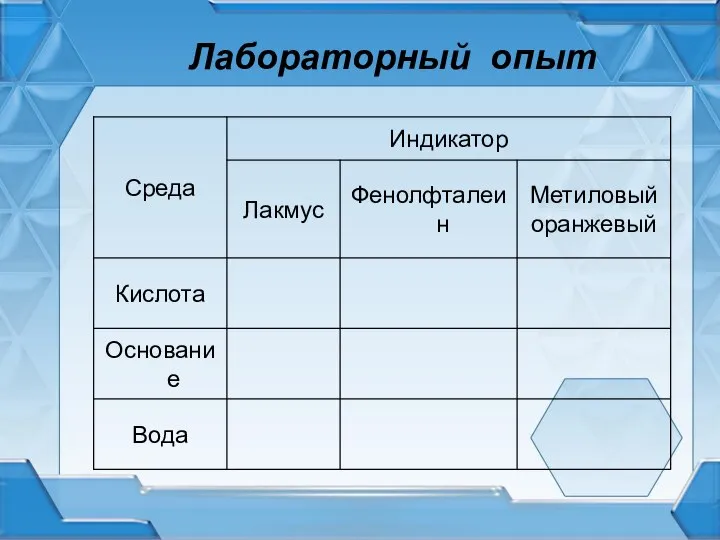
Слайд 8Индикаторы
органические соединения, изменяющие свою окраску при изменении среды растворов,т.е рН

Слайд 9Универсальный индикатор
Это смесь кислотно-основных индикаторов, позволяющая определить значение рН от 1 до

10.
Слайд 11Окраска индикаторов в различных средах

Слайд 12Лабораторная работа: «Определение рН в растворах СМС»











 Очистка белков (Разделение белков из гетерогенной белковой смеси)
Очистка белков (Разделение белков из гетерогенной белковой смеси) Современные сплавы на основе циркония
Современные сплавы на основе циркония Химические методы анализа. Гравиметрический метод анализа
Химические методы анализа. Гравиметрический метод анализа Полиуретаны. Структура и строение
Полиуретаны. Структура и строение Предельные углеводороды насыщенные, парафины, алканы
Предельные углеводороды насыщенные, парафины, алканы Сфера влияния химии
Сфера влияния химии Активность каталазы
Активность каталазы Основы переработки нефти и нефтепродуктов
Основы переработки нефти и нефтепродуктов Ковалентная полярная химическая связь
Ковалентная полярная химическая связь Первые попытки классификации химических элементов
Первые попытки классификации химических элементов Фенолы
Фенолы Коррозия металлов
Коррозия металлов Химические свойства щелочей (тема 6)
Химические свойства щелочей (тема 6) Лекции_ ОБМЕН ЛИПИДОВ
Лекции_ ОБМЕН ЛИПИДОВ Кислоты. Классификация кислот (8 класс)
Кислоты. Классификация кислот (8 класс) Основные классы неорганических соединений
Основные классы неорганических соединений Спирты и фенолы
Спирты и фенолы Презентация на тему по химии витамины
Презентация на тему по химии витамины  Химический состав клетки
Химический состав клетки Кинетика химических и биохимических процессов. Часть 1
Кинетика химических и биохимических процессов. Часть 1 Альдегиды. Строение молекул
Альдегиды. Строение молекул Молекулярно-кинетическая теория. Макро- и микропараметры
Молекулярно-кинетическая теория. Макро- и микропараметры Кислоты, их классификация и свойства
Кислоты, их классификация и свойства Оксиды. Классификация и химические свойства
Оксиды. Классификация и химические свойства Нуклеирующие добавки
Нуклеирующие добавки Составление уравнений окислительно-восстановительных реакций
Составление уравнений окислительно-восстановительных реакций Свойства нефти
Свойства нефти Химические реакции (2)
Химические реакции (2)