Слайд 2Ярослав Гейровский
Чешский химик, иностранный член АН СССР. Создал полярографию, сконструировал первый полярограф.

Лауреат Нобелевской премии по химии.
Родился: 20 декабря 1890 г.,
Умер: 27 марта 1967 г. (76 лет)
Слайд 4В электрохимическую ячейку обязательно добавляется индиферентный (фоновый) электролит, тем самым стремятся свести

все виды массопереноса к диффузии.
Iост. = Iф + Iконд.
Поляризация – изменение потенциала электрода под действием электрического тока.
ΔЕ = Е – ЕРАВ.
ΔЕ – поляризация электрода
Е – потенциал электрода под током
ЕРАВ. – потенциал электрода в отсутствии тока
Превращение вещества на электроде, происходящее под действием электрического тока – электрохимическая реакция включает в себя несколько зависимых стадий:
Подвод разряжающихся ионов из глубины раствора в приэлектродный слой
Диссоциация сложных ионов (например, комплексных) и дегидротация ионов
Электрохимическая реакция (разряд ионов)
Отвод продуктов реакции вглубь амальгамы
Слайд 6Природа предельного тока
В зависимости от лимитирующей стадии процесса предельный ток может быть:
диффузионный;
кинетический;
каталитический;
адсорбционный.
Признаки

диффузионного тока
Температурная зависимость (ΔId/ Δt).102 = 1.2-2.0 %/0C
Зависимость от высоты столба ртути – прямолинейная зависимость
Линейная зависимость предельного тока от концентрации в интервале 10-2-10-5 М
Признаки кинетического тока
Температурная зависимость (ΔIкин./ Δt).102 = 10-20 %/0C
Высота столба ртути не влияет на скорость химической реакции
Линейная зависимость предельного тока от концентрации в интервале 10-2-10-4 М
Признаки каталитического тока
Еще более высокий температурный коэффициент
Высота столба ртути не влияет на скорость химической реакции
Линейная зависимость предельного тока от концентрации в интервале 10-7-10-8 М
Слайд 7Уравнение обратимой катодной волны. Уравнение Ильковича - Гейровского
Если заранее известно, что

процесс обратимый, то можно найти число электронов, участвующих в электродной реакции, и наоборот.
Слайд 9Амперометрическое титрование
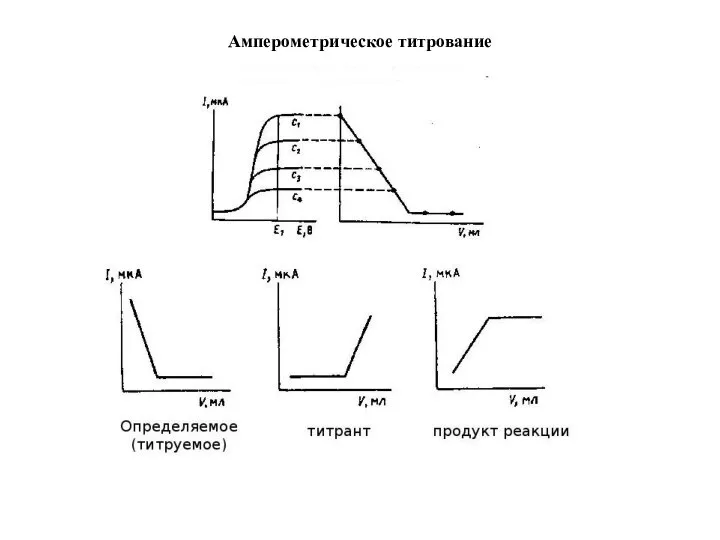
Слайд 10Индикаторными электродами для амперометрического титрования чаще всего служат вращающийся платиновый или графитовый

электроды (титрование по току окисления). Большое число органических реагентов, окисляющихся при потенциалах поляризации этих электродов и пригодных в качестве титрантов, позволяет найти условия для селективного определения многих элементов.
Селективность определения можно повысить, подобрав условия для протекания химической реакции в процессе титрования (регулирование рН, введение маскирующих агентов и т.д.)
Ртутный капающий электрод применяют гораздо реже (титрование по току восстановления).
Селективность таких определений не очень высока. Кроме того, в этом случае необходимо удалять растворенный кислород и тратить время на успокоение раствора после перемешивания при прибавлении очередной порции титранта.
Достоинством метода амперометрического титрования является прежде всего экспрессность и простота. Для построения кривой титрования по измерениям тока после прибавления нескольких порций титранта до и после к.т.т. Требуется гораздо меньше времени, чем на регистрацию вольтамперограмм и построение градуировочного графика в методе прямой вольтамперометрии. Кроме того, нет необходимости удалять растворенный кислород. Не нужна дорогая аппаратура.








 Производство полимеров в РК
Производство полимеров в РК Виды химической связи
Виды химической связи Алканы: состав, строение, изомерия, номенклатура, получение
Алканы: состав, строение, изомерия, номенклатура, получение Окислительно-восстановительные реакции. Типы химических реакций
Окислительно-восстановительные реакции. Типы химических реакций Диссоциация кислот, щелочей солей
Диссоциация кислот, щелочей солей L4_Aminoacids, peptides, proteins (2)
L4_Aminoacids, peptides, proteins (2) Періодична система хімічних елементів
Періодична система хімічних елементів Презентация на тему Эфиры и жиры
Презентация на тему Эфиры и жиры  Презентация на тему Альдегиды и их свойства
Презентация на тему Альдегиды и их свойства  Химическое равновесие и способы его смещения
Химическое равновесие и способы его смещения Теория электронных смещений в органических молекулах
Теория электронных смещений в органических молекулах Коррозия металлов
Коррозия металлов Выращивание кристаллов соли (домашний эксперимент)
Выращивание кристаллов соли (домашний эксперимент) Графен. Нобелевская премия 2016
Графен. Нобелевская премия 2016 Первоначальные химические понятия
Первоначальные химические понятия Презентация на тему Переработка нефти
Презентация на тему Переработка нефти  Методы активации карбоксильной группы
Методы активации карбоксильной группы Золь. Свойства золи
Золь. Свойства золи Электролиз. Электролитическая диссоциация
Электролиз. Электролитическая диссоциация Типы химических реакций
Типы химических реакций Карбид кальция. Назначение
Карбид кальция. Назначение Кислоты. Классификация кислот (8 класс)
Кислоты. Классификация кислот (8 класс) Рука руку моет. Механизм двух реакций
Рука руку моет. Механизм двух реакций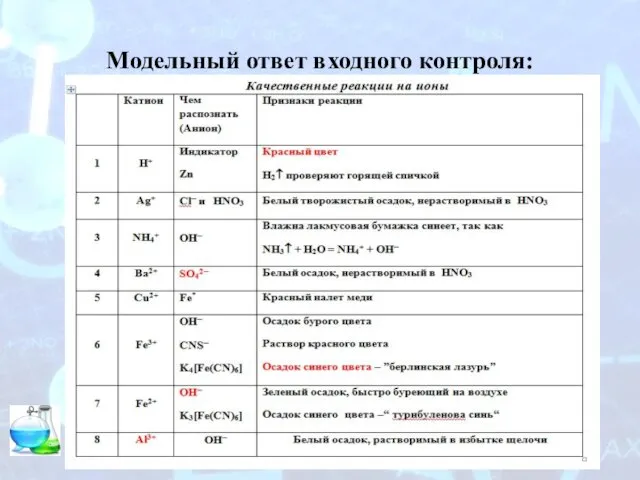 Модельный ответ входного контроля
Модельный ответ входного контроля DOC-20221011-WA0003
DOC-20221011-WA0003 Способы получения металлов. Сплавы металлов
Способы получения металлов. Сплавы металлов Классификация химических реакций
Классификация химических реакций Неметаллы. Агрегатные состояния неметаллов
Неметаллы. Агрегатные состояния неметаллов