Содержание
- 2. Основные требования, предъявляемые к экспресс–анализу: расход минимальных количеств лекарственных форм, простота и быстрота выполнения, достаточная точность
- 3. Для выполнения качественного экспресс–анализа используют цветные или осадочные химические реакции на соответствующие катионы, анионы неорганических или
- 4. Количественный экспресс-анализ может быть выполнен титриметрическими или физико-химическими методами.
- 5. Из титрометрических методов для количественного экспресс-анализа хлоридов, бромидов, йодидов используют аргентометрию или меркуриметрию. Соли цинка, магния,
- 6. Из физико-химических методов, для количественного экспресс-анализа лекарственных форм применяют рефрактометрию.
- 7. 2 . РАСЧЕТЫ. ПРЕДВАРИТЕЛЬНЫЙ РАСЧЕТ НАВЕСКИ И КОЛИЧЕСТВА ТИТРОВАННОГО РАСТВОРА. РАСЧЕТ СОДЕРЖАНИЯ ДЕЙСТВУЮЩЕГО ВЕЩЕСТВА.
- 8. Предварительный расчет массы (объема) лекарственной формы α с концентрацией препарата ⊂ (по прописи ), на титрование
- 9. Объем титранта V, который должен быть затрачен на титрование массы или объема а лекарственной формы с
- 10. РАСЧЕТ СОДЕРЖАНИЯ ДЕЙСТВУЮЩЕГО ВЕЩЕСТВА.
- 11. При выполнении анализа титриметрическим методами содержание лекарственного вещества Х вычисляют в процентах по формуле:
- 12. Где V – объем титранта, израсходованный на титрование (мл); К – коэффициент поправки титрованного раствора; Т-
- 13. Где V1 и V2 – объемы титрантов (мл), К1 и К2 – их коэффициенты поправок. Если
- 14. А – объем разведения; А1 – аликвотная часть раствора, взятая на анализ после разведения. б) при
- 15. расчет количественного содержания можно провести по среднему ориентировочному титру Т ср. Эта масса смеси определяемых веществ
- 16. где Т 1 – титр первого компонента; а1 – прописанная масса первого компонента; Т2 – титр
- 17. Используют также расчеты по условному титру (Т усл. ).
- 18. Так, например, кофеин- бензоат натрия анализируют в лекарственных формах по бензоату натрия. Условный титр кофеин -
- 19. Содержание натрия бензоата в кофеин-бензоате натрия в соответствии с требованиями ФС колеблется от 58 до 62%.
- 20. Для оценки качества лекарственных средств, изготовленных в аптеках, применяются два термина: "Удовлетворяет" ("Годная продукция") или "Не
- 21. Неудовлетворительность изготовленных лекарственных средств устанавливается по следующим показателям их качества: 1.1. Несоответствие по описанию (внешний вид,
- 22. 1.6. Несоответствие прописи по подлинности: 1.6.1. Ошибочная замена одного лекарственного вещества другим, отсутствие прописанного или наличие
- 23. 1.7. Отклонения от прописи по массе или объему; 1.7.1. Отклонения по общей массе (объему); 1.7.2. Отклонения
- 24. 1.8. Несоответствие по величине рН; 1.9. Несоответствие по величине плотности; 1.10. Несоответствие по стерильности; 1.11. Несоответствие
- 25. Изменения в составе лекарственных форм (если необходимо) должны производиться только с согласия врача, за исключением случаев,
- 26. Изменения в количестве отпущенного лекарственного средства или отпуск таблеток вместо порошков должны также отмечаться на требовании,
- 28. Скачать презентацию

























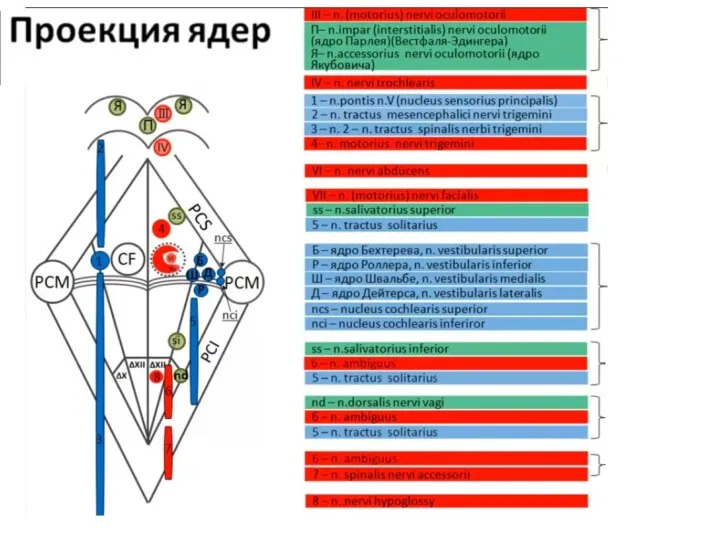 Проекция ядер черепных нервов
Проекция ядер черепных нервов Боль в спине. Классификация боли в спине по течению
Боль в спине. Классификация боли в спине по течению Нарушение ритма сердца
Нарушение ритма сердца Устройство работы скорой помощи в г. Энгельс
Устройство работы скорой помощи в г. Энгельс Ревматикалық аурулардың маскасы
Ревматикалық аурулардың маскасы Пути оттока внутриглазной жидкости из глазного яблока
Пути оттока внутриглазной жидкости из глазного яблока Разбор клинического случая. Кататравма
Разбор клинического случая. Кататравма Қартаюдың патофизиологиялық аспектілері
Қартаюдың патофизиологиялық аспектілері Ботаниканың фармациядағы маңызы
Ботаниканың фармациядағы маңызы Псевдофурункулез
Псевдофурункулез Бронхиальная астма
Бронхиальная астма Иммунитет
Иммунитет Зарядка для глаз - Гарри Поттер
Зарядка для глаз - Гарри Поттер Диагностический подход к пациентам с солидными новообразованиями
Диагностический подход к пациентам с солидными новообразованиями Мазок на наличие бациллы Леффлера
Мазок на наличие бациллы Леффлера Су бұрқақтар мен суару су құбырының сумен жабдықтау жүйелерін жобалау
Су бұрқақтар мен суару су құбырының сумен жабдықтау жүйелерін жобалау Идиопатический легочный фиброз
Идиопатический легочный фиброз Заболевания сосудистого тракта
Заболевания сосудистого тракта Проблемы здоровья и долголетия. Маникюр
Проблемы здоровья и долголетия. Маникюр Diagnostické a léčebné postupy u poranění břicha
Diagnostické a léčebné postupy u poranění břicha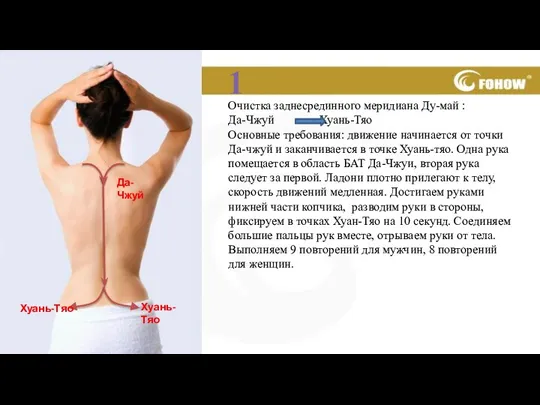 Очистка заднесрединного меридиана Ду-май
Очистка заднесрединного меридиана Ду-май Заболевания системы пищеварения. Энтероколит
Заболевания системы пищеварения. Энтероколит ABG case studies & interpretation
ABG case studies & interpretation Сестринский уход при заболеваниях органов кроветворения у детей
Сестринский уход при заболеваниях органов кроветворения у детей Профилактика и лечение вирусной инфекции человека
Профилактика и лечение вирусной инфекции человека Знакомство с проектами. Виды терапии
Знакомство с проектами. Виды терапии Синдром Вольфа Паркинсона Уайта
Синдром Вольфа Паркинсона Уайта 4 февраля – всемирный день борьбы против рака
4 февраля – всемирный день борьбы против рака