Слайд 2ХЕЛЬСИНКСКАЯ ДЕКЛАРАЦИЯ
ВСЕМИРНОЙ МЕДИЦИНСКОЙ АССОЦИАЦИИ
Этические принципы проведения медицинских исследований с участием человека

в качестве субъекта
Бразилия 2013 г.
Слайд 3Преамбула
1. Всемирная Медицинская Ассоциация (ВМА) разработала Хельсинкскую Декларацию в качестве свода этических

принципов проведения медицинских исследований с участием человека в качестве субъекта, в том числе исследований биологических материалов или данных, допускающих идентификацию лица, от которого они были получены.
Текст Декларации предназначен для использования в качестве целостного документа, и каждое его отдельное положение должно применяться с учетом всех других применимых положений.
2. В соответствии с полномочиями ВМА, Декларация адресована, прежде всего, врачам. ВМА призывает других лиц, вовлеченных в медицинские исследования с участием человека в качестве субъекта, следовать этим принципам.
Слайд 4HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
Основные принципы
3. Женевская декларация ВМА определяет долг врача

следующими словами: "Здоровье моего пациента будет моей главной заботой", а международный Кодекс медицинской этики гласит: "Врач при оказании медицинской помощи должен действовать в интересах пациента".
4. Долг врача – поддерживать и охранять здоровье, благополучие и права пациентов, в том числе тех, которые участвуют в медицинском исследовании. Знания и совесть врача должны быть направлены на служение этому долгу.
5. Прогресс медицины основан на научных исследованиях, которые, в конечном счете, должны включать исследования с участием людей в качестве субъектов.
Слайд 5HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
6. Основная цель медицинских исследований с участием человека

в качестве субъекта состоит в том, чтобы понять причины, механизмы развития и последствия заболеваний и совершенствовать профилактические, диагностические и терапевтические вмешательства (методы, процедуры и виды терапии). Даже лучшие из проверенных вмешательств должны постоянно посредством исследований подвергаться оценке на предмет их безопасности, эффективности, действенности, доступности и качества.
7. Медицинские исследования должны проводиться с соблюдением этических стандартов, гарантирующих уважение ко всем субъектам исследований и защиту их здоровья и прав.
8. В то время как основная цель медицинских исследований – получение новых знаний, эта цель никогда не должна превалировать над правами и интересами отдельных субъектов исследования.
Слайд 6HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
9. Долгом врача, вовлеченного в медицинское исследование, является

защита жизни, здоровья, достоинства, неприкосновенности, права на самоопределение, частную жизнь и конфиденциальность персональных данных субъектов исследования. Ответственность за защиту субъектов исследования всегда несет врач или иной медицинский работник, и ни в коем случае такая ответственность не может быть возложена на субъекта исследования, даже если он дал свое согласие.
Слайд 7HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
10. Врачи должны учитывать как национальные, так и

международные этические и правовые нормы и стандарты проведения исследований с участием человека в качестве субъекта. Никакие национальные или международные этические или правовые требования не должны умалять или отменять меры по защите субъектов исследования, установленные настоящей Декларацией.
11. Медицинские исследования должны проводиться таким образом, чтобы минимизировать возможный вред окружающей среде.
Слайд 8HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
12. Медицинские исследования с участием человека в качестве

субъекта должны проводиться только лицами, имеющими соответствующую этическую и научную подготовку, образование и квалификацию. Исследование с участием пациентов или здоровых добровольцев требует контроля со стороны компетентного и имеющего соответствующую квалификацию врача или иного медицинского работника.
13. Группам, в недостаточной мере привлекаемым к участию в медицинских исследованиях, необходимо обеспечить возможность участия в них.
Слайд 9HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
14. Врачи, сочетающие медицинские исследования с оказанием медицинской

помощи, должны привлекать к участию в них своих пациентов только в той степени, в какой это оправдано с точки зрения потенциальной профилактической, диагностической или терапевтической ценности, и если врач имеет достаточные основания полагать, что участие в исследовании не скажется неблагоприятным образом на здоровье пациентов, являющихся субъектами исследования.
15. Субъектам, пострадавшим в результате участия в исследовании, должны быть гарантированы соответствующие компенсация и лечение.
Слайд 10HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
Риски, неудобства и польза
16. В медицинской практике и

в медицинских исследованиях большинство вмешательств сопряжено с определенными рисками и неудобствами.
Медицинское исследование с участием человека в качестве субъекта может проводиться только тогда, когда важность цели исследования превышает риски и неудобства для субъектов исследования.
Слайд 11HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
Риски, неудобства и польза
17. Каждому медицинскому исследованию с

участием человека в качестве субъекта должно предшествовать тщательное сопоставление возможного риска и неудобств для включенных в исследование лиц или групп с ожидаемой пользой как для этих, так и для других лиц или групп населения, страдающих от заболевания/состояния, при котором проводится данное исследование.
Должны быть предприняты меры по минимизации рисков. Риски должны постоянно контролироваться, оцениваться и документироваться исследователями.
Слайд 12HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
18. Врачи не должны принимать участие в исследованиях

с участием людей в качестве субъектов, если они не уверены в том, что произведена надлежащая оценка возможного риска, и что его можно адекватно контролировать.
Если выясняется, что риски превышают ожидаемую пользу, либо становится очевиден определенный исход исследования, врачи должны оценить целесообразность продолжения, изменения либо немедленной остановки исследования.
Слайд 13HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
Уязвимые лица и группы лиц
19. Некоторые лица и

группы лиц являются особо уязвимыми, и есть повышенная вероятность проявления по отношению к ним несправедливости либо причинения дополнительного вреда.
Все уязвимые лица и группы лиц должны получать особую защиту.
20. Медицинское исследование с участием уязвимых групп лиц оправдано только в том случае, если оно имеет отношение к потребностям и приоритетам оказания медицинской помощи именно данной категории лиц и не может быть проведено с участием лиц, не относящихся к уязвимой группе. Кроме того, эта категория лиц должна получать пользу от теоретических и практических знаний или нового метода вмешательства, полученных в результате исследования.
Слайд 14HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
Научные требования и протоколы исследований
21. Медицинские исследования с

участием человека в качестве субъекта должны соответствовать общепринятым научным принципам и основываться на глубоком знании научной литературы, других источников информации, на результатах достаточных лабораторных исследований и, при необходимости, исследований на животных. Необходимо проявлять гуманность по отношению к животным, используемым в исследованиях.
22. Дизайн и порядок выполнения каждого исследования с участием человека в качестве субъекта должны быть четко описаны и обоснованы в протоколе исследования.
Слайд 15HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
Научные требования и протоколы исследований
Протокол должен освещать этические

аспекты исследования и содержать информацию о том, как обеспечивается соблюдение принципов настоящей Декларации. Протокол должен содержать информацию об источниках финансирования, спонсорах исследования, принадлежности к какими-либо организациям, возможных конфликтах интересов, методах стимулирования субъектов исследования и информацию, относящуюся к условиям лечения и/или компенсации субъектам в случае нанесения вреда их здоровью в результате участия в исследовании.
В клинических исследованиях протокол должен также описывать соответствующие условия, действующие после окончания исследования.
Слайд 16HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
Комитеты по этике
23. Перед началом исследования протокол должен

быть направлен для рассмотрения, комментирования, выработки рекомендаций и одобрения в соответствующий комитет по этике. Такой комитет должен быть прозрачен в своей деятельности, независим от исследователя, спонсора и любого иного неуместного влияния, должен иметь надлежащую квалификацию. Он должен учитывать законы и подзаконные акты страны или стран, в которых планируется проведение исследования, а также соответствующие международные нормы и стандарты, которые, однако, не должны умалять или отменять меры по защите субъектов исследования, установленные настоящей Декларацией.
Слайд 17HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
Комитеты по этике
У комитета должно быть право осуществлять

мониторинг текущих исследований. Исследователь обязан предоставлять комитету информацию, необходимую для такого мониторинга, в особенности информацию о любых серьезных нежелательных явлениях. Никакие поправки к протоколу не могут быть внедрены без рассмотрения и одобрения комитета. После окончания исследования исследователи должны представить в комитет финальный отчет, содержащий резюме результатов и выводов исследования.
Слайд 18HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
Частная жизнь и конфиденциальность
24. Должны быть приняты все

меры для защиты частной жизни субъектов исследования и конфиденциальности их персональных данных.
Слайд 19HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
Информированное согласие
25. Участие в качестве субъектов исследования лиц,

способных дать информированное согласие, должно быть добровольным. Несмотря на то, что в ряде случаев может быть уместной консультация с родственниками или лидерами социальной группы, ни одно лицо, способное дать информированное согласие, не может быть включено в исследование, если оно не дало своего собственного добровольного согласия.
Слайд 20HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
Информированное согласие
26. В медицинском исследовании с участием в

качестве субъектов исследования лиц, способных дать информированное согласие, каждый потенциальный субъект должен получить достаточную информацию о целях, методах, источниках финансирования, любых возможных конфликтах интересов, принадлежности к каким-либо организациям, ожидаемой пользе и потенциальных рисках, о неудобствах, которые могут возникнуть вследствие участия в исследовании, условиях, действующих после окончания исследования, а также о любых иных значимых аспектах исследования. Потенциальный субъект исследования должен быть проинформирован о своем праве отказаться от участия в исследовании или отозвать свое согласие на участие в любой момент без каких-либо неблагоприятных для себя последствий. Особое внимание должно уделяться специфическим информационным потребностям каждого потенциального субъекта, а также методам, используемым для предоставления информации.
Слайд 21HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
Убедившись, что потенциальный субъект понял предоставленную ему информацию,

врач или иное лицо, имеющее соответствующую квалификацию, должны получить добровольное информированное согласие субъекта на участие в исследовании, предпочтительно в письменной форме. Если согласие не может быть выражено в письменной форме, должно быть надлежащим образом оформлено и засвидетельствовано устное согласие.
Всем субъектам медицинского исследования должна быть предоставлена возможность получения информации об общих выводах и результатах исследования.
Слайд 22HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
27. При получении информированного согласия на участие в

исследовании врач должен проявлять особую осмотрительность в тех случаях, когда потенциальный субъект находится в зависимом по отношению к врачу положении, или может дать согласие под давлением. В таких случаях информированное согласие должно быть получено лицом, имеющим соответствующую квалификацию и полностью независимым от такого рода отношений.
Слайд 23HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
28. Если потенциальным субъектом исследования является лицо, неспособное

дать информированное согласие, врач должен получить информированное согласие его законного представителя. Такие лица не должны включаться в исследования, которые не несут для них вероятной пользы, кроме случаев, когда такое исследование проводится в целях улучшения оказания медицинской помощи группе людей, представителем которой является потенциальный субъект, не может быть заменено исследованием на лицах, способных дать информированное согласие, а также связано только с минимальными рисками и неудобствами
Слайд 24HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
29. Если потенциальный субъект, признанный не способным дать

информированное согласие, способен, тем не менее, выразить собственное отношение к участию в исследовании, врач должен запросить его мнение в дополнение к согласию его законного представителя. Несогласие потенциального субъекта должно учитываться.
Слайд 25HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
30. Исследования с участием субъектов, физически или психически

неспособных дать согласие, например, пациентов, находящихся в бессознательном состоянии, могут проводиться только при условии, что физическое или психическое состояние, препятствующее получению информированного согласия, является неотъемлемой характеристикой исследуемой группы. В таких случаях врач должен запрашивать информированное согласие у законного представителя. Если такой представитель не доступен, и если включение пациента не может быть отсрочено, исследование может проводиться без получения информированного согласия при условии, что особые причины для включения субъектов в исследование в состоянии, препятствующем предоставлению информированного согласия, оговорены в протоколе исследования, а проведение исследования одобрено комитетом по этике. При первой возможности должно быть получено согласие субъекта или его законного представителя на продолжение участия в исследовании.
Слайд 26HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
31. Врач должен предоставить пациенту полную информацию о

том, какие из аспектов лечения относятся к проводимому исследованию. Отказ пациента участвовать в исследовании или решение о выходе из исследования не должны отражаться на его взаимоотношениях с врачом.
Слайд 27HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
32. В медицинских исследованиях с использованием биологических материалов

или данных, допускающих идентификацию лица, от которого они были получены, например, при исследованиях материалов либо данных, содержащихся в биобанках или аналогичных хранилищах, врач должен получить информированное согласие на получение, хранение и/или повторное использование таких материалов и данных. Могут иметь место исключения, когда получение согласия для такого исследования невозможно или нецелесообразно. В таких случаях исследование может проводиться только после рассмотрения и одобрения комитетом по этике.
Слайд 28HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
Использование плацебо
33. Польза, риски, неудобства и эффективность нового

вмешательства должны оцениваться в сравнении с лучшими из проверенных вмешательств, за исключением следующих случаев:
- когда не существует проверенного метода вмешательства, приемлемым является использование в исследованиях плацебо или отсутствия вмешательства, либо
Слайд 29HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
Использование плацебо
- когда в силу убедительных и научно-обоснованных

методологических причин использование любого вмешательства, менее эффективного, чем лучшее из уже проверенных, а также использование плацебо либо отсутствия вмешательства необходимы для оценки эффективности либо безопасности исследуемого вмешательства, при этом пациенты, получающие вмешательство, менее эффективное, чем лучшее из уже проверенных, плацебо, или не получающие никакого вмешательства, не будут подвергаться дополнительному риску причинения серьезного или необратимого ущерба здоровью в результате неполучения лучшего из уже проверенных вмешательств.
Крайне важно не допускать злоупотребления такой возможностью.
Слайд 30HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
Условия после окончания исследования
34. До начала исследования спонсоры,

исследователи и государственные органы стран, в которых планируется исследование, должны предусмотреть возможность доступа участников исследования к требующейся им терапии, если в процессе исследования выяснилось, что она приносит им пользу. Эта информация должна быть доведена до сведения участников исследования в процессе получения информированного согласия.
Слайд 31HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
Регистрация исследований, публикации и распространение результатов
35. Каждое исследование

с участием людей в качестве субъектов исследования должно быть зарегистрировано в публично доступной базе данных прежде, чем в него будет включен первый субъект.
Слайд 32
Research Registration and Publication and Dissemination of Results
Регистрация исследований, публикации и распространение

результатов
36. Исследователи, авторы, спонсоры, редакторы и издатели несут этические обязательства в отношении публикации и распространения результатов исследования. Исследователи обязаны обеспечить открытый доступ к результатам проведенных ими исследований с участием человека в качестве субъекта, и несут ответственность за полноту и достоверность отчетов об исследованиях. Все стороны должны неукоснительно придерживаться общепринятых этических принципов при подготовке отчетов об исследованиях. Как положительные, так и отрицательные, а также не позволяющие сделать окончательные выводы результаты исследований должны публиковаться или иным образом становиться публично доступными. В публикации должны быть указаны источники финансирования, принадлежность к каким-либо организациям и имеющиеся конфликты интересов. Отчеты об исследованиях, проведенных с нарушением принципов, установленных настоящей Декларацией, не должны приниматься к публикации.
Слайд 33HELSINKI DECLARATION WORLD MEDICAL ASSOCIATION
Непроверенные вмешательства в клинической практике
37. При лечении конкретного

пациента, если проверенных вмешательств не существует или существующие не оказывают должного эффекта, врач, после консультации с экспертами и получения информированного согласия пациента или его законного представителя, может использовать непроверенное вмешательство, если, по мнению врача, его применение дает надежду спасти жизнь пациента, восстановить его здоровье или облегчить страдания. Такое вмешательство должно впоследствии стать объектом исследования, организованного с целью оценки его эффективности и безопасности. В любом случае, вся новая информация должна документироваться и, в соответствующих случаях, становиться публично доступной.
































 Туберкулёз
Туберкулёз Вроджені вади серця. Діагностика, клініка
Вроджені вади серця. Діагностика, клініка Задняя тампонада носа
Задняя тампонада носа Жатырдан кан кетулер
Жатырдан кан кетулер Потребности пациента
Потребности пациента ВИЧ
ВИЧ Как использовать современную медицину и её возможности для продления жизни Удовольствие жить всегда
Как использовать современную медицину и её возможности для продления жизни Удовольствие жить всегда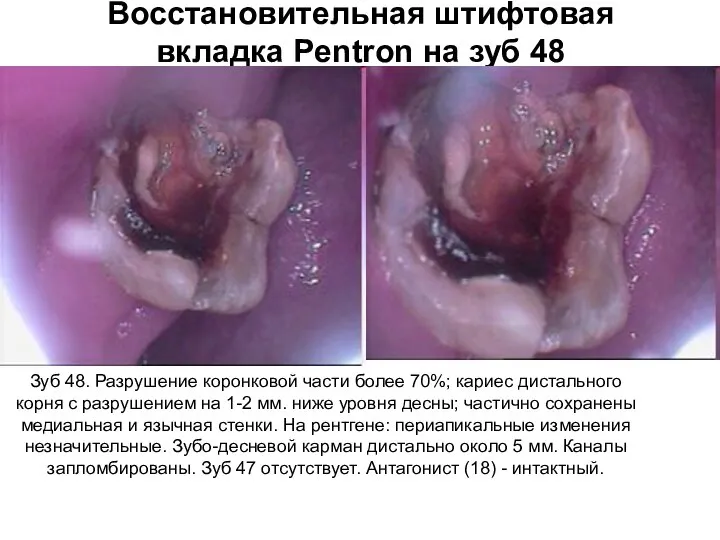 Восстановительная штифтовая вкладка Pentron на зуб 48
Восстановительная штифтовая вкладка Pentron на зуб 48 Функциональная диагностика. Электрокардиография
Функциональная диагностика. Электрокардиография Мерцание и трепетание
Мерцание и трепетание Медсовет по ОНМК
Медсовет по ОНМК Гемотрансфузии. Фильтры
Гемотрансфузии. Фильтры Заболевание глаз
Заболевание глаз Особенности работы цепи передачи электронов в клетках головного мозга. Активация работы митохондрий
Особенности работы цепи передачи электронов в клетках головного мозга. Активация работы митохондрий Нәрестенің бас өлшемдері және иық, жамбас өлшемдері
Нәрестенің бас өлшемдері және иық, жамбас өлшемдері Сбор информации у пациента с сердечной патологией
Сбор информации у пациента с сердечной патологией Максимальные порции для детей по возрастам
Максимальные порции для детей по возрастам Патология дыхательной системы. Очаговая пневмония
Патология дыхательной системы. Очаговая пневмония Вопросы непрерывного медицинского образования. Аккредитация
Вопросы непрерывного медицинского образования. Аккредитация Проба на индивидуальную совместимость по системе АВО
Проба на индивидуальную совместимость по системе АВО Нарушение белкового обмена при патологии печени
Нарушение белкового обмена при патологии печени Информация коронавирус. Как избежать зимней инфекции
Информация коронавирус. Как избежать зимней инфекции Денсаулық сақтаудағы инвестицияның экономикалық бағасы
Денсаулық сақтаудағы инвестицияның экономикалық бағасы Артрозы. Причины и факторы риска развития артроза
Артрозы. Причины и факторы риска развития артроза Обзор современных методов исследований характеристик электрокардиосигналов
Обзор современных методов исследований характеристик электрокардиосигналов Физиологические особенности репродуктивной системы женщины
Физиологические особенности репродуктивной системы женщины Неблагоприятное воздействие лекарственных средств на плод: эмбриотоксичность, тератогенность
Неблагоприятное воздействие лекарственных средств на плод: эмбриотоксичность, тератогенность Сестренский уход при рассеяном склерозе
Сестренский уход при рассеяном склерозе