Содержание
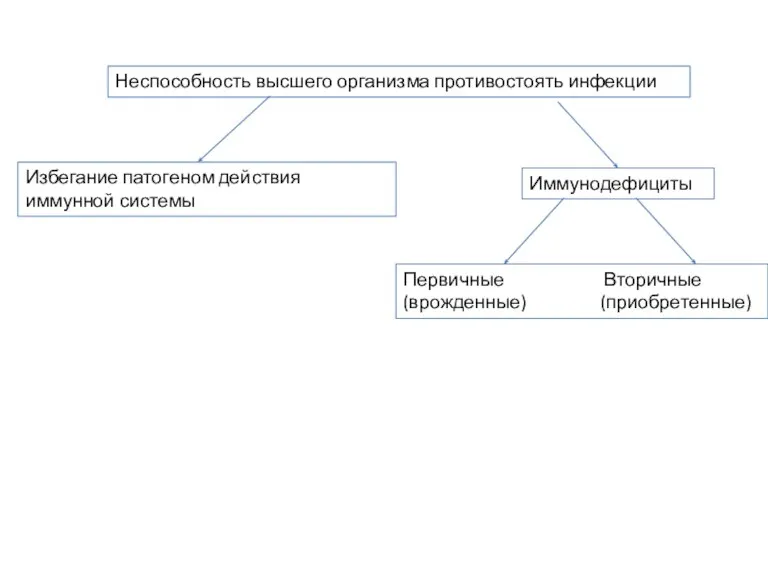
- 2. Иммунодефициты Первичные Вторичные (врожденные) (приобретенные) Неспособность высшего организма противостоять инфекции Избегание патогеном действия иммунной системы
- 3. Многие инфекционные агенты существуют в нескольких антигенных вариантах. Streptococcus pneumoniae – 84 серотипа = 84 варианта
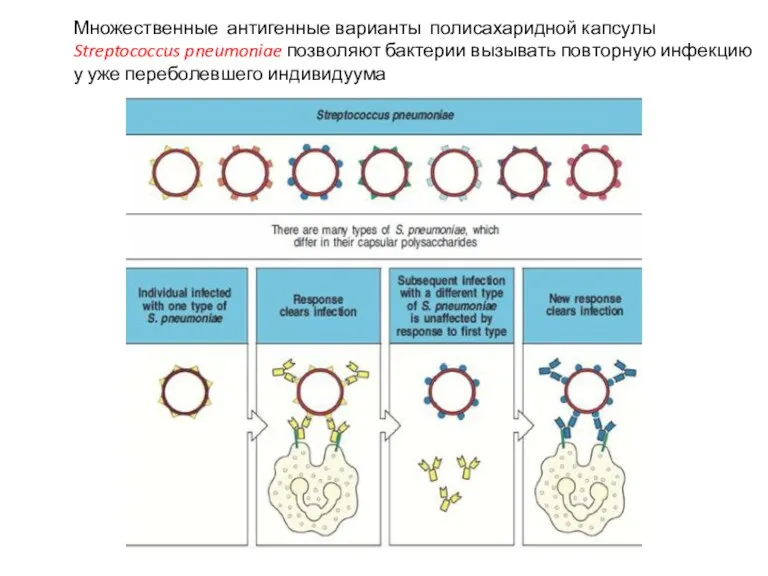
- 4. Множественные антигенные варианты полисахаридной капсулы Streptococcus pneumoniae позволяют бактерии вызывать повторную инфекцию у уже переболевшего индивидуума
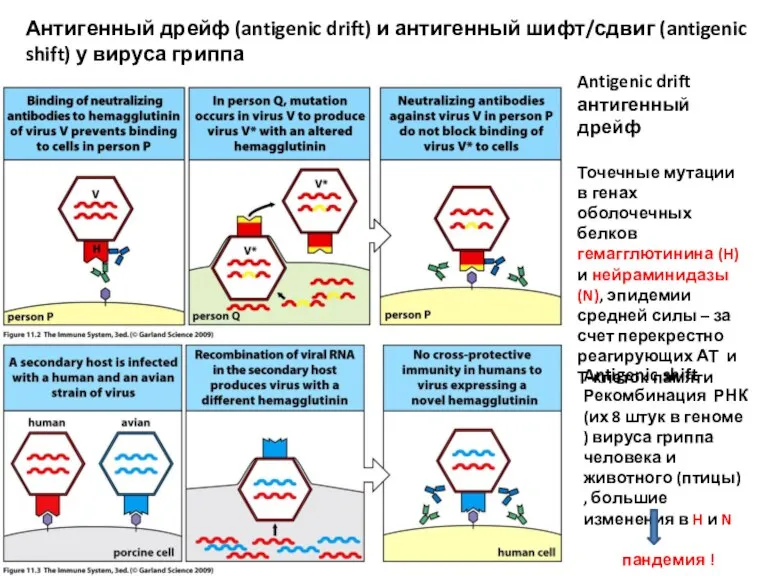
- 5. Антигенный дрейф (antigenic drift) и антигенный шифт/сдвиг (antigenic shift) у вируса гриппа Antigenic drift антигенный дрейф
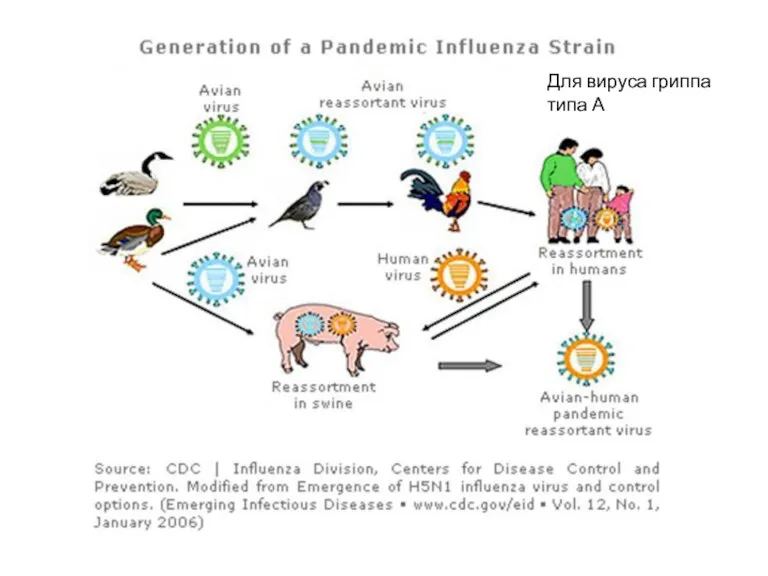
- 6. Для вируса гриппа типа А
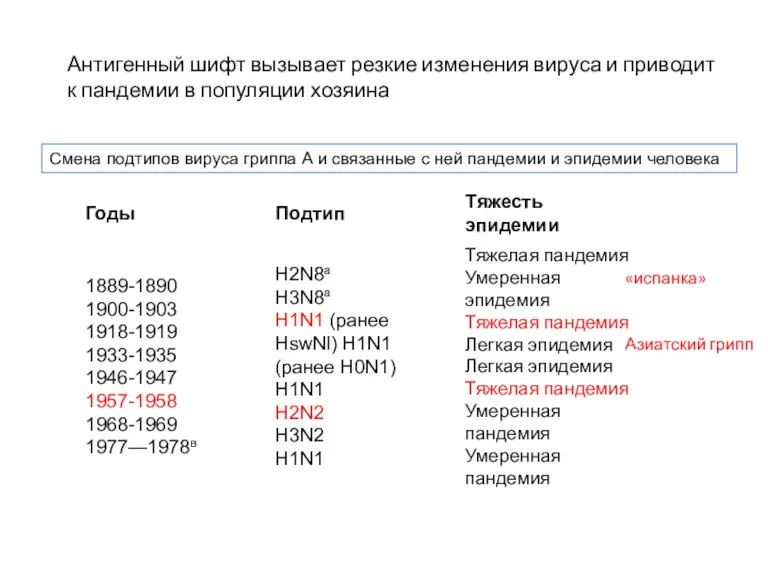
- 7. Смена подтипов вируса гриппа А и связанные с ней пандемии и эпидемии человека Антигенный шифт вызывает
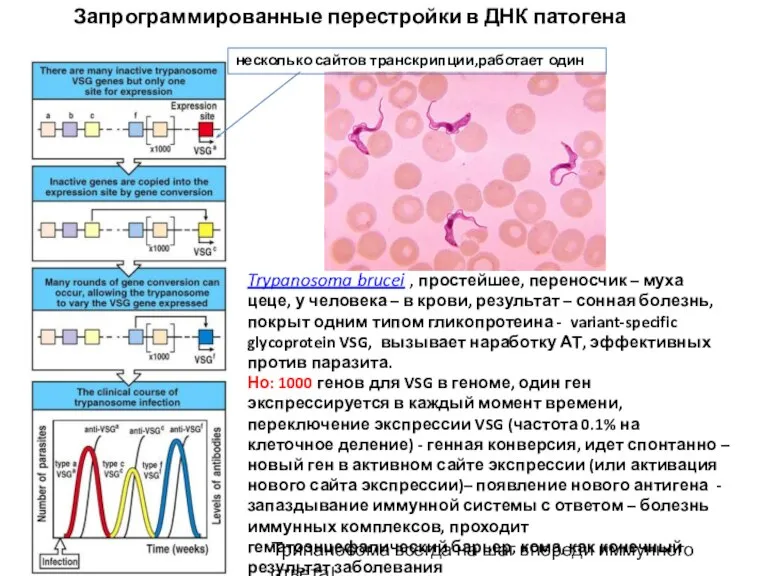
- 8. Запрограммированные перестройки в ДНК патогена Trypanosoma brucei , простейшее, переносчик – муха цеце, у человека –
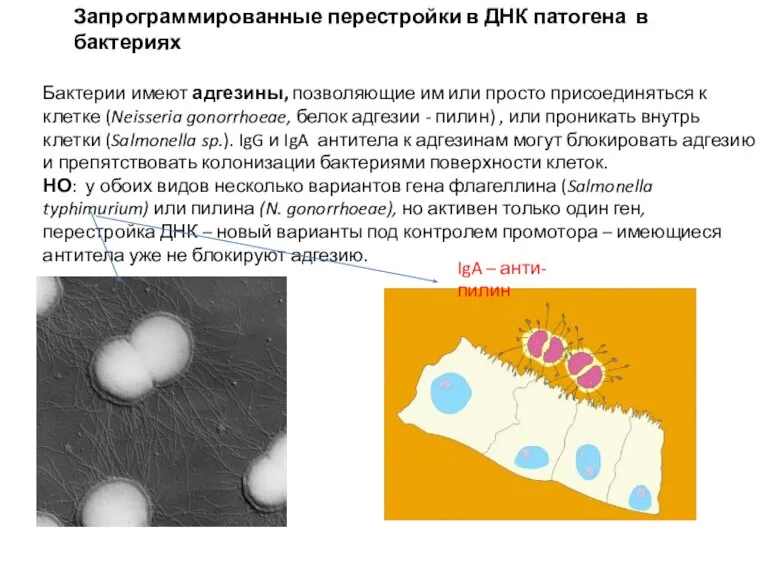
- 9. Бактерии имеют адгезины, позволяющие им или просто присоединяться к клетке (Neisseria gonorrhoeae, белок адгезии - пилин)
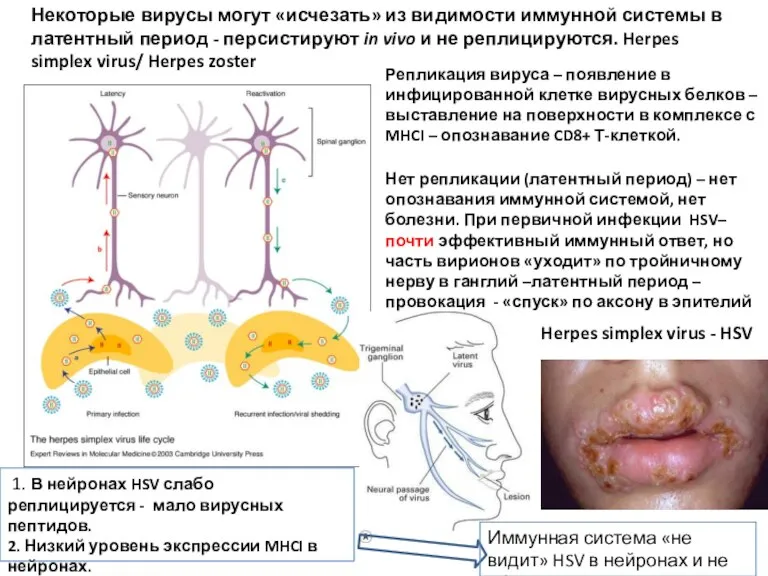
- 10. Некоторые вирусы могут «исчезать» из видимости иммунной системы в латентный период - персистируют in vivo и
- 11. На самом деле, в нервных ганглиях с персистирующим HSV есть CD8+ Т-клетки и CD68+ макрофаги, повышен
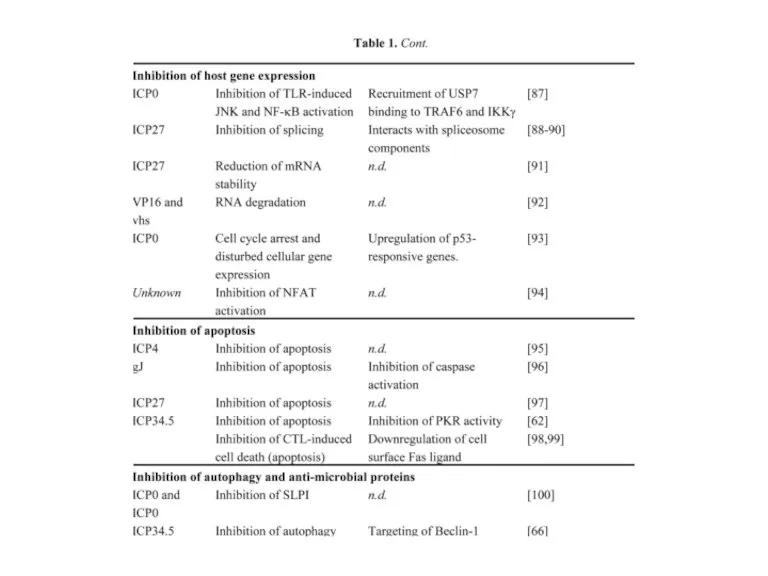
- 12. Каковы молекулярные механизмы избегания вирусом HSV нормального иммунного ответа в клетках эпителия? M. L. Oldham, R.K.
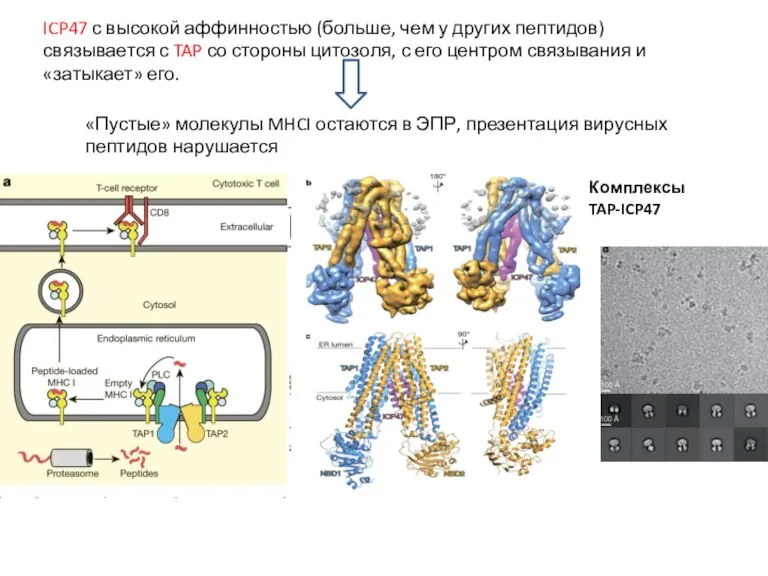
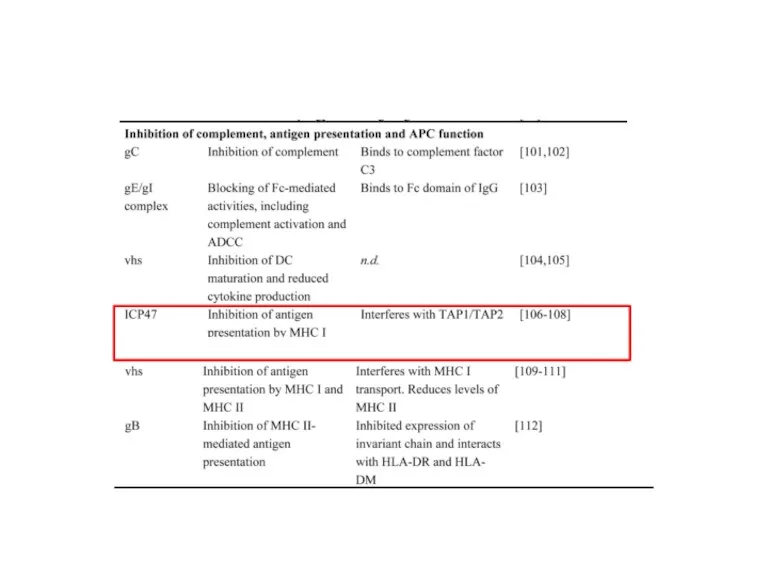
- 13. ICP47 с высокой аффинностью (больше, чем у других пептидов) связывается с TAP со стороны цитозоля, с
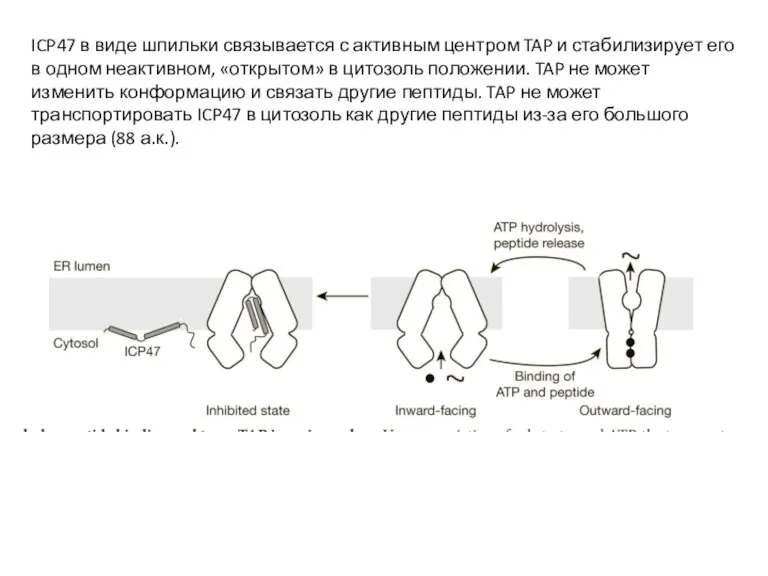
- 14. ICP47 в виде шпильки связывается с активным центром TAP и стабилизирует его в одном неактивном, «открытом»
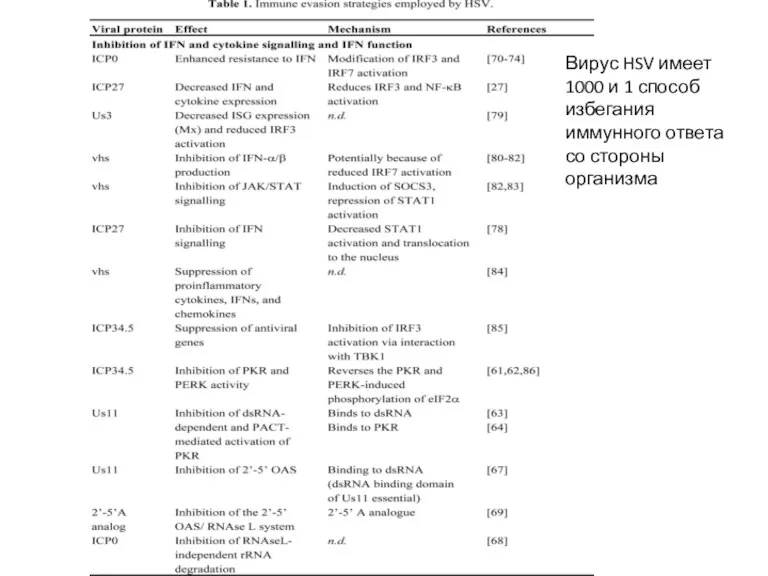
- 15. Вирус HSV имеет 1000 и 1 способ избегания иммунного ответа со стороны организма
- 18. Epstein-Barr virus EBV Инфицирует В-клетки через СD21 и MHCII. Первичная инфекция – или бессимптомно или инфекционный
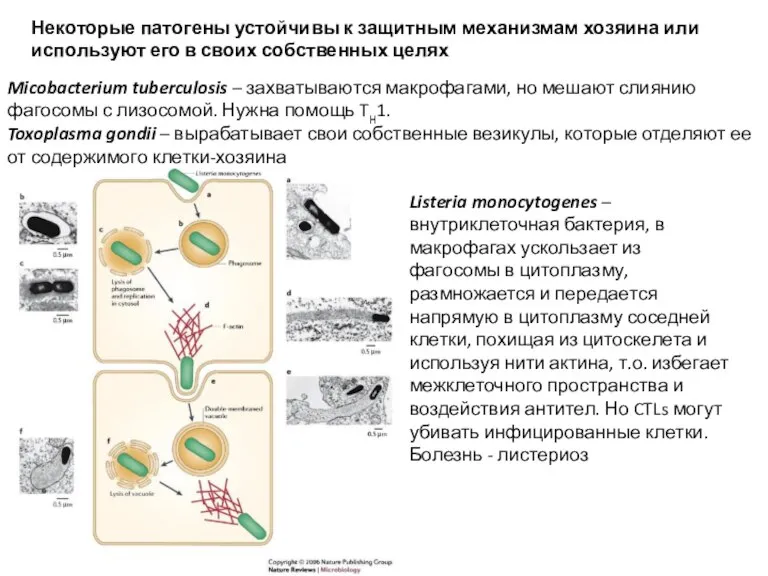
- 19. Некоторые патогены устойчивы к защитным механизмам хозяина или используют его в своих собственных целях Micobacterium tuberculosis
- 20. Врожденные иммунодефициты (более 100) –дефекты в генах, участвующих в контроле иммунного ответа Общая особенность - в
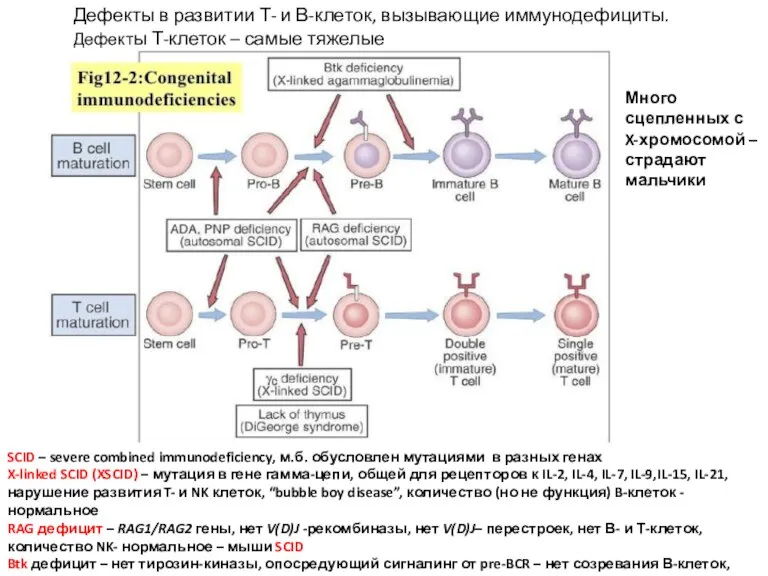
- 21. Дефекты в развитии Т- и В-клеток, вызывающие иммунодефициты. Дефекты Т-клеток – самые тяжелые SCID – severe
- 22. Синдром приобретенного иммунодефицита СПИД/AIDS подавление иммунного ответа, вызванное инфекцией HIV (human immunodeficiency virus) 1981 – первое
- 23. Пути попадания HIV в организм человека: Через слизистую половых путей – основной путь С кровью (через
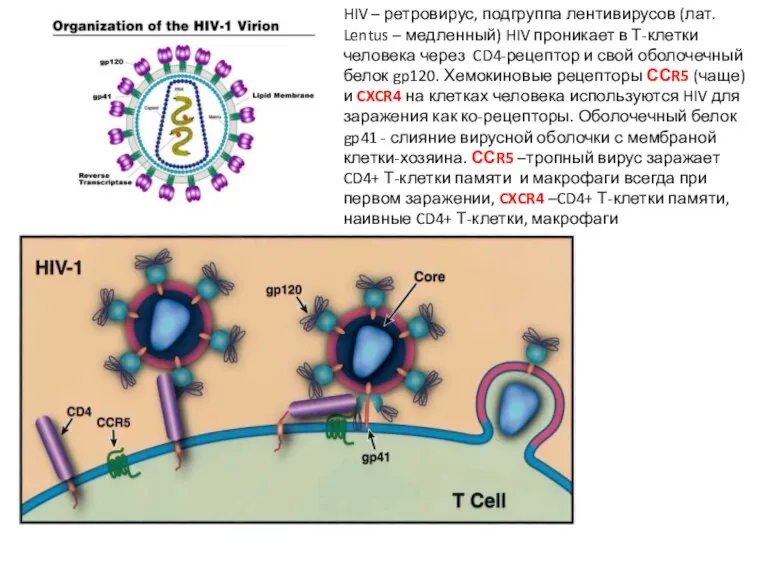
- 24. HIV – ретровирус, подгруппа лентивирусов (лат. Lentus – медленный) HIV проникает в Т-клетки человека через CD4-рецептор
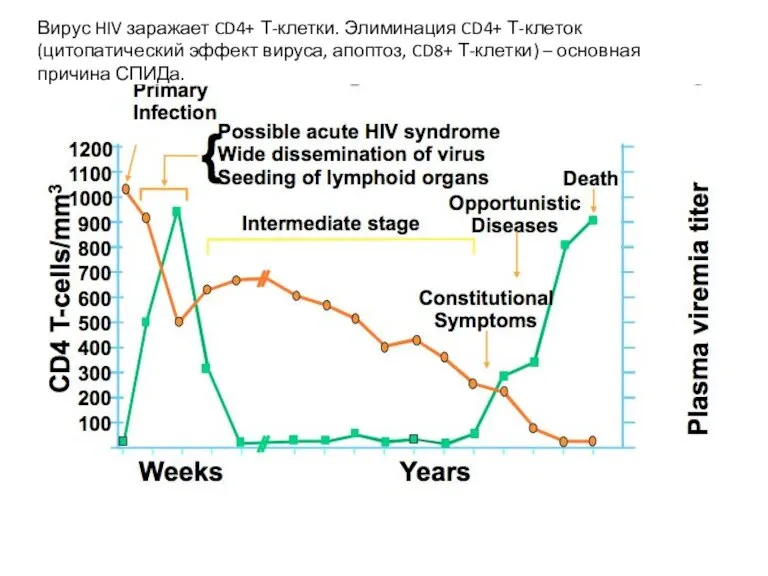
- 25. Вирус HIV заражает CD4+ Т-клетки. Элиминация CD4+ Т-клеток (цитопатический эффект вируса, апоптоз, CD8+ Т-клетки) – основная
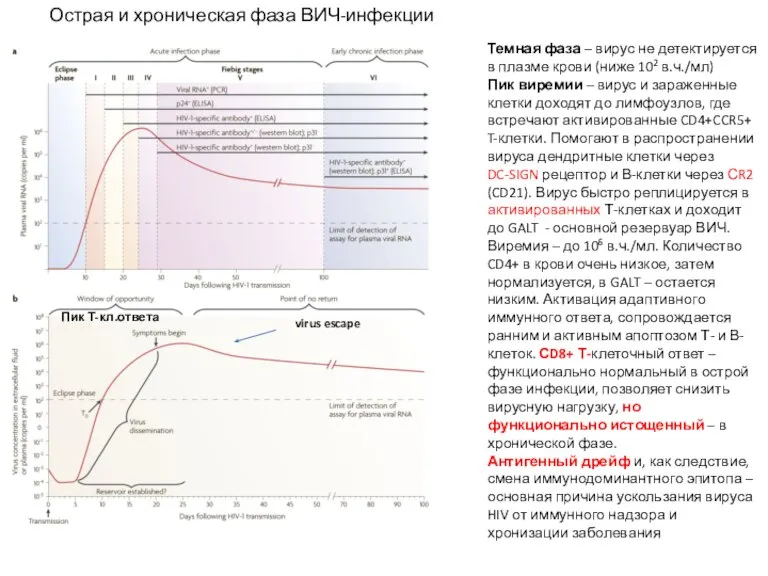
- 26. Темная фаза – вирус не детектируется в плазме крови (ниже 102 в.ч./мл) Пик виремии – вирус
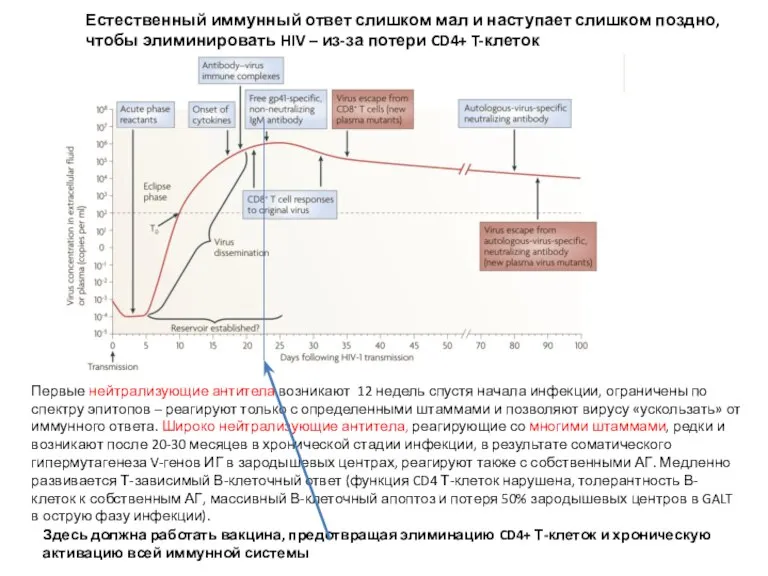
- 27. Первые нейтрализующие антитела возникают 12 недель спустя начала инфекции, ограничены по спектру эпитопов – реагируют только
- 28. Вакцина против ВИЧ должна обеспечивать присутствие широко нейтрализующих антител в плазме и слизистых
- 29. Антигенный дрейф и функциональное истощение CTLs – основные причины неспособности иммунной системы человека элиминировать ВИЧ
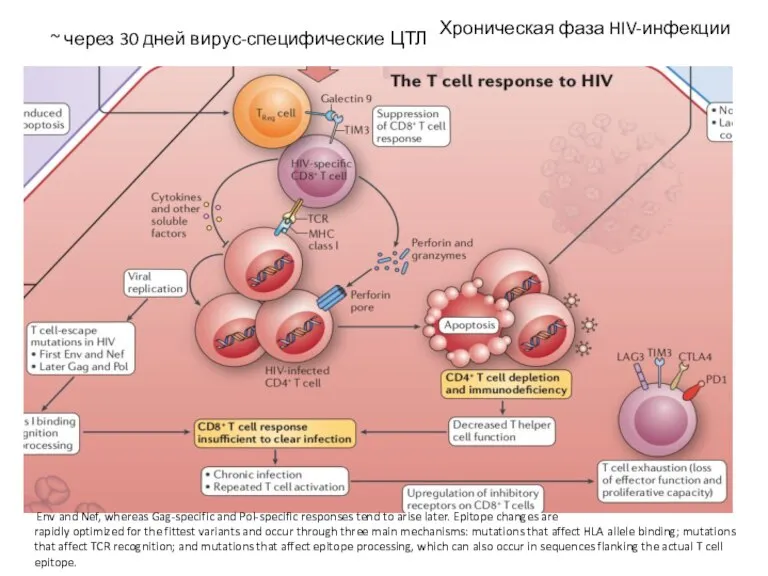
- 30. ~ через 30 дней вирус-специфические ЦТЛ Env and Nef, whereas Gag-specific and Pol-specific responses tend to
- 31. Хроническая фаза ВИЧ-инфекции Результат хронической антигенной стимуляции CD8+ T-клеток и, как следствие, повышенной экспрессии ингибирующих рецепторов
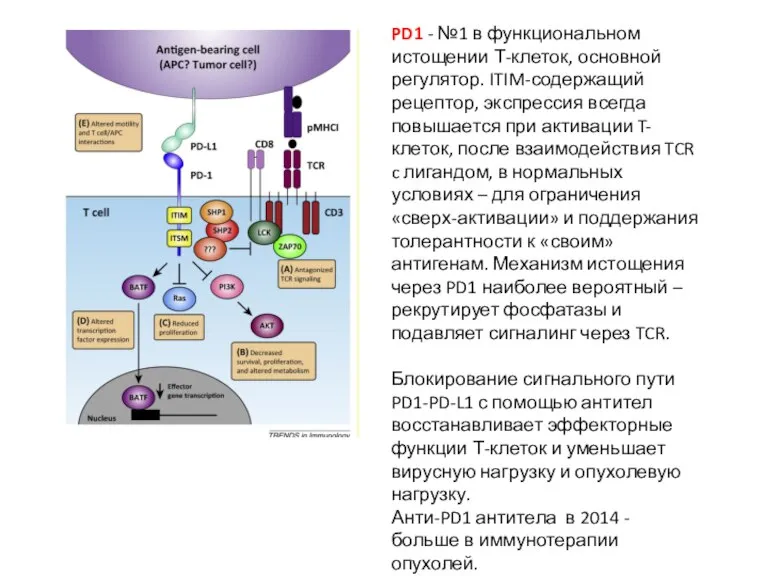
- 32. PD1 - №1 в функциональном истощении Т-клеток, основной регулятор. ITIM-содержащий рецептор, экспрессия всегда повышается при активации
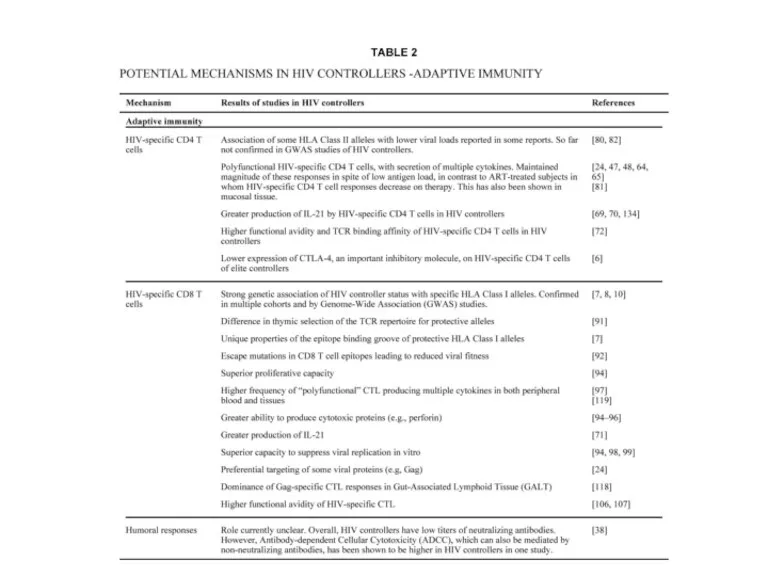
- 33. Около 1% ВИЧ-зараженных – «элит-контроллеры» или «элит-нон-прогрессоры» или «элит-супрессоры». Без ретровирусной терапии – вирусная нагрузка не
- 36. ССR5del Это теперь не зазорно! 2008. Timothy Brown, also known as the «Berlin patient» 1995 –
- 38. Скачать презентацию












 Новий Презентація Microsoft PowerPoint
Новий Презентація Microsoft PowerPoint Фелинотерапия. Перспективы применения совместно с иппотерапией
Фелинотерапия. Перспективы применения совместно с иппотерапией Проекционные зоны коры головного мозга
Проекционные зоны коры головного мозга Важнейшие открытия в медицине нового времени
Важнейшие открытия в медицине нового времени УЗИ предстательной железы
УЗИ предстательной железы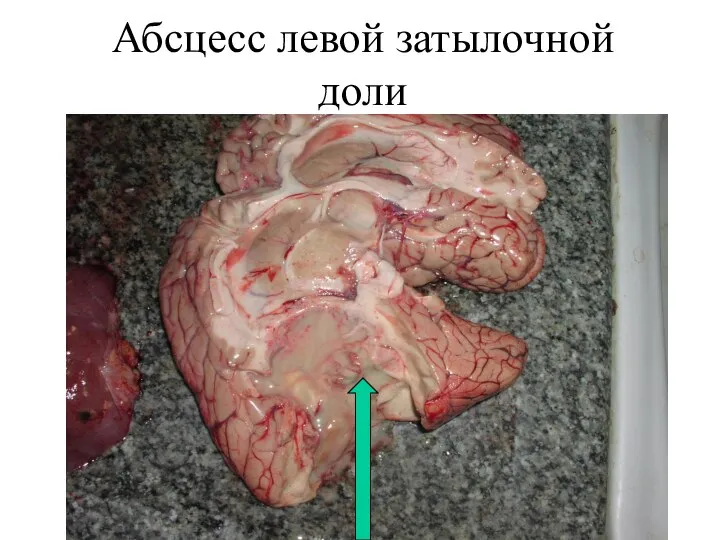 Абсцесс мозга. Препараты
Абсцесс мозга. Препараты Пектин. Применение пектина в медицине
Пектин. Применение пектина в медицине Шок
Шок Амебіаз: клініка, ускладнення, діагностика та лікуванння
Амебіаз: клініка, ускладнення, діагностика та лікуванння Доказательная медицина
Доказательная медицина Дискинезии желчевыводящих путей
Дискинезии желчевыводящих путей Болезнь кленового сиропа
Болезнь кленового сиропа Инфекционные заболевания 21 века
Инфекционные заболевания 21 века Лекарства. Фармакология
Лекарства. Фармакология Магнитно-резонансная томография при патологиях печени
Магнитно-резонансная томография при патологиях печени Сестринский уход при заболеваниях органов дыхания у детей (часть 2)
Сестринский уход при заболеваниях органов дыхания у детей (часть 2) Иммунитет на страже нашего здоровья
Иммунитет на страже нашего здоровья Частная психопатология. Практика 6
Частная психопатология. Практика 6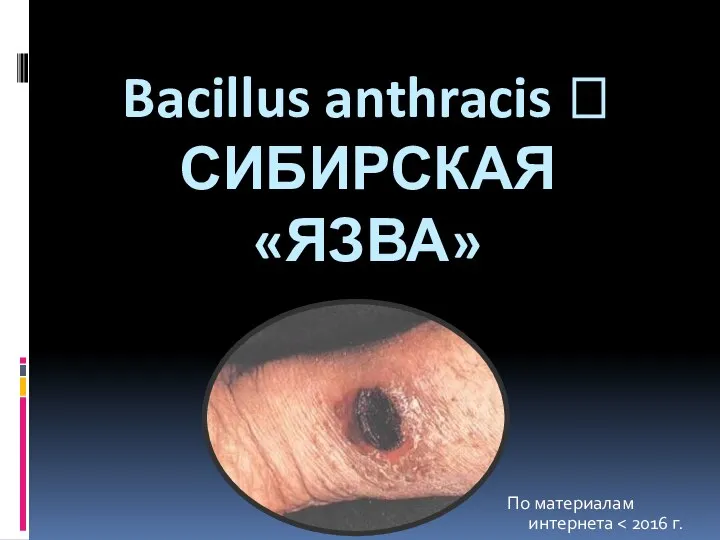 Сибирская язва
Сибирская язва Средства, влияющие на систему крови. Плазмозамещающие средства. Лекция №15
Средства, влияющие на систему крови. Плазмозамещающие средства. Лекция №15 Типы амбулаторно-поликлинических учреждений
Типы амбулаторно-поликлинических учреждений Фармацевтика України
Фармацевтика України Гирудотерапия
Гирудотерапия Хромосомные болезни
Хромосомные болезни Хирургическое лечение глаукомы
Хирургическое лечение глаукомы Перелом голени
Перелом голени Если хочешь быть здоровым. Раздел: Здоровое питание. Урок: Полезные продукты и их значение для организма
Если хочешь быть здоровым. Раздел: Здоровое питание. Урок: Полезные продукты и их значение для организма Вред курения
Вред курения