Содержание
- 2. Классификация анионов
- 3. Ва2+ + SO42- → BaSO4↓ Pb2+ + SO4 2-→ PbSO4 ↓ Ва2+ + СО32-→ ВаСО3↓ Общепринятого
- 4. АНИОНЫ I АНАЛИТИЧЕСКОЙ ГРУППЫ SO42- (сульфат- ион) SO32- (сульфит -ион) S2O32- (тиосульфат-ион) CO32- (карбонат-ион) PO43- (фосфат-ион)
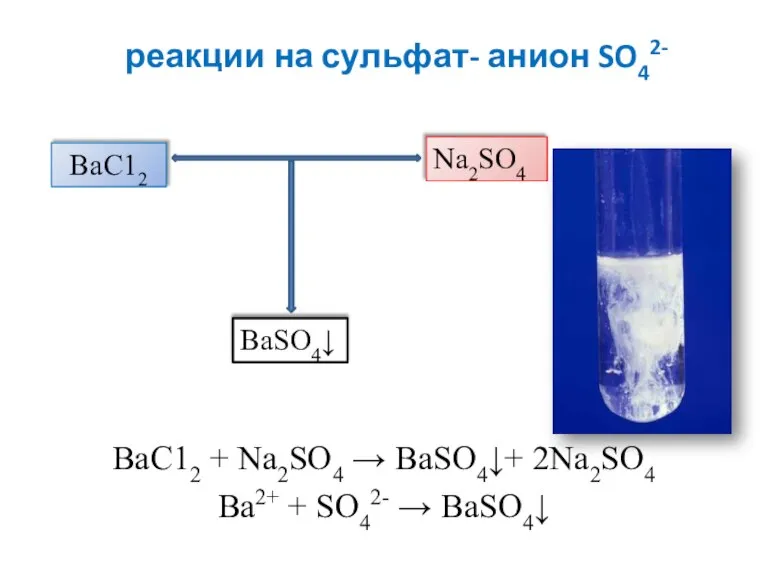
- 5. реакции на сульфат- анион SO42- ВаС12 + Na2SO4 → BaSO4↓+ 2Na2SO4 Ва2+ + SO42- → BaSO4↓
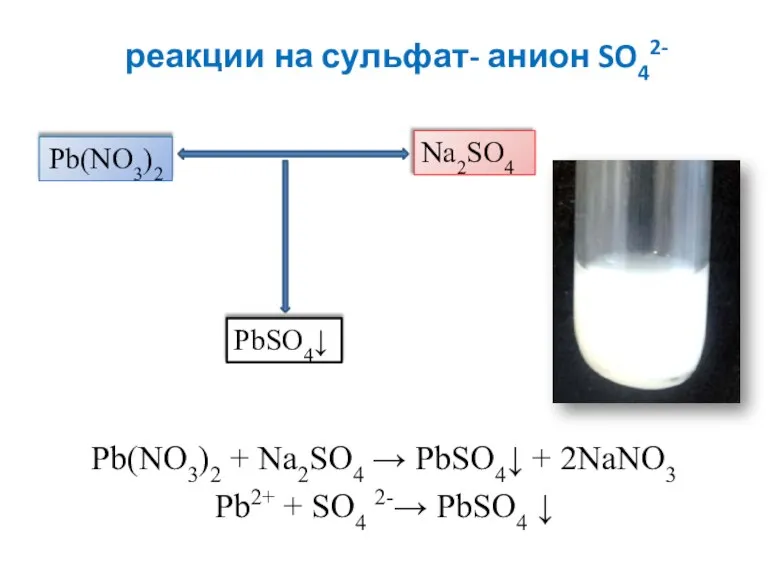
- 6. реакции на сульфат- анион SO42- Pb(NO3)2 + Na2SO4 → PbSO4↓ + 2NaNO3 Pb2+ + SO4 2-→
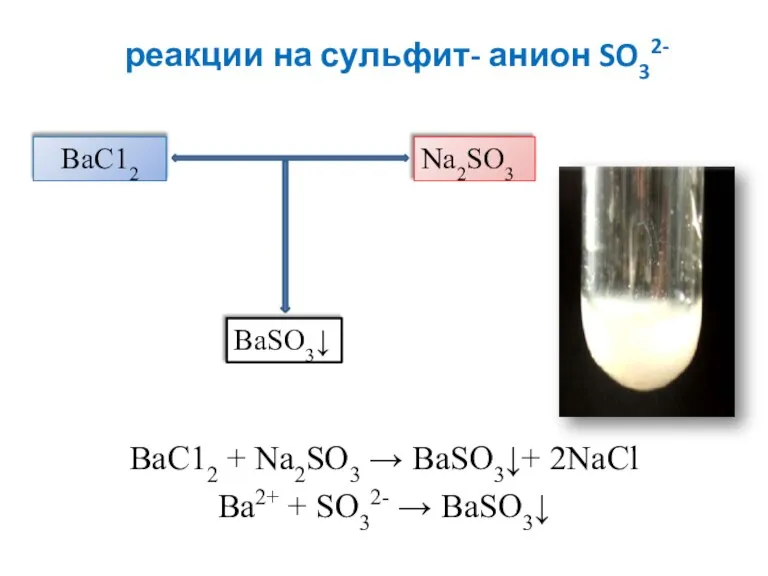
- 7. реакции на сульфит- анион SO32- ВаС12 + Na2SO3 → BaSO3↓+ 2NaCl Ва2+ + SO32- → BaSO3↓
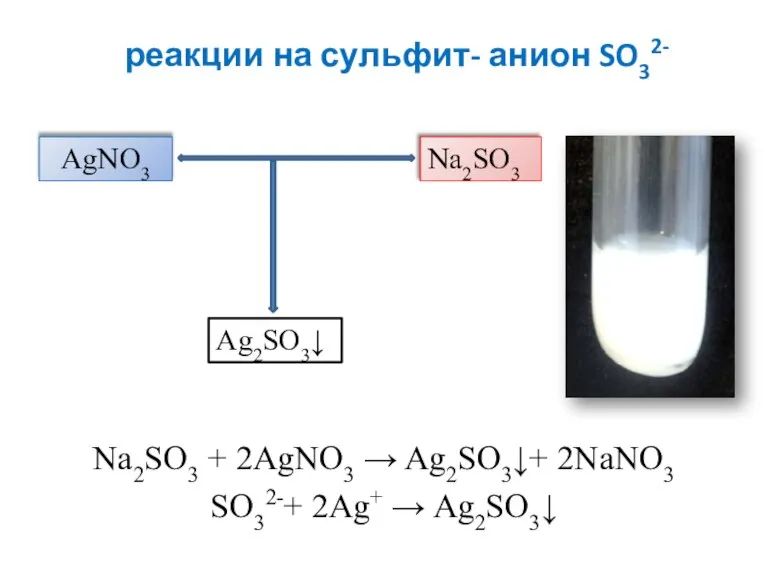
- 8. реакции на сульфит- анион SO32- Na2SO3 + 2AgNO3 → Ag2SO3↓+ 2NaNO3 SO32-+ 2Ag+ → Ag2SO3↓ AgNO3
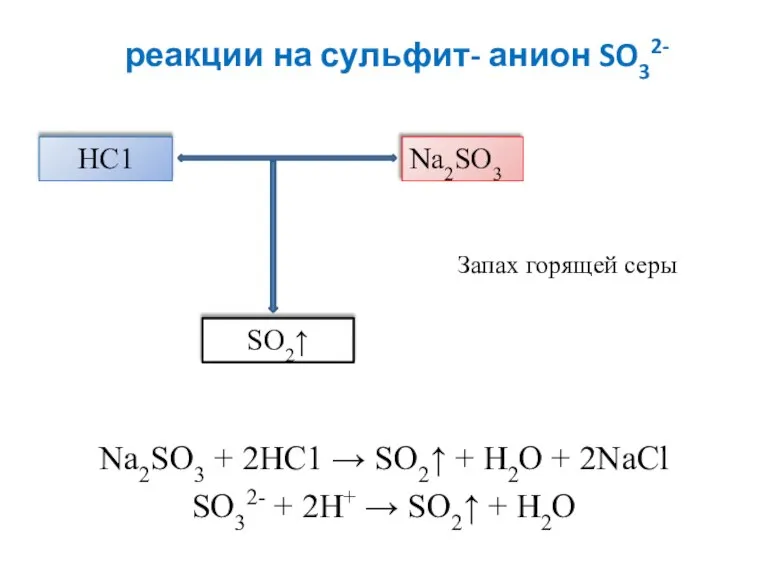
- 9. реакции на сульфит- анион SO32- Na2SO3 + 2НС1 → SO2↑ + Н2О + 2NaCl SO32- +
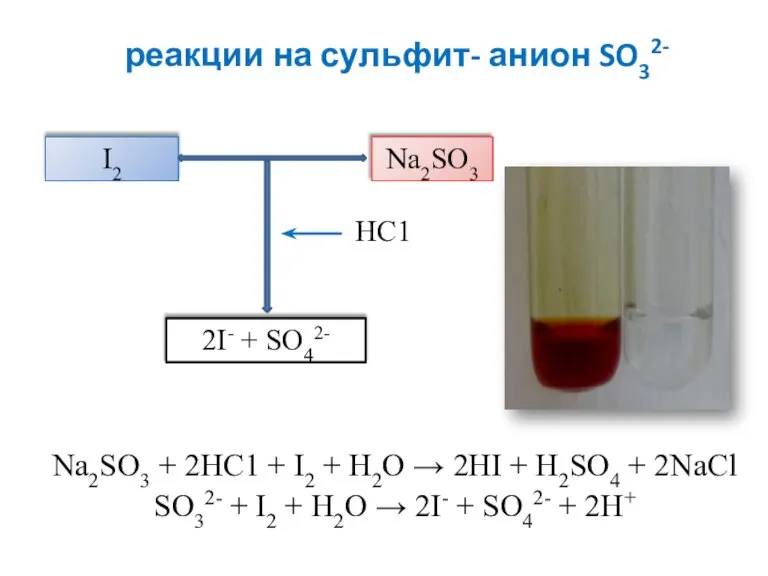
- 10. реакции на сульфит- анион SO32- Na2SO3 + 2НС1 + I2 + Н2О → 2HI + H2SO4
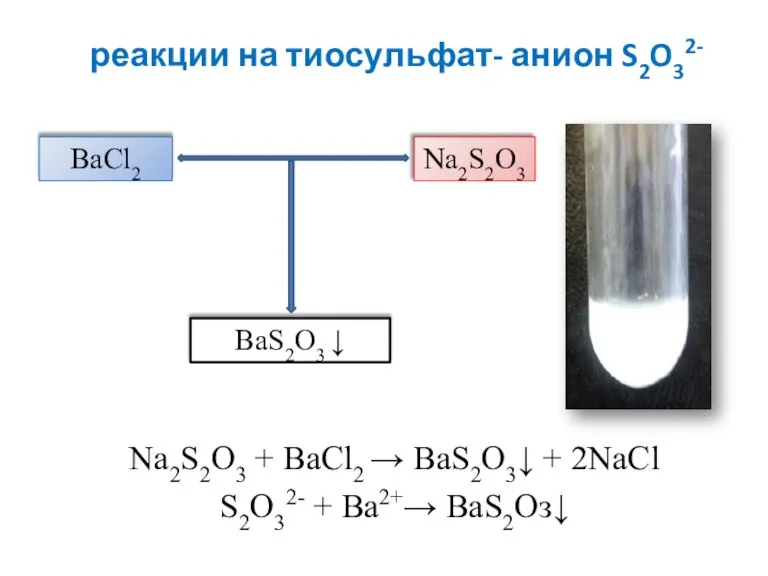
- 11. реакции на тиосульфат- анион S2O32- Na2S2O3 + BaCl2 → ВаS2О3↓ + 2NaCl S2O32- + Ba2+→ ВаS2Оз↓
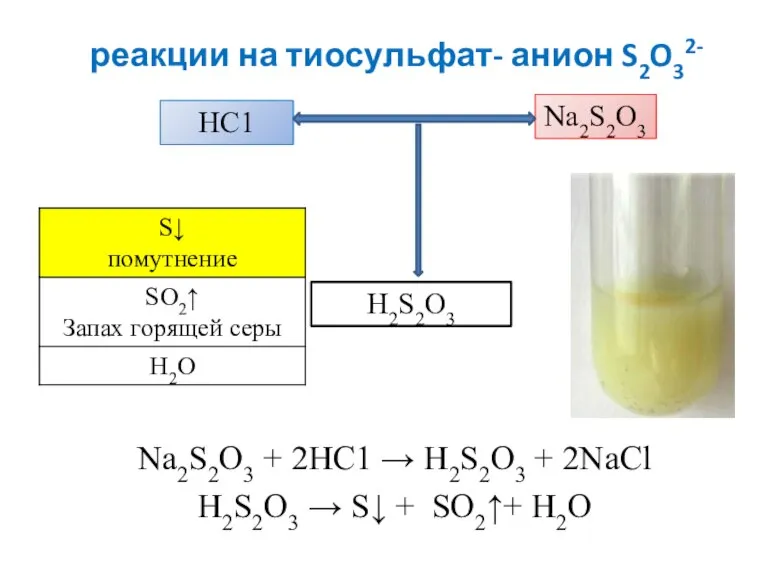
- 12. реакции на тиосульфат- анион S2O32- Na2S2O3 + 2HC1 → H2S2O3 + 2NaCl H2S2O3 → S↓ +
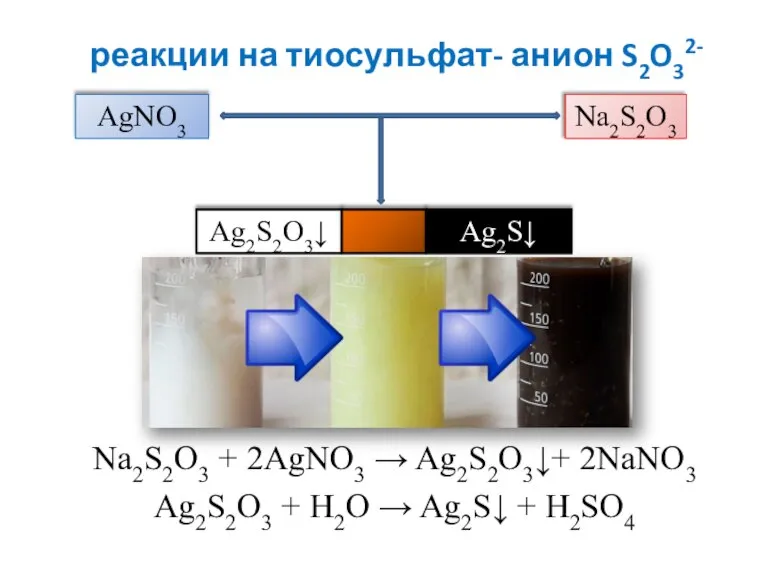
- 13. реакции на тиосульфат- анион S2O32- Na2S2O3 + 2AgNO3 → Ag2S2O3↓+ 2NaNO3 Ag2S2O3 + H2O → Ag2S↓
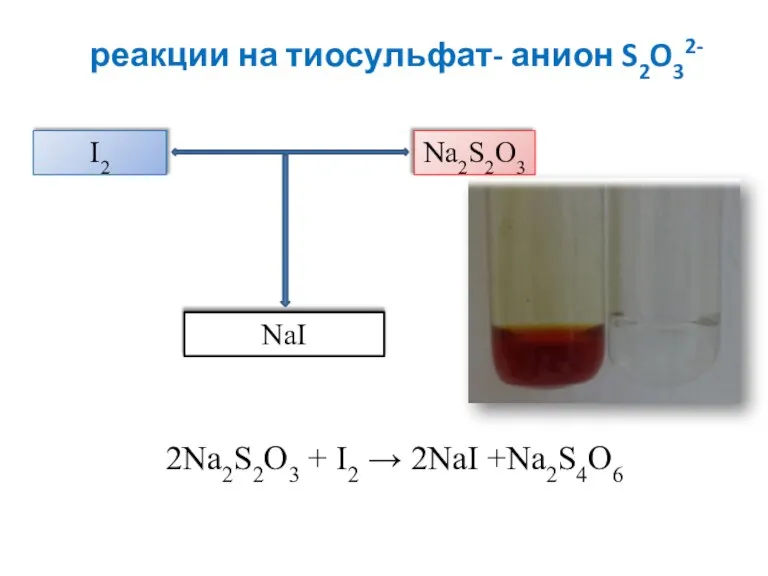
- 14. реакции на тиосульфат- анион S2O32- 2Na2S2O3 + I2 → 2NaI +Na2S4O6 I2 Na2S2O3 NaI
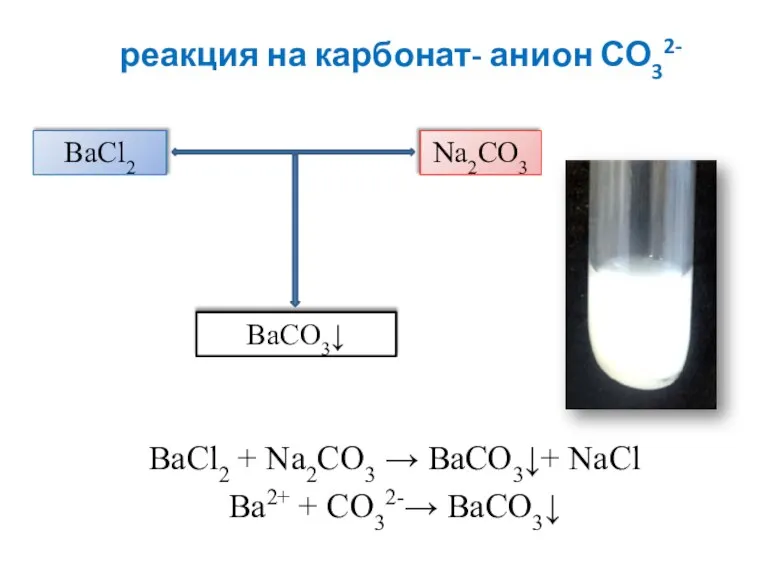
- 15. реакция на карбонат- анион СО32- ВаСl2 + Na2CO3 → ВаСО3↓+ NaCl Ва2+ + СО32-→ ВаСО3↓ ВаСl2
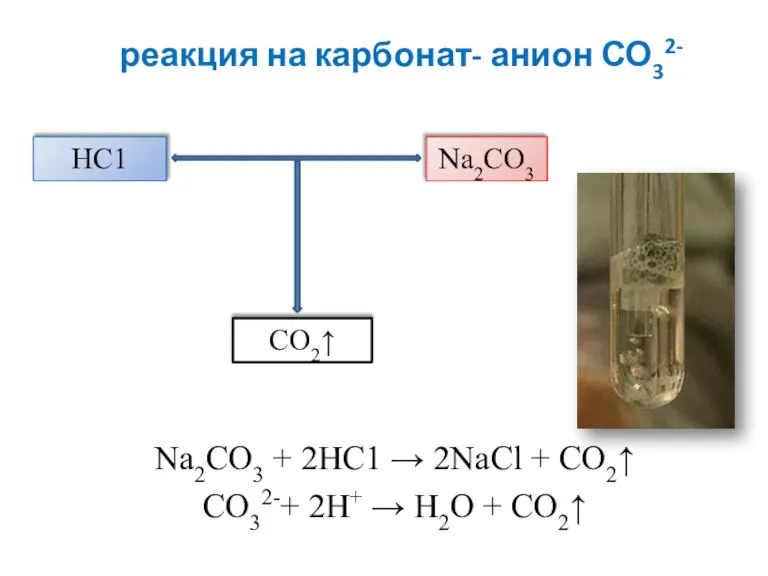
- 16. реакция на карбонат- анион СО32- Na2CO3 + 2HC1 → 2NaCl + CO2↑ CO32-+ 2H+ → H2O
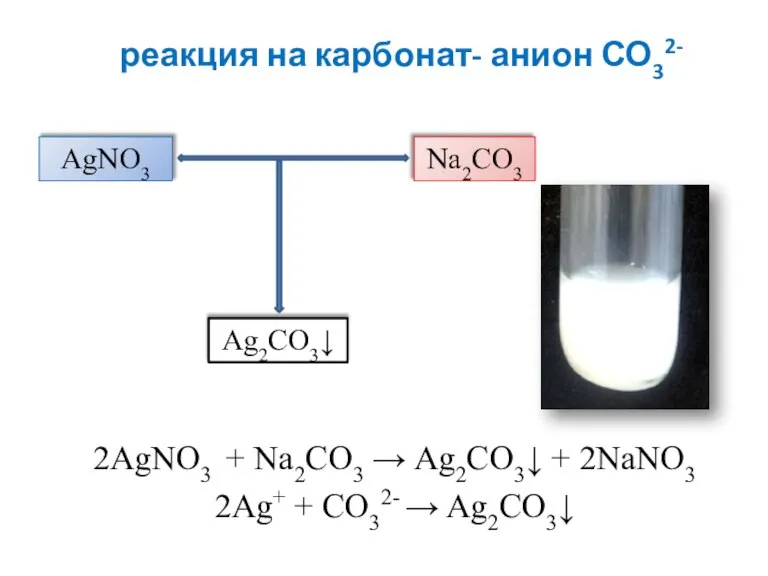
- 17. реакция на карбонат- анион СО32- 2AgNO3 + Na2CO3 → Ag2CO3↓ + 2NaNO3 2Ag+ + CO32- →
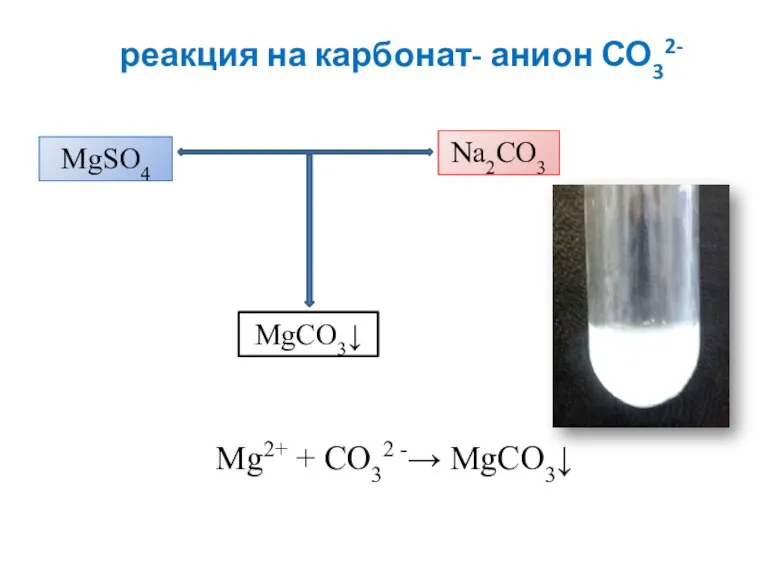
- 18. реакция на карбонат- анион СО32- Мg2+ + CO32 -→ МgCO3↓ МgSO4 Na2CO3 МgCO3↓
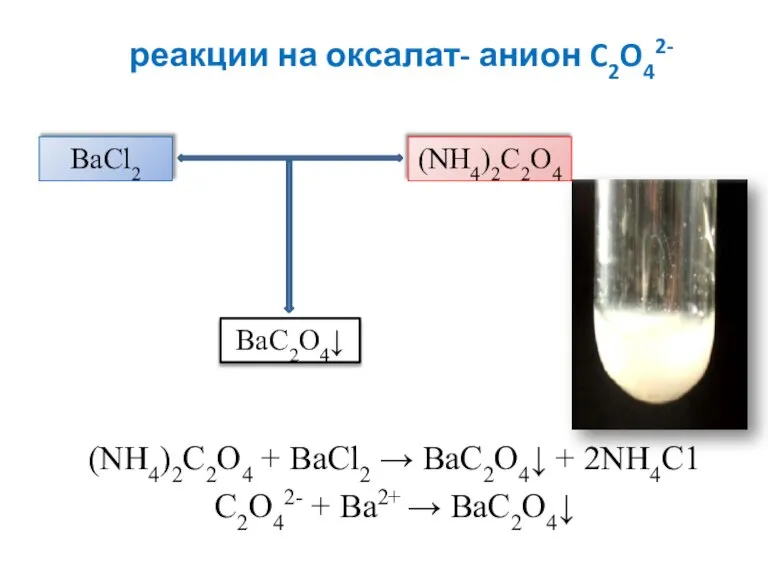
- 19. реакции на оксалат- анион C2O42- (NH4)2C2O4 + BaCl2 → ВаС2O4↓ + 2NH4C1 C2O42- + Ba2+ →
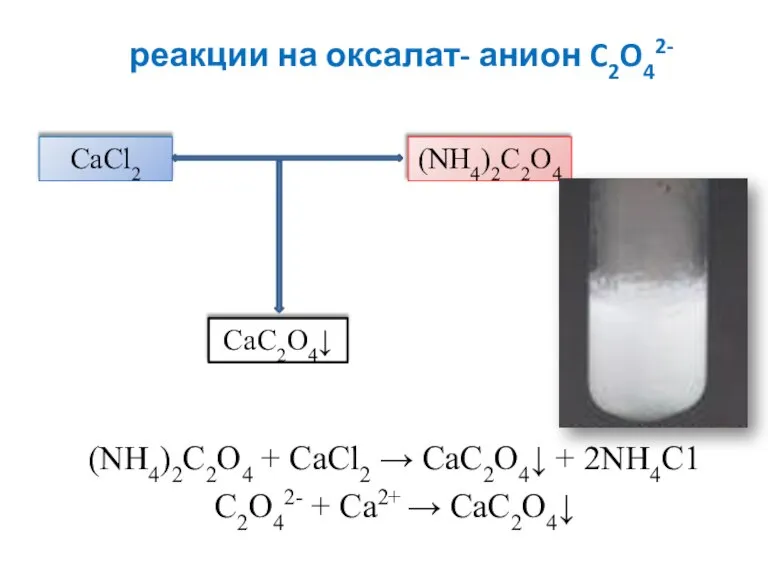
- 20. реакции на оксалат- анион C2O42- (NH4)2C2O4 + CaCl2 → CаС2O4↓ + 2NH4C1 C2O42- + Ca2+ →
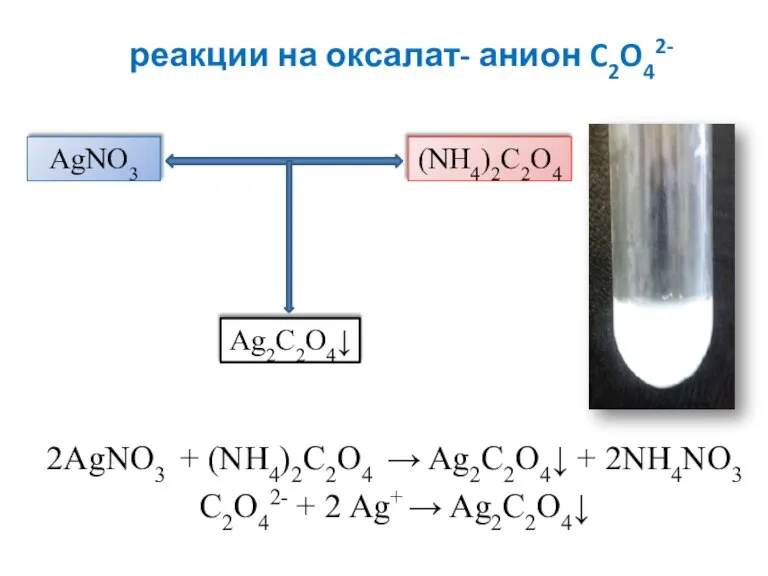
- 21. реакции на оксалат- анион C2O42- 2AgNO3 + (NH4)2C2O4 → Ag2С2O4↓ + 2NH4NO3 C2O42- + 2 Ag+
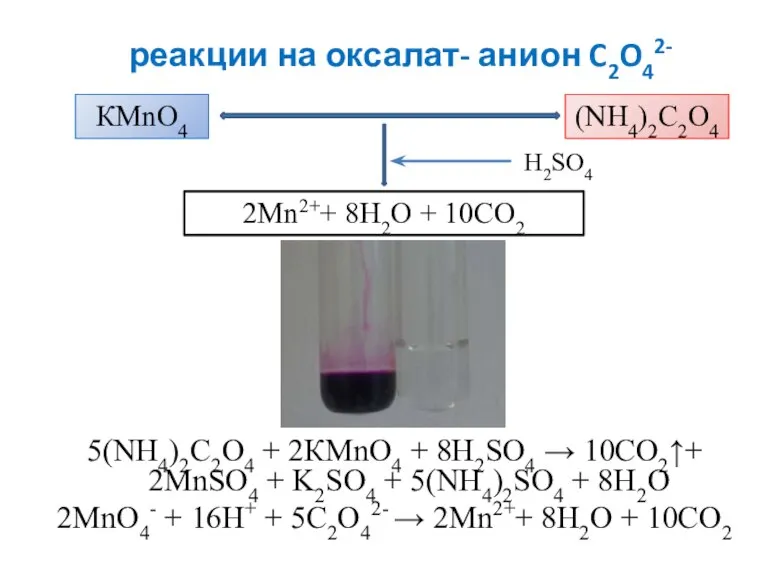
- 22. реакции на оксалат- анион C2O42- 5(NH4)2C2O4 + 2КМnО4 + 8H2SO4 → 10CO2↑+ 2MnSO4 + K2SO4 +
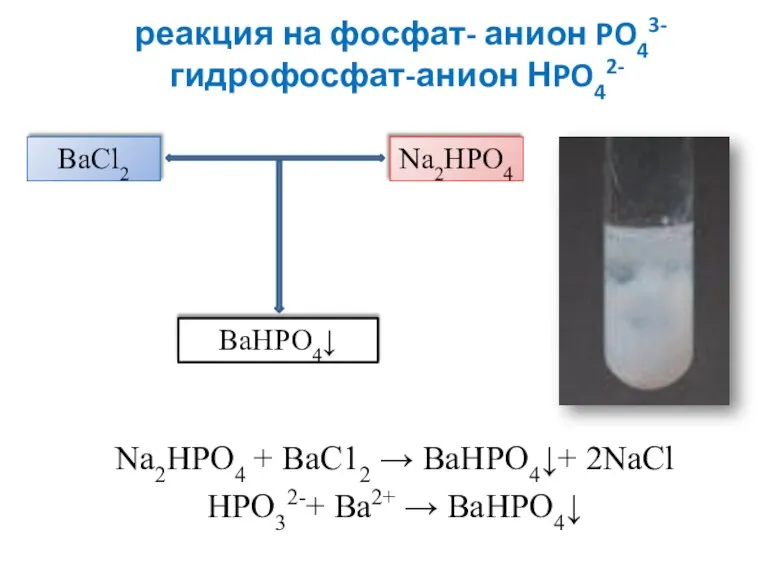
- 23. реакция на фосфат- анион PO43- гидрофосфат-анион НPO42- Na2HPO4 + ВаС12 → ВаНРО4↓+ 2NaCl НРО32-+ Ва2+ →
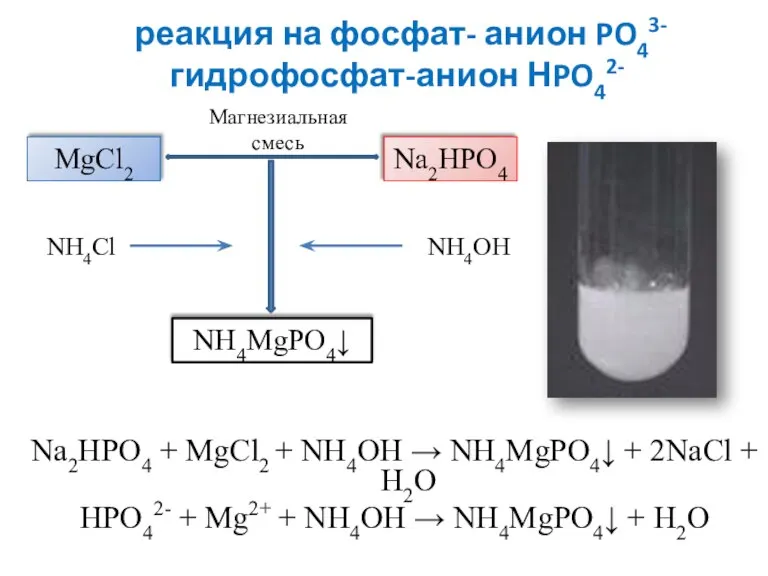
- 24. реакция на фосфат- анион PO43- гидрофосфат-анион НPO42- Na2HPO4 + MgCl2 + NH4OH → NH4MgPO4↓ + 2NaCl
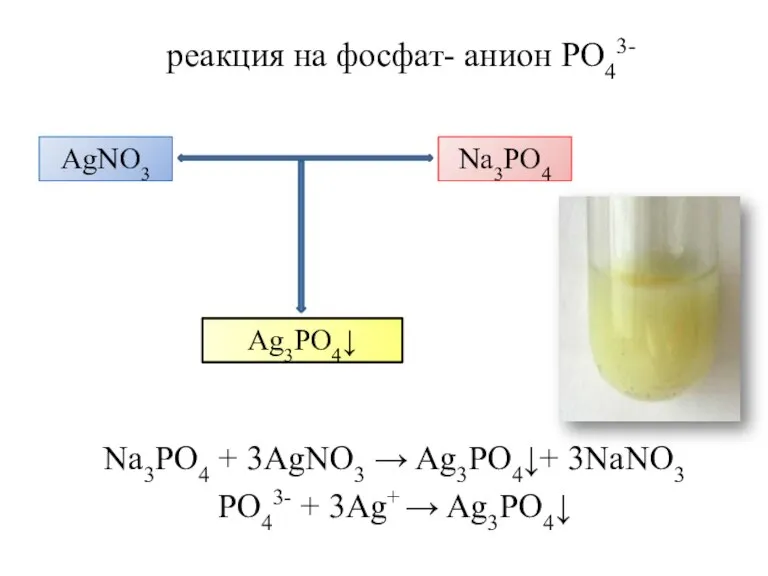
- 25. реакция на фосфат- анион PO43- Na3PO4 + 3AgNO3 → Ag3PO4↓+ 3NaNO3 PO43- + 3Ag+ → Ag3PO4↓
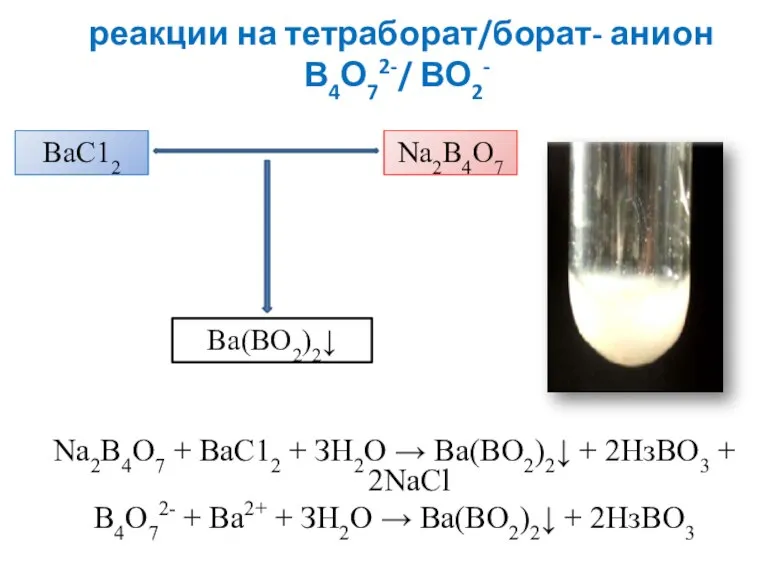
- 26. реакции на тетраборат/борат- анион В4О72-/ ВО2- Na2B4O7 + ВаС12 + ЗН2О → Ba(BO2)2↓ + 2НзВО3 +
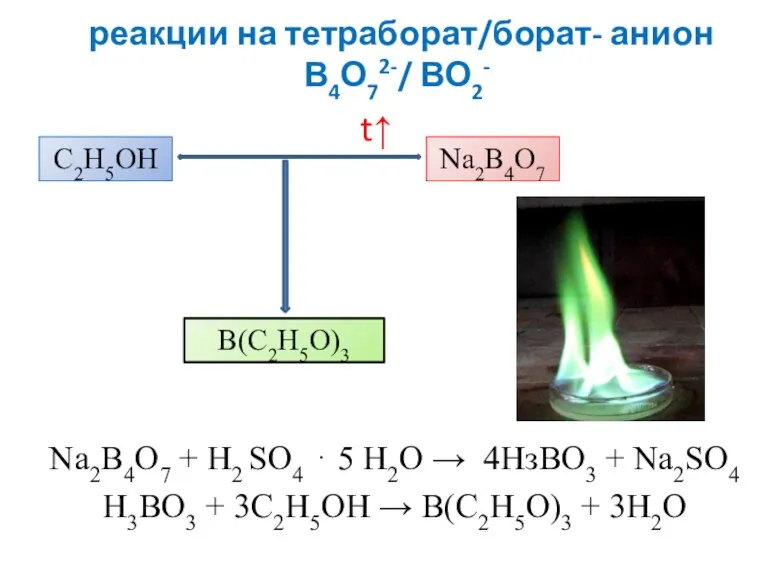
- 27. реакции на тетраборат/борат- анион В4О72-/ ВО2- Na2B4O7 + Н2 SО4 ⋅ 5 H2O → 4НзВО3 +
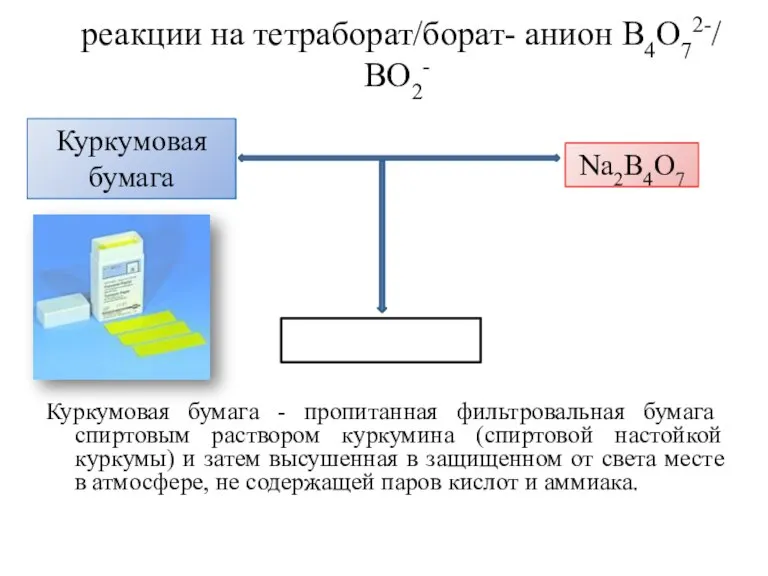
- 28. реакции на тетраборат/борат- анион В4О72-/ ВО2- Куркумовая бумага - пропитанная фильтровальная бумага спиртовым раствором куркумина (спиртовой
- 30. Скачать презентацию



 Тренажёр: знаки химических элементов
Тренажёр: знаки химических элементов Алкены. Физические и химические свойства
Алкены. Физические и химические свойства Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Химически опасные объекты Аварии, связанные с выбросом АХОВ
Химически опасные объекты Аварии, связанные с выбросом АХОВ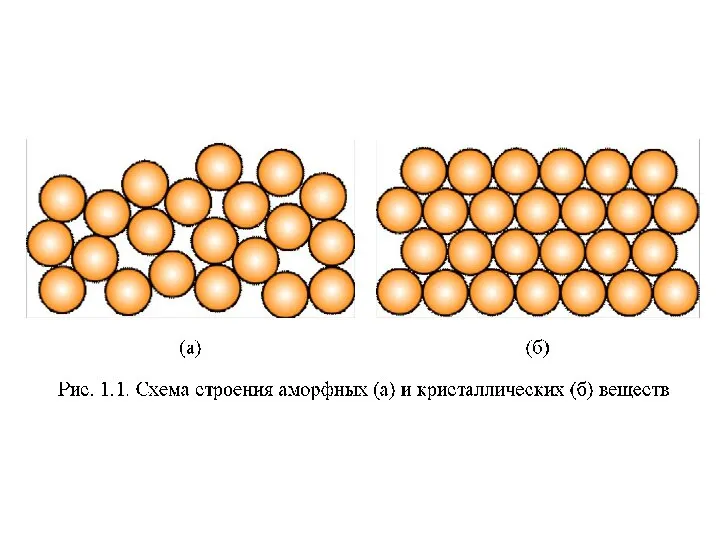 Материаловедение
Материаловедение Синтетические волокна
Синтетические волокна Презентация на тему Неметаллы, особенности строения
Презентация на тему Неметаллы, особенности строения  Электролиз (катод)
Электролиз (катод) Основные принципы работы химических сенсоров
Основные принципы работы химических сенсоров Химическая картина мира
Химическая картина мира Основания: определение, классификация, химические свойства
Основания: определение, классификация, химические свойства Металлы. Общая характеристика, химические свойства. Получение
Металлы. Общая характеристика, химические свойства. Получение Вебинар. Гидролиз солей
Вебинар. Гидролиз солей Свойства радиоактивных элементов
Свойства радиоактивных элементов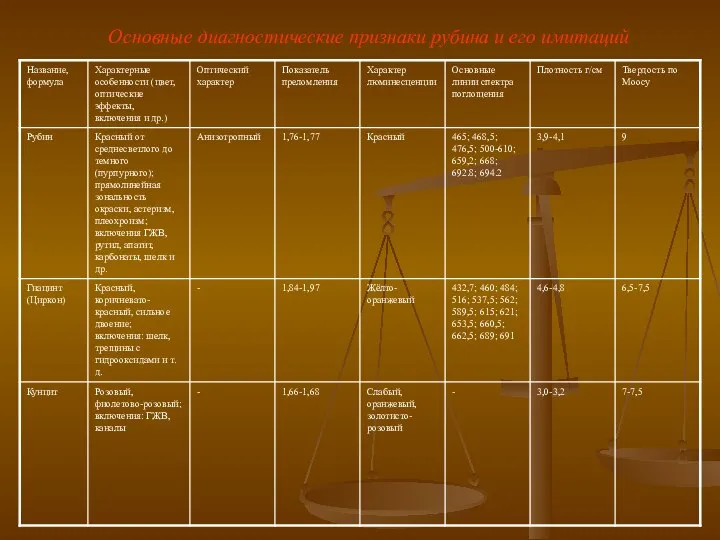 Основные диагностические признаки рубина и его имитаций
Основные диагностические признаки рубина и его имитаций Генетические ряды неорганических соединений
Генетические ряды неорганических соединений Двойные латуни. Диаграмма состояния. Примеси. Структура и свойства
Двойные латуни. Диаграмма состояния. Примеси. Структура и свойства Вуглеводи. Визначення вуглеводів
Вуглеводи. Визначення вуглеводів Галогены. Обобщение знаний
Галогены. Обобщение знаний Подготовка к ГИА по химии
Подготовка к ГИА по химии Предпосылки открытия Периодического закона Д. И. Менделеевым
Предпосылки открытия Периодического закона Д. И. Менделеевым ОВ. Структура и принцип работы параметры ОВ
ОВ. Структура и принцип работы параметры ОВ Абсолютное первенство по химии - 2012
Абсолютное первенство по химии - 2012 строение атома углерода. Валентные состояния атома углерода
строение атома углерода. Валентные состояния атома углерода Общая характеристика элементов IIА группы
Общая характеристика элементов IIА группы Вода… Химические названия
Вода… Химические названия Водород – первый элемент в периодической таблице
Водород – первый элемент в периодической таблице Кристаллы, выращенные учащимися
Кристаллы, выращенные учащимися