Содержание
- 2. Содержание Алкены Номенклатура Изомерия Физические свойства Строение алкенов Химические свойстваХимические свойства (Химические свойства (реакцииХимические свойства (реакции
- 3. Алкены Алкенами или олефинами, или этиленовыми углеводородами называются углеводороды, содержащие в молекуле одну двойную связь и
- 4. Номенклатура Название алкенов по систематической номенклатуре образуют из названий аналогично построенных алканов, заменяя суффиксы –ан на
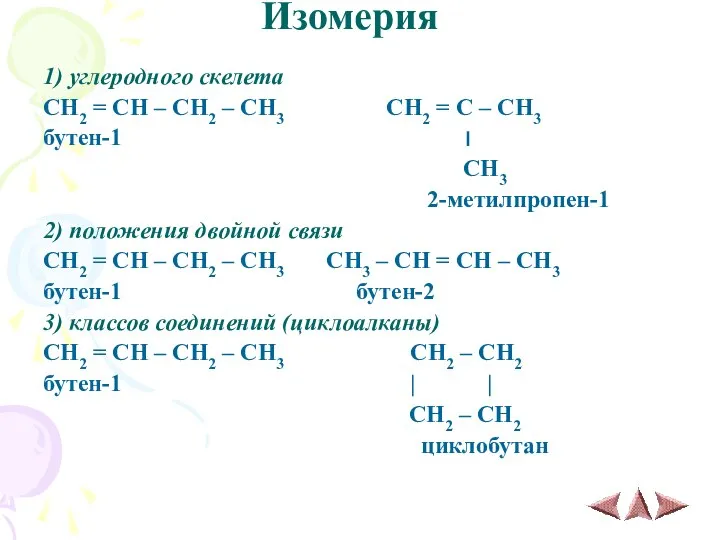
- 5. Изомерия 1) углеродного скелета CH2 = CH – CH2 – CH3 CH2 = C – CH3
- 6. 4) пространственная CH3 H H H \ / \ / C = C C = C
- 7. Физические свойства По физическим свойствам этиленовые углеводороды близки к алканам. При нормальных условиях углеводороды C2–C4 –
- 8. Строение алкенов Углеродные атомы в молекуле этилена находятся в состоянии sp2-гибридизации, т.е. в гибридизации участвуют одна
- 9. Каждая оставшаяся гибридная орбиталь атомов углерода перекрывается с s- орбиталью атомов водорода, приводя к образованию в
- 10. Длина связи λ – расстояние между центрами ядер связанных друг с другом атомов (нм). Энергия связи
- 11. σ-связь – плотность электронного облака максимальна вдоль оси, соединяющей ядра атомов. π–связь – плотность электронного облака
- 12. π- Связь менее прочна, чем σ- связь, так как p- орбитали с параллельными осями перекрываются значительно
- 13. Химические свойства Для алкенов наиболее типичными являются реакции присоединения. 1) Галогенирование. Алкены при обычных условиях присоединяют
- 14. 2) Гидрирование. Легко присоединяют водород в присутствии катализаторов (Pt, Pd, Ni) образуя предельные углеводороды. CH3–CH=CH2 +
- 15. Присоединение галогеноводородов к пропилену и другим несимметричным алкенам происходит в соответствии с правилом В.В.Марковникова (водород присоединяется
- 16. 4) Гидратация. В присутствии минеральных кислот олефины присоединяют воду, образуя спирты. H+ CH3−C=CH2 + H2O →
- 17. Окисление Алкены легко окисляются. В зависимости от условий проведения реакции образуются различные продукты. 1) При сжигании
- 18. 3) При окислении алкенов разбавленным раствором перманганата калия образуются двухатомные спирты – гликоли (реакция Е.Е.Вагнера). Реакция
- 19. Реакция полимеризации. Реакцией полимеризации называется процесс образования высокомолекулярного соединения (полимера) путем соединения друг с другом молекул
- 20. Получение 1) Дегидрогенизация алканов при повышенной температуре с катализатором. CH3–CH2–CH2–CH3 ––300°C,Cr2O3 → CH2=CH–CH2–CH3(бутен-1) + H2 CH3–CH2–CH2–CH3
- 21. Порядок дегидратации вторичных и третичных спиртов определяется правилом А.М.Зайцева: при образовании воды атом водорода отщепляется от
- 22. 4) Реакция дегалогенирования (отщепление двух атомов галогена от соседних атомов углерода) при нагревании дигалогенидов с активными
- 24. Скачать презентацию




















 Тренажёр: знаки химических элементов
Тренажёр: знаки химических элементов Алкены. Физические и химические свойства
Алкены. Физические и химические свойства Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Химически опасные объекты Аварии, связанные с выбросом АХОВ
Химически опасные объекты Аварии, связанные с выбросом АХОВ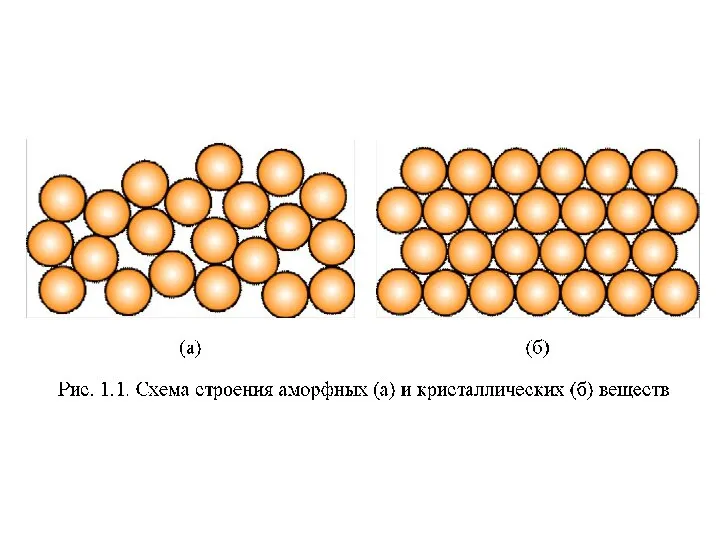 Материаловедение
Материаловедение Синтетические волокна
Синтетические волокна Презентация на тему Неметаллы, особенности строения
Презентация на тему Неметаллы, особенности строения  Электролиз (катод)
Электролиз (катод) Основные принципы работы химических сенсоров
Основные принципы работы химических сенсоров Химическая картина мира
Химическая картина мира Основания: определение, классификация, химические свойства
Основания: определение, классификация, химические свойства Металлы. Общая характеристика, химические свойства. Получение
Металлы. Общая характеристика, химические свойства. Получение Вебинар. Гидролиз солей
Вебинар. Гидролиз солей Свойства радиоактивных элементов
Свойства радиоактивных элементов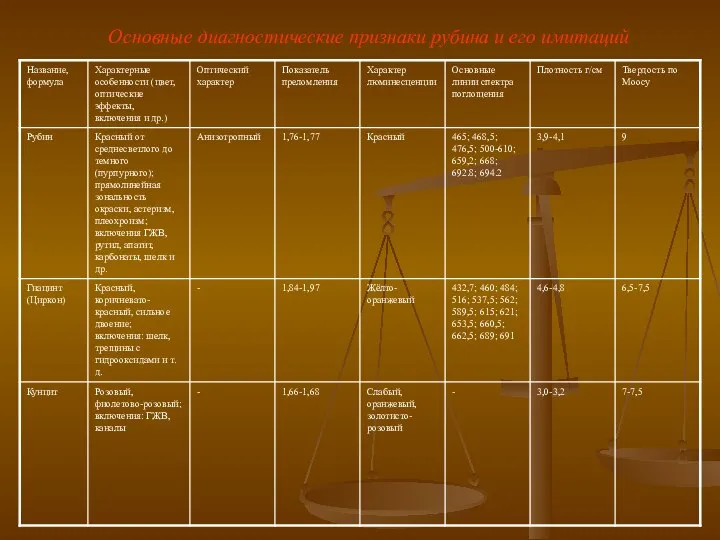 Основные диагностические признаки рубина и его имитаций
Основные диагностические признаки рубина и его имитаций Генетические ряды неорганических соединений
Генетические ряды неорганических соединений Двойные латуни. Диаграмма состояния. Примеси. Структура и свойства
Двойные латуни. Диаграмма состояния. Примеси. Структура и свойства Вуглеводи. Визначення вуглеводів
Вуглеводи. Визначення вуглеводів Галогены. Обобщение знаний
Галогены. Обобщение знаний Подготовка к ГИА по химии
Подготовка к ГИА по химии Предпосылки открытия Периодического закона Д. И. Менделеевым
Предпосылки открытия Периодического закона Д. И. Менделеевым ОВ. Структура и принцип работы параметры ОВ
ОВ. Структура и принцип работы параметры ОВ Абсолютное первенство по химии - 2012
Абсолютное первенство по химии - 2012 строение атома углерода. Валентные состояния атома углерода
строение атома углерода. Валентные состояния атома углерода Общая характеристика элементов IIА группы
Общая характеристика элементов IIА группы Вода… Химические названия
Вода… Химические названия Водород – первый элемент в периодической таблице
Водород – первый элемент в периодической таблице Кристаллы, выращенные учащимися
Кристаллы, выращенные учащимися