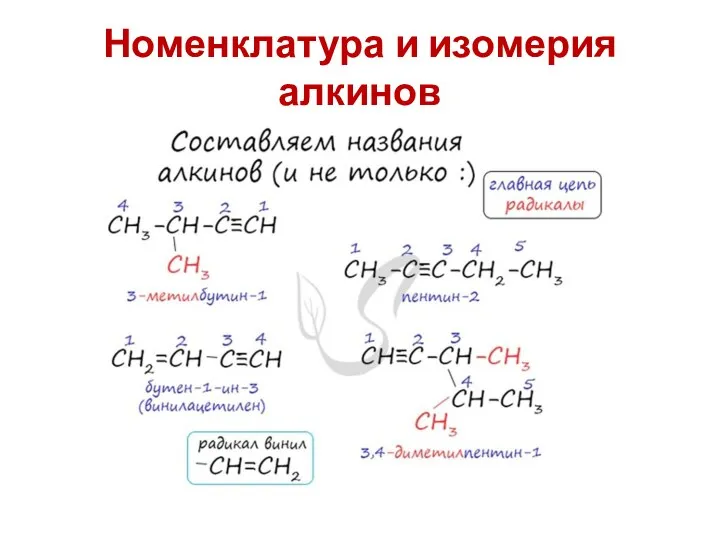
Слайд 2Номенклатура и изомерия алкинов
Слайд 3В молекулах алканов присутствуют тройные связи, длина которых составляет 0,121 нм
Тип гибридизации
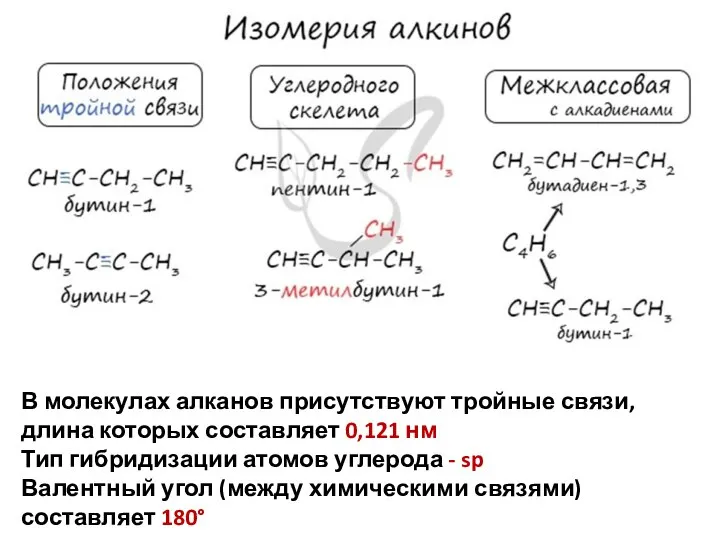
атомов углерода - sp
Валентный угол (между химическими связями) составляет 180°
Слайд 4Получение алкинов
1. Пиролиз метана
При нагревании метана до 1000 °C происходит димеризация молекул метана,

в ходе чего отщепляется водород.
2CH4 → (t) CH≡CH + 3H2
2. Синтез Бертло
Осуществляется напрямую, из простых веществ. Протекает на вольтовой (электрической) дуге, в атмосфере водорода.
2C + H2 → (t, вольтова дуга) CH≡CH
3. Разложение карбида кальция
В результате разложения карбида кальция образуется ацетилен и гидроксид кальция II.
CaC2 + 2H2O → CH≡CH + Ca(OH)2
Слайд 5Получение гомологов ацетилена возможно в реакциях дегидрогалогенирования дигалогеналканов, в которых атомы галогена

расположены у одного атома углерода или у двух соседних атомов.
Слайд 6Химические свойства алкинов
1. Гидрирование
Водород присоединяется к атомам углерода, образующим тройную связь. Пи-связи (π-связи)

рвутся, остается единичная сигма-связь (σ-связь).
CH≡C-CH3 + H2 → (t, Ni) CH2=CH-CH3
(в реакции участвует 1 моль водорода)
CH2=CH-CH3 + H2 → (t, Ni) CH3-CH2-CH3
(в реакции участвует 1 моль водорода)
CH≡CH + 2H2 → (t, Ni) CH3-CH3
(в реакции участвует 2 моль водорода)
Слайд 72. Галогенирование
Реакция с бромной водой является качественной для непредельных соединений, содержащих двойные (и
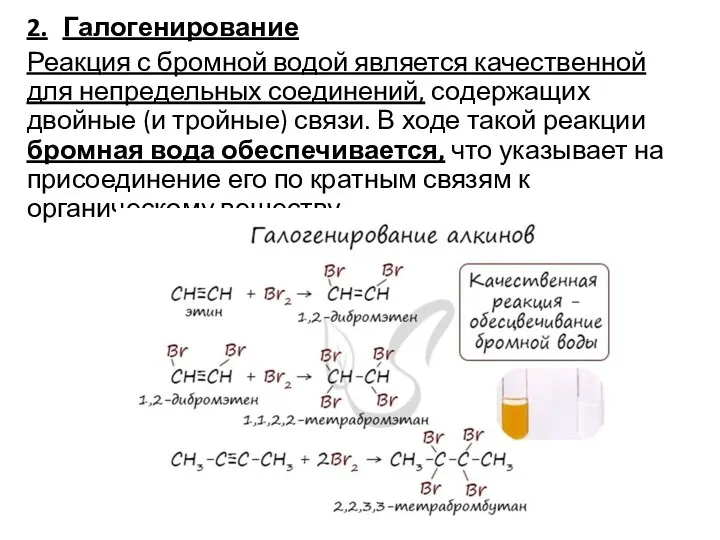
тройные) связи. В ходе такой реакции бромная вода обеспечивается, что указывает на присоединение его по кратным связям к органическому веществу.
Слайд 83. Гидрогалогенирование
Алкины вступают в реакции гидрогалогенирования, протекающие по типу присоединения.
Гидрогалогенирование протекает по правилу
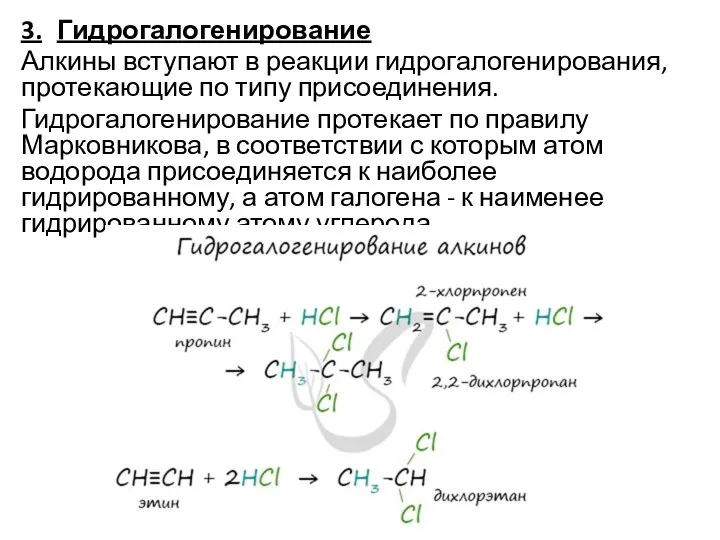
Марковникова, в соответствии с которым атом водорода присоединяется к наиболее гидрированному, а атом галогена - к наименее гидрированному атому углерода.
Слайд 94. Реакция Кучерова
Реакцией Кучерова называют гидратацию ацетиленовых соединений с образованием карбонильных соединений. Открыта
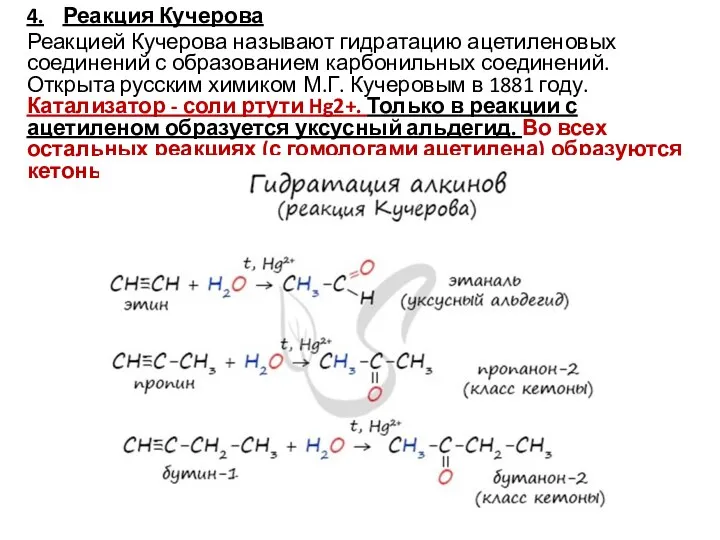
русским химиком М.Г. Кучеровым в 1881 году. Катализатор - соли ртути Hg2+. Только в реакции с ацетиленом образуется уксусный альдегид. Во всех остальных реакциях (с гомологами ацетилена) образуются кетоны.
Слайд 105. Окисление
При горении алкины, как и все органические соединения, сгорают с образование углекислого

газа и воды - полное окисление.
2CH≡CH + 5O2 → 4CO2 + 2H2O
Сильные окислители (особенно в подкисленной среде) способны разрывать молекулы алкинов в самом слабом месте - в месте тройной связи.
Так, при окислении пропина, образуется уксусная кислота и муравьиная кислота, окисляющаяся до угольной кислоты, которая распадается на углекислый газ и воду.
Слайд 116. Реакция Н.Д. Зелинского (тримеризация ацетилена)
Данная реакция протекает при пропускании ацетилена над активированным
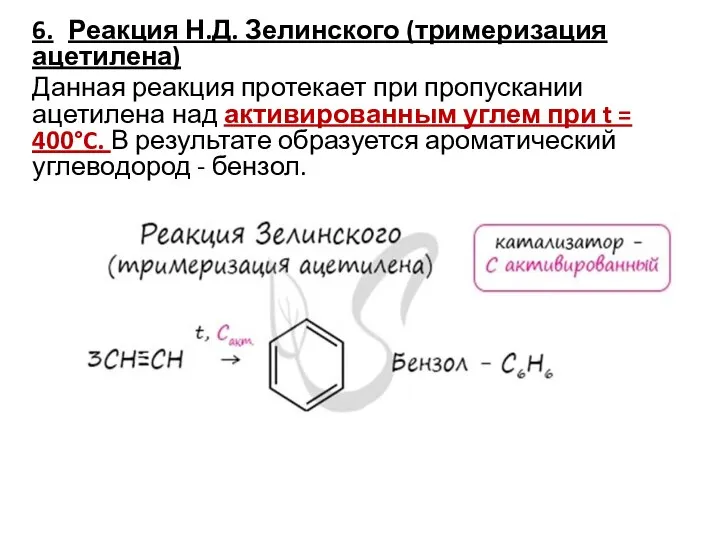
углем при t = 400°C. В результате образуется ароматический углеводород - бензол.
Слайд 127. Димеризация ацетилена
Димеризация ацетилена происходит при наличии катализатора - солей меди I. В
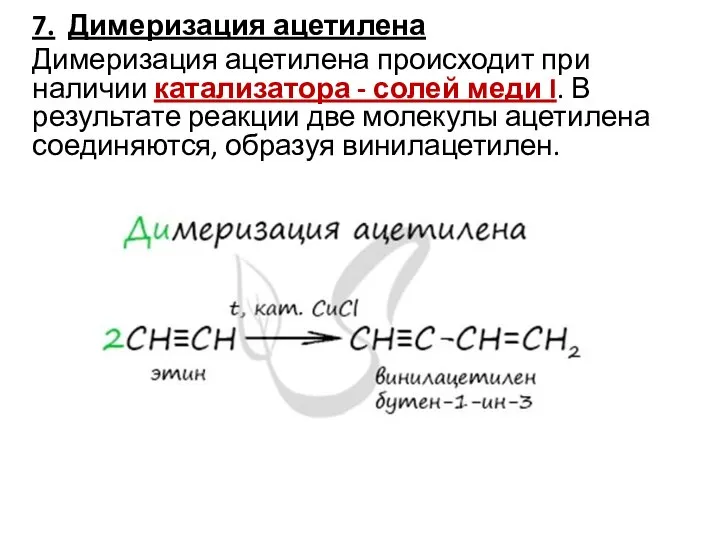
результате реакции две молекулы ацетилена соединяются, образуя винилацетилен.











 Рівняння характеристики крупності
Рівняння характеристики крупності Химическая связь
Химическая связь Красители для волос. Первая группа
Красители для волос. Первая группа Комплексонометрическое титрование. 5 лекция. Часть 2
Комплексонометрическое титрование. 5 лекция. Часть 2 Металлы
Металлы Кислоты
Кислоты Карбоксилденген этоксилаттар
Карбоксилденген этоксилаттар Сухой лёд
Сухой лёд Органические реагенты
Органические реагенты Относительная молекулярная масса вещества
Относительная молекулярная масса вещества Судың диссоциациясы
Судың диссоциациясы Презентация на тему Биополимеры
Презентация на тему Биополимеры  Презентация на тему Классификация химических реакций 11 класс
Презентация на тему Классификация химических реакций 11 класс  Бытовая химия
Бытовая химия Ферменттер.Ферменттердің құрылымы.Биохимиялық маңызы
Ферменттер.Ферменттердің құрылымы.Биохимиялық маңызы Резиновые материалы и клеи. Тема 7.5
Резиновые материалы и клеи. Тема 7.5 Пористые стекла
Пористые стекла Разбор контрольной работы. Химия (9 класс)
Разбор контрольной работы. Химия (9 класс) Идеальный газ
Идеальный газ Электролитическая диссоциация
Электролитическая диссоциация Повторение по теме: « Химическая связь. Строение вещества». Виды химических связей Типы кристаллических
Повторение по теме: « Химическая связь. Строение вещества». Виды химических связей Типы кристаллических Строение атома. Периодический закон
Строение атома. Периодический закон Соединения щелочноземельных металлов
Соединения щелочноземельных металлов Химические реакции. Классификация
Химические реакции. Классификация Материаловедение. Влияние нагрева на структуру деформированного металла. (Тема 5)
Материаловедение. Влияние нагрева на структуру деформированного металла. (Тема 5) Золото
Золото Пластмассы
Пластмассы Изучение основного солевого состава брендов бутилированной воды, присутствующих на рынке России
Изучение основного солевого состава брендов бутилированной воды, присутствующих на рынке России