Содержание
- 2. Щелочные металлы
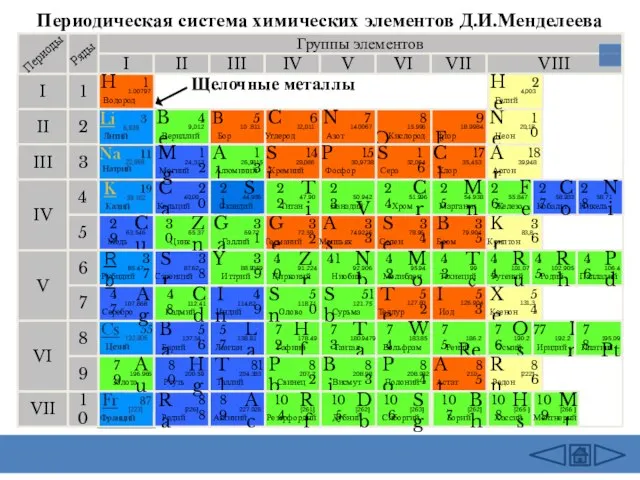
- 3. Периодическая система химических элементов Д.И.Менделеева Группы элементов I III II VIII IV V VI VII II
- 4. Группы элементов I III II VIII IV V VI VII II I III VII VI V
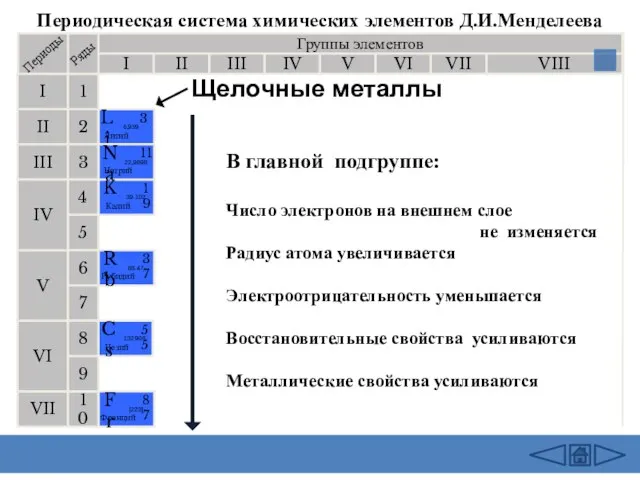
- 5. Периодическая система химических элементов Д.И.Менделеева Группы элементов I III II VIII IV V VI VII II
- 6. Периодическая система химических элементов Д.И.Менделеева Группы элементов I III II VIII IV V VI VII II
- 7. Периодическая система химических элементов Д.И.Менделеева Группы элементов I III II VIII IV V VI VII II
- 8. Периодическая система химических элементов Д.И.Менделеева Группы элементов I III II VIII IV V VI VII II
- 9. Периодическая система химических элементов Д.И.Менделеева Группы элементов I III II VIII IV V VI VII II
- 10. Периодическая система химических элементов Д.И.Менделеева Группы элементов I III II VIII IV V VI VII II
- 11. Щелочные металлы Литий Натрий Калий Рубидий Цезий Фрайций История открытия
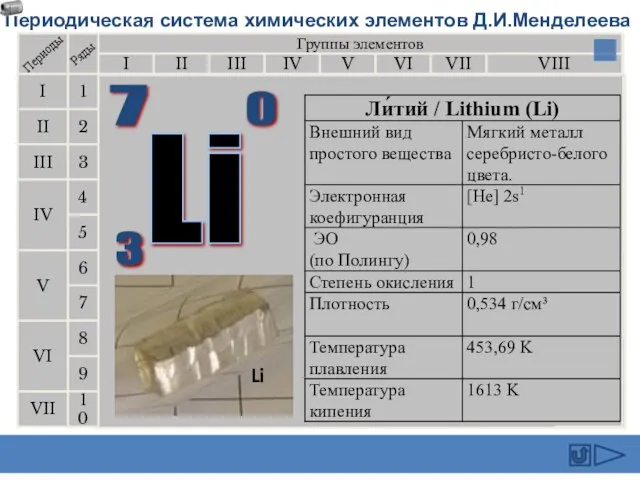
- 12. Литий был открыт в 1817 г. А. Арфведсоном в минерале петалите. Берцелиус предложил назвать ее литионом
- 13. Натрий (Natrium, от англ. и франц. Sodium, нем. Natrium от древнеевр. neter — бурлящее вещество. В
- 14. Калий (англ. Potassium, франц. Potassium, нем. Kalium) открыл в 1807 г. Г.Дэви, производивший электролиз твердого, слегка
- 15. При спектроскопическом анализе минерала лепидолит (фторсиликат лития и алюминия) и обнаружились две новые красные линии в
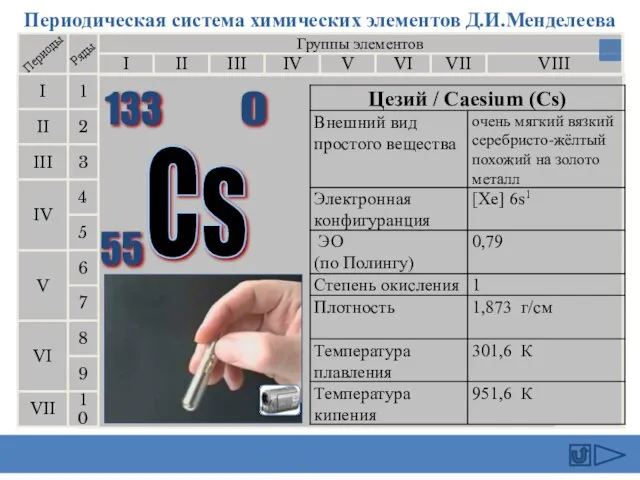
- 16. Цезий (англ. Cesium, франц. Cesium, нем. Caesium) - первый элемент, открытый с помощью спектрального анализа. Р.Бунзен
- 17. Этот элемент был предсказан Д.И.Менделеевым (как Эка-цезий), и был открыт (по его радиоактивности) в 1939 г.
- 18. Природные соединения лития Сподуменн
- 19. Природные соединения натрия Галит
- 20. Природные соединения калия Сильвин
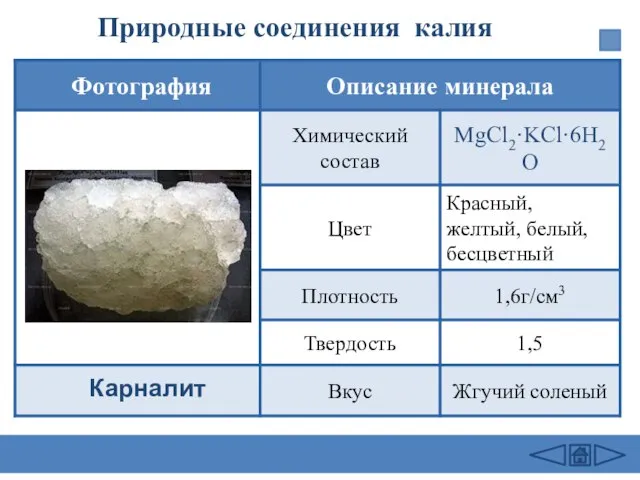
- 21. Природные соединения калия Карналит
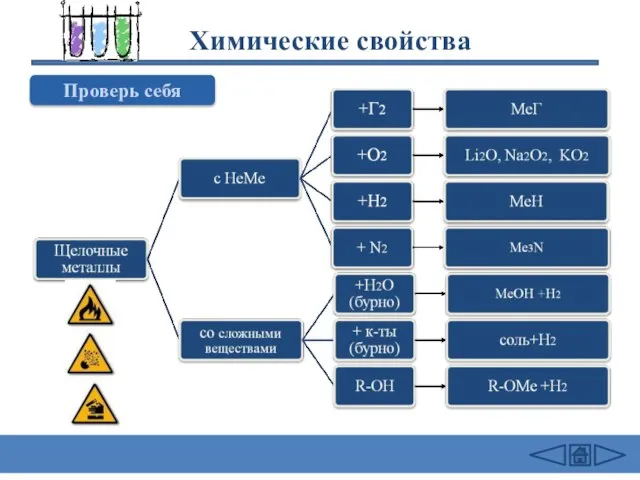
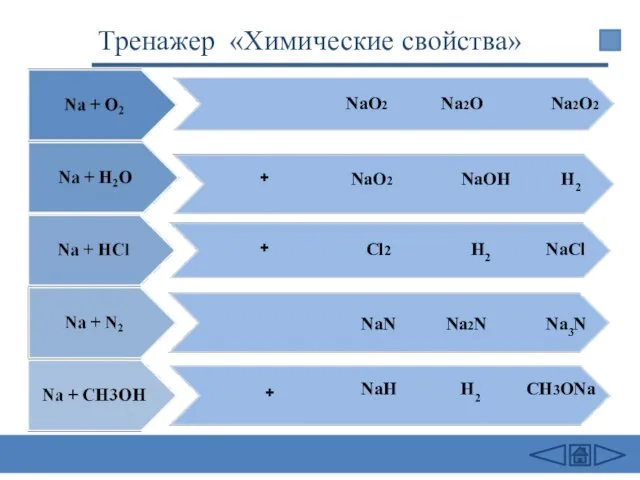
- 22. Химические свойства Проверь себя
- 23. Химические свойства 2Na + Cl2 = 2NaCl (в атмосфере F2 и Cl2 щелочные Me самовоспламеняются) 4Li
- 24. Качественное определение щелочных металлов Li+ Na+ K+ Для распознавания соединений щелочных металлов по окраске пламени исследуемое
- 25. 1) Электролиз расплавов соединений щелочных металлов: 2МеCl = 2Ме + Cl2 4МеOH = 4Ме + 2Н2О
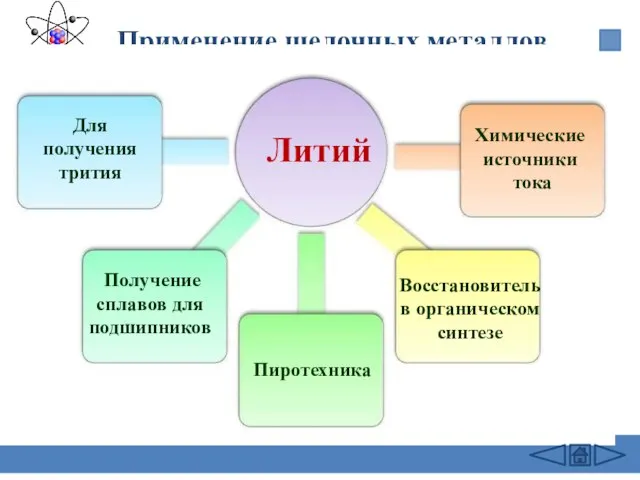
- 26. Применение щелочных металлов Литий Для получения трития Получение сплавов для подшипников Восстановитель в органическом синтезе Химические
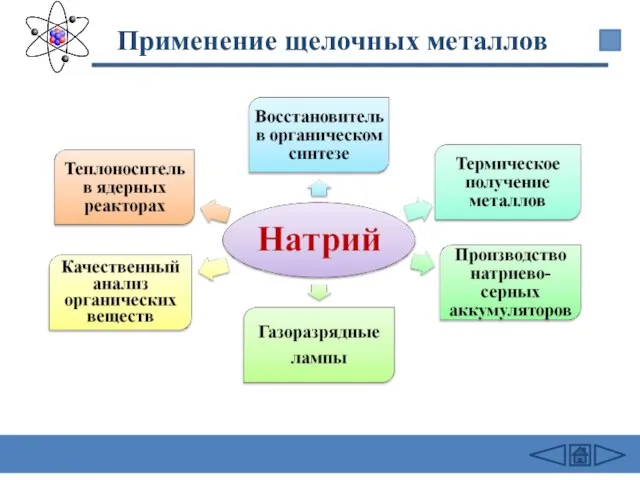
- 27. Применение щелочных металлов
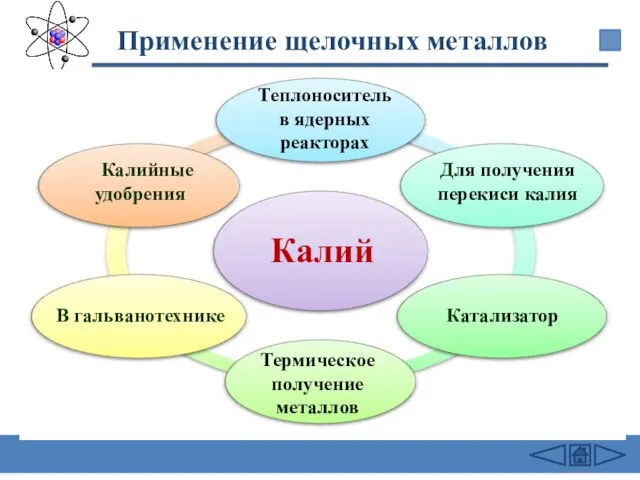
- 28. Применение щелочных металлов Калий В гальванотехнике Калийные удобрения Для получения перекиси калия Катализатор Термическое получение металлов
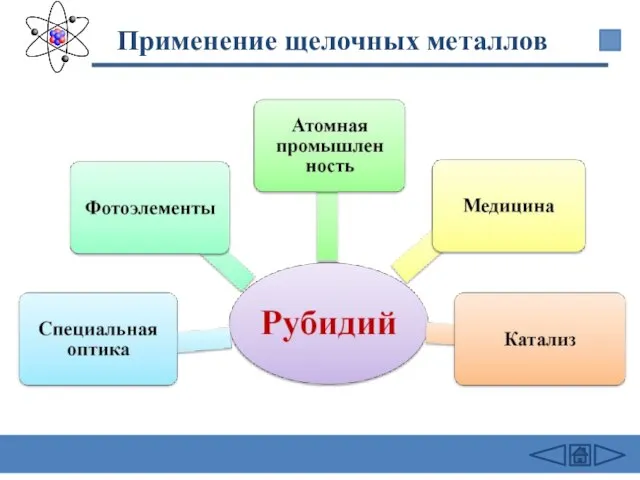
- 29. Применение щелочных металлов
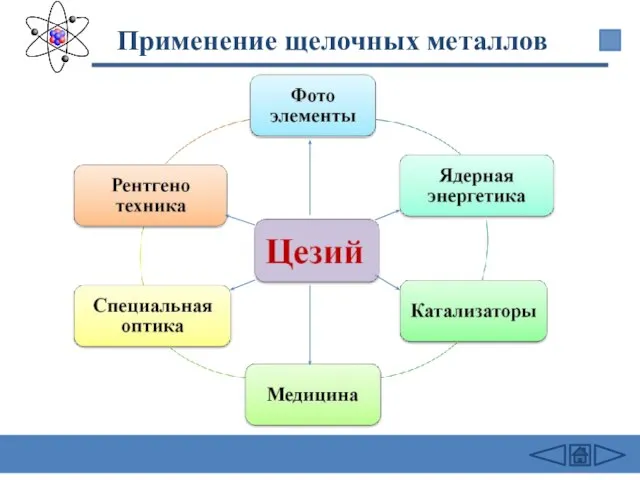
- 30. Применение щелочных металлов
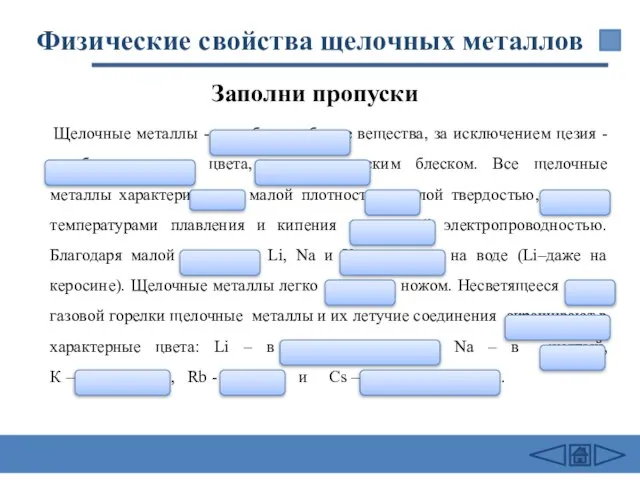
- 31. Физические свойства щелочных металлов Щелочные металлы - серебристо–белые вещества, за исключением цезия - серебристо-желтого цвета, с
- 32. 1. Предложил назвать калий от арабского «алкали» - щелочь И. Арфведсон Г.Деви Й. Берцеллиус 2. В
- 33. + + + NаО2 Nа2O2 NаОН NaCl Na2N Na3N NаО2 Cl2 NaN NaH Na2O H2 H2
- 34. Габриелян О.С. Химия. 9 класс: Учеб. для общеобразоват.учебн. заведений.-М.: Дрофа, Ахметов Н. С. Общая и неорганическая
- 36. Скачать презентацию



















 Тренажёр: знаки химических элементов
Тренажёр: знаки химических элементов Алкены. Физические и химические свойства
Алкены. Физические и химические свойства Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Химически опасные объекты Аварии, связанные с выбросом АХОВ
Химически опасные объекты Аварии, связанные с выбросом АХОВ Материаловедение
Материаловедение Синтетические волокна
Синтетические волокна Презентация на тему Неметаллы, особенности строения
Презентация на тему Неметаллы, особенности строения  Электролиз (катод)
Электролиз (катод) Основные принципы работы химических сенсоров
Основные принципы работы химических сенсоров Химическая картина мира
Химическая картина мира Основания: определение, классификация, химические свойства
Основания: определение, классификация, химические свойства Металлы. Общая характеристика, химические свойства. Получение
Металлы. Общая характеристика, химические свойства. Получение Вебинар. Гидролиз солей
Вебинар. Гидролиз солей Свойства радиоактивных элементов
Свойства радиоактивных элементов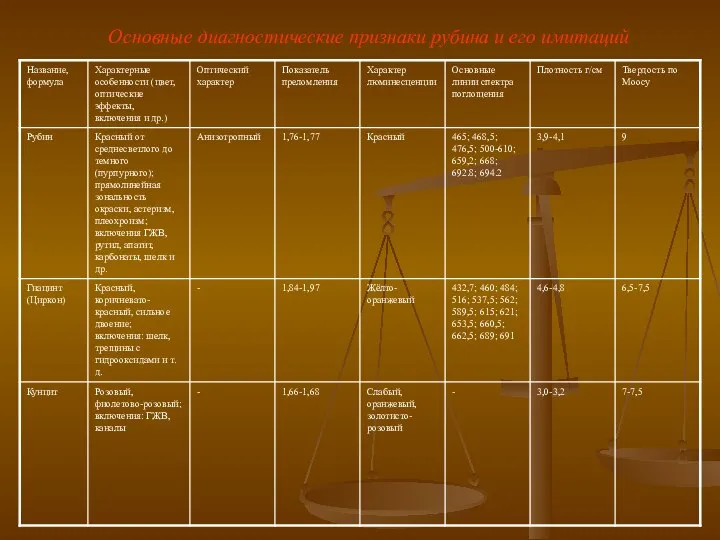 Основные диагностические признаки рубина и его имитаций
Основные диагностические признаки рубина и его имитаций Генетические ряды неорганических соединений
Генетические ряды неорганических соединений Двойные латуни. Диаграмма состояния. Примеси. Структура и свойства
Двойные латуни. Диаграмма состояния. Примеси. Структура и свойства Вуглеводи. Визначення вуглеводів
Вуглеводи. Визначення вуглеводів Галогены. Обобщение знаний
Галогены. Обобщение знаний Подготовка к ГИА по химии
Подготовка к ГИА по химии Предпосылки открытия Периодического закона Д. И. Менделеевым
Предпосылки открытия Периодического закона Д. И. Менделеевым ОВ. Структура и принцип работы параметры ОВ
ОВ. Структура и принцип работы параметры ОВ Абсолютное первенство по химии - 2012
Абсолютное первенство по химии - 2012 строение атома углерода. Валентные состояния атома углерода
строение атома углерода. Валентные состояния атома углерода Общая характеристика элементов IIА группы
Общая характеристика элементов IIА группы Вода… Химические названия
Вода… Химические названия Водород – первый элемент в периодической таблице
Водород – первый элемент в периодической таблице Кристаллы, выращенные учащимися
Кристаллы, выращенные учащимися