Содержание
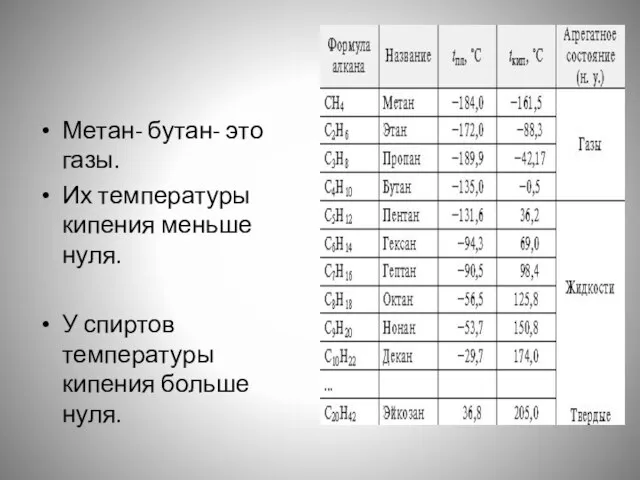
- 2. Физические свойства спиртов Почему в ряду спиртов отсутствуют газы?
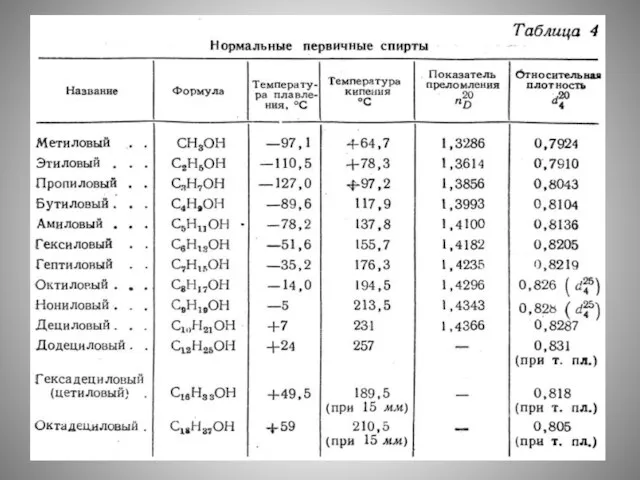
- 3. Физические свойства спиртов Метанол, этанол и пропанол смешиваются с водой во всех соотношениях. С ростом молекулярной
- 4. Физические свойства спиртов Растворимость спиртов с разветвленной структурой выше, чем у спиртов с имеющих неразветвленное, нормальное
- 5. Если смешать, например, 5 мл воды и 5 мл спирта, то суммарный объем будет меньше 10
- 6. Физические свойства спиртов Добыли как-то комсомольцы 200 литровую бочку спирта. И решили отпраздновать это дело. Нашли
- 7. Физические свойства спиртов Местные - куда им деваться? Разбавили. Комсомольцы прибыли и видят, что получилось не
- 8. На все эти «почему» отвечает водородная связь.
- 9. Химическую связь между атомами водорода одной молекулы (или её части) и атомами наиболее электоротрицательных элементов (фтор,
- 10. Метан- бутан- это газы. Их температуры кипения меньше нуля. У спиртов температуры кипения больше нуля.
- 11. Спирты обладают аномально высокими температурами кипения по сравнению со многими классами органических соединений и чем можно
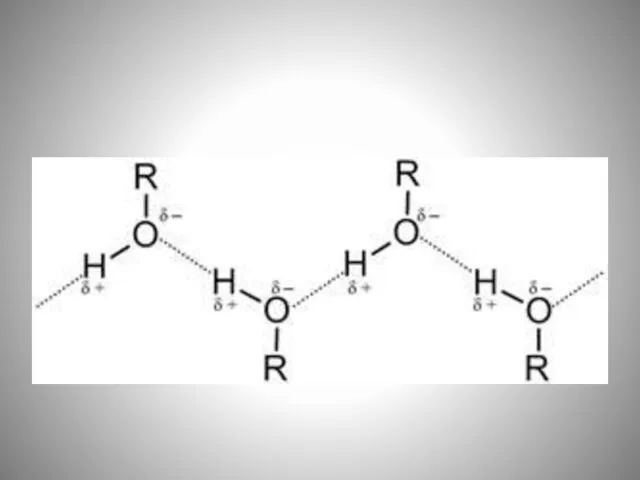
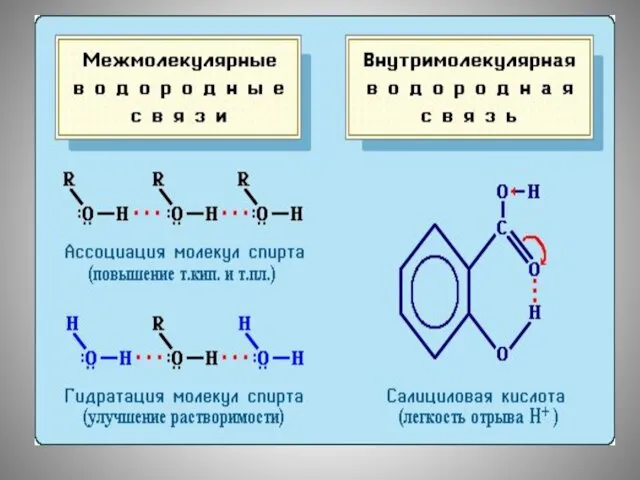
- 13. Это объясняется тем, что между молекулами спиртов возникают водородные связи, благодоря которым образуются межмолекулярные ассоциаты. Водородные
- 15. молекулы спирта как и воды, являются ассоциированными жидкостями за счет водородных связей, возникающих между молекулами: .
- 16. На разрыв любой связи необходимо затратить энергию. Раз энергия затрачивается- температура кипения больше нуля. А раз
- 19. Между атомом водорода одной молекулы и атомом кислорода другой (воды и спирта) устанавливается водородная связь:
- 20. В любом спирте есть нерастворимая часть – радикал, который удерживается в воде благодаря наличию водородных связей.
- 21. Что же происходит при смешивании спирта с водой?
- 22. Этому есть два объяснения: 1. Молекулы спирта притягиваются к молекулам воды сильнее, чем молекулы воды между
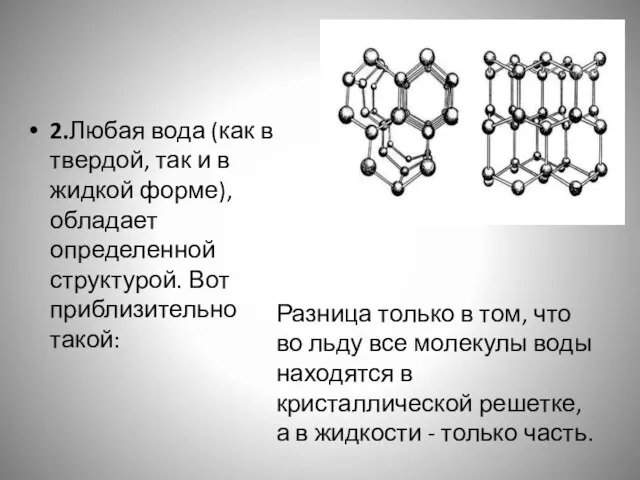
- 23. 2.Любая вода (как в твердой, так и в жидкой форме), обладает определенной структурой. Вот приблизительно такой:
- 24. Размер полости в кристаллической решетке воды как раз таков, что туда помещается молекула спирта. За счет
- 25. В результате получается химическое соединение — гидрат спирта, молекула которого занимает объем меньший, нежели молекула спирта
- 26. И если брать в качестве примера смесь 50 мл воды и 50 мл спирта, то 4
- 27. Запах. Низшие спирты обладают характерным алкогольным запахом, запах средних гомологов сильный и часто неприятный. Высшие спирты
- 28. Все спирты легче воды (плотность ниже единицы). Низшие спирты легче воспламеняются и горят бесцветным пламенем. Спирты
- 30. Скачать презентацию






















 Общая характеристика неметаллов
Общая характеристика неметаллов Изомерия. Классификация органических веществ.
Изомерия. Классификация органических веществ. Химия спирты одноатомные предельные
Химия спирты одноатомные предельные Композитные материалы
Композитные материалы Демокрит его вклад в развитие взглядов на строение вещества
Демокрит его вклад в развитие взглядов на строение вещества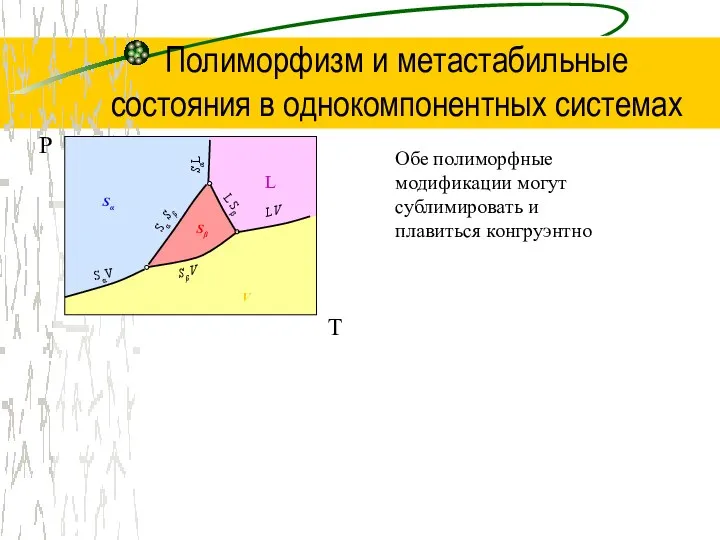 Полиморфизм и метастабильные состояния в однокомпонентных системах
Полиморфизм и метастабильные состояния в однокомпонентных системах Основи масообміну
Основи масообміну Количество вещества. Моль
Количество вещества. Моль Алюміній. Фізичні та хімічні властивості
Алюміній. Фізичні та хімічні властивості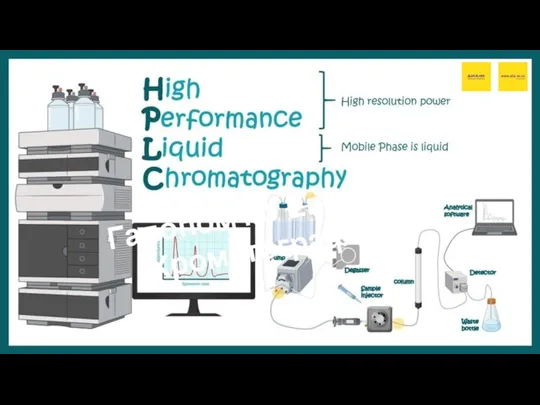 Хроматография
Хроматография Углеродистые конструкционные стали
Углеродистые конструкционные стали Жидкокристаллический эластомер как роторный актуатор
Жидкокристаллический эластомер как роторный актуатор Презентация на тему Игра по химии «Остров Периодическая Система»
Презентация на тему Игра по химии «Остров Периодическая Система»  Свойства растворов электролитов
Свойства растворов электролитов Производство аммиака
Производство аммиака Кислород. Общая характеристика, получение и свойства
Кислород. Общая характеристика, получение и свойства Презентация на тему Металлы
Презентация на тему Металлы  Количество вещества, число Авогадро, молярная масса, молярный объём, уравнение связи
Количество вещества, число Авогадро, молярная масса, молярный объём, уравнение связи Алкены
Алкены Презентация на тему Электронное и пространственное строение молекулы метана
Презентация на тему Электронное и пространственное строение молекулы метана  Циклоалканы. Физические свойства
Циклоалканы. Физические свойства Кислород
Кислород Синтетические органические соединения
Синтетические органические соединения Турнир Деда Мороза. Викторина по химии
Турнир Деда Мороза. Викторина по химии Презентация на тему Алмазы Индии
Презентация на тему Алмазы Индии  Алкены
Алкены Значимые личности в химии
Значимые личности в химии Стан електронів у атомі
Стан електронів у атомі