Содержание
- 2. Движущая сила реакции – это возможность образования новой более стабильной системы, обладающей минимальной потенциальной энергией. Факторы,
- 3. Химическая реакция характеризуется 2 факторами: Термодинамическим - изменением свободной энергии; Кинетическим – скоростью превращения и его
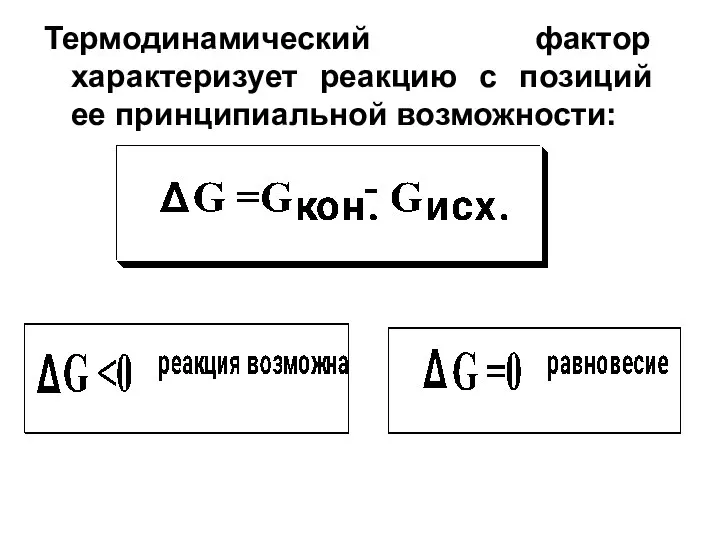
- 4. Термодинамический фактор характеризует реакцию с позиций ее принципиальной возможности:
- 5. В соответствии с уравнением Гиббса: ∆Н – изменение энтальпии (разность энергий разрывающихся и вновь образующихся связей);
- 6. Реакционная способность вещества – способность вещества вступать в ту или иную реакцию и реагировать с большей
- 7. Теория переходного состояния При переходе от исх. в-в к продуктам реагирующая система должна пройти через некоторое
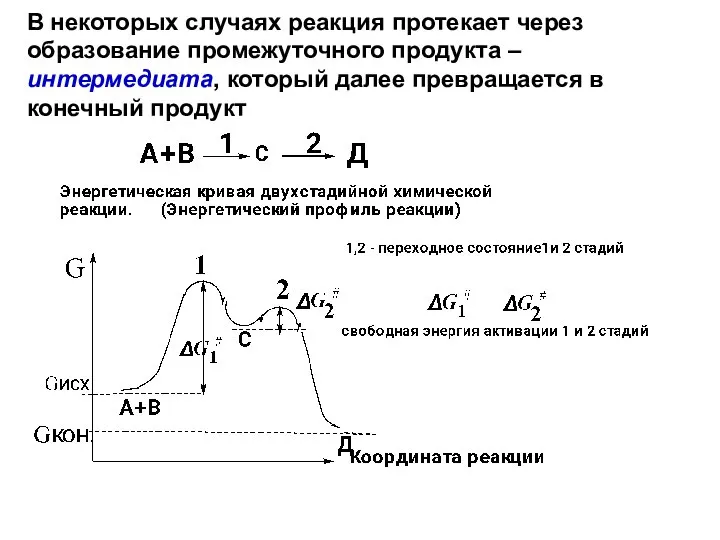
- 8. В некоторых случаях реакция протекает через образование промежуточного продукта – интермедиата, который далее превращается в конечный
- 9. Первая стадия будет лимитирующей, так как: Скорость химических реакций определяется относительной стабильностью интермедиатов, образующихся в лимитирующей
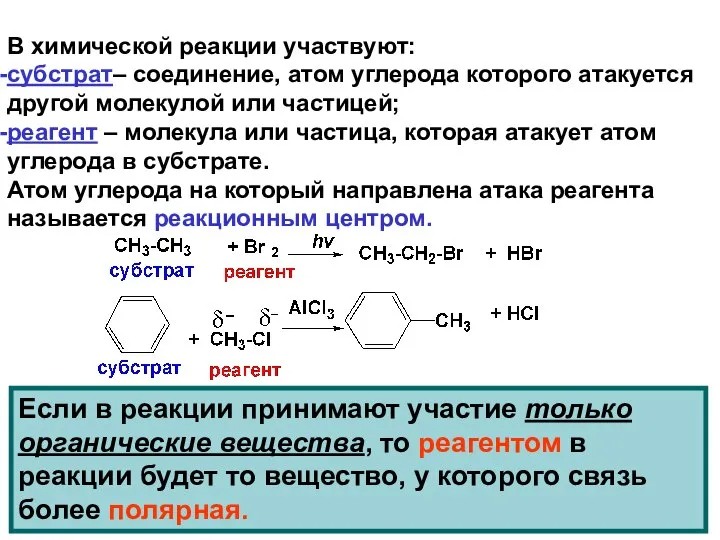
- 10. В химической реакции участвуют: субстрат– соединение, атом углерода которого атакуется другой молекулой или частицей; реагент –
- 11. Типы реагентов Радикальные – свободные атомы или частицы с неспаренным электроном (R) Электрофильные – частицы, которые
- 12. Радикалы (R) Атомы или частицы со свободными электронами: 1. Атомы: F ∙ , Cl ∙, Br
- 13. Электрофилы Е⊕ Атомы с вакантной орбиталью или частицы их содержащие: 1. Катионы: Cl⊕ , Br⊕ ,
- 14. Электрофилы можно классифицировать в зависимости от типа электрофильного атома
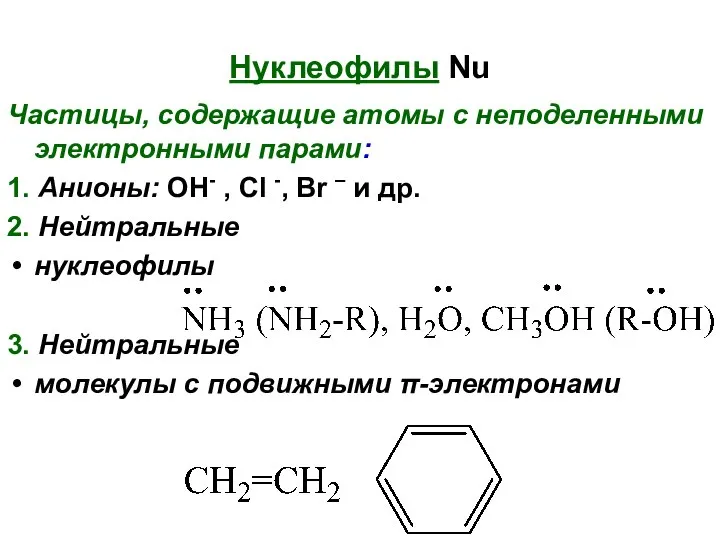
- 15. Нуклеофилы Nu Частицы, содержащие атомы с неподеленными электронными парами: 1. Анионы: OH- , Cl -, Br
- 16. Нуклеофилы можно классифицировать в зависимости от типа нуклеофильного атома
- 17. Классификация органических реакций А). По способу разрыва и образования ковалентной связи в субстрате: а) радикальные: гомолитический
- 18. б) ионные: гетеролитический разрыв связей (гетеролиз)- электронная пара связи переходит на АО только одного атома (образуются
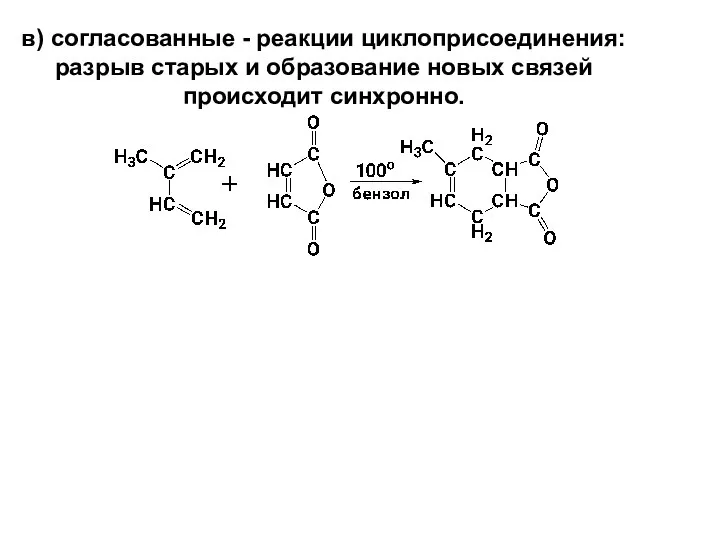
- 19. в) согласованные - реакции циклоприсоединения: разрыв старых и образование новых связей происходит синхронно.
- 20. Б. По направлению реакции, т.е. по результату конечного химического превращения: 1). Замещения (S) – происходит замещение
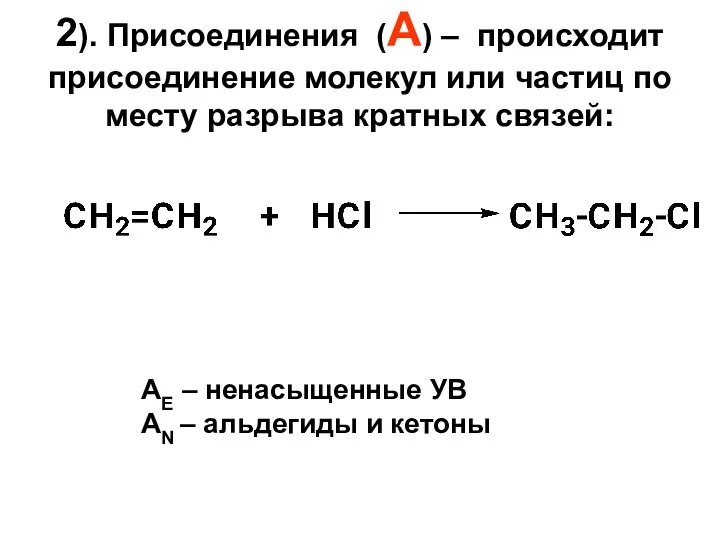
- 21. 2). Присоединения (А) – происходит присоединение молекул или частиц по месту разрыва кратных связей: АЕ –
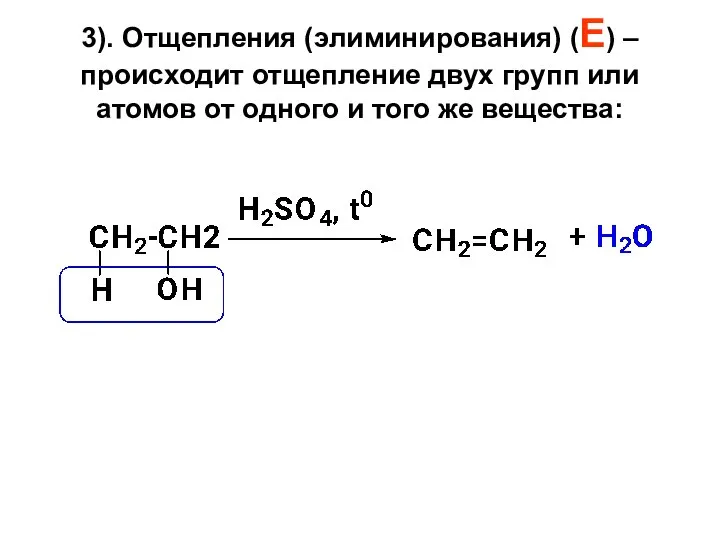
- 22. 3). Отщепления (элиминирования) (Е) – происходит отщепление двух групп или атомов от одного и того же
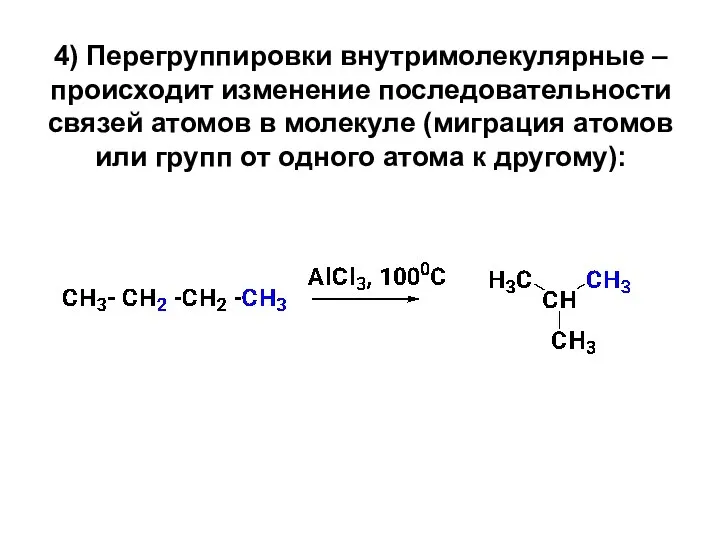
- 23. 4) Перегруппировки внутримолекулярные – происходит изменение последовательности связей атомов в молекуле (миграция атомов или групп от
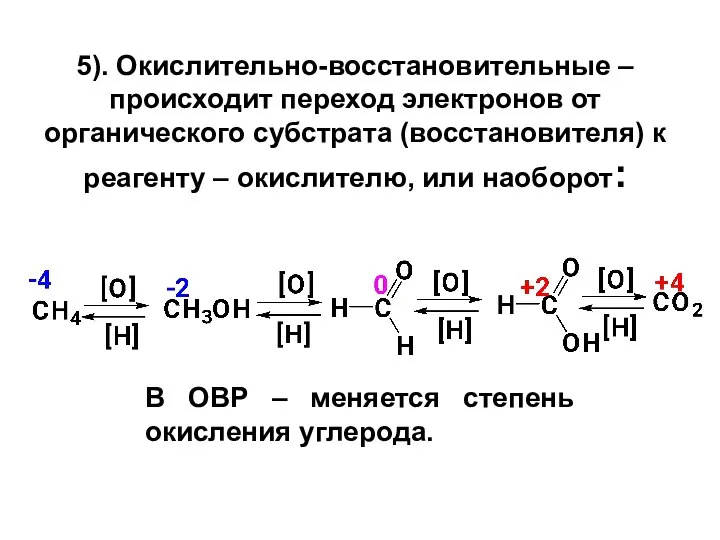
- 24. 5). Окислительно-восстановительные – происходит переход электронов от органического субстрата (восстановителя) к реагенту – окислителю, или наоборот:
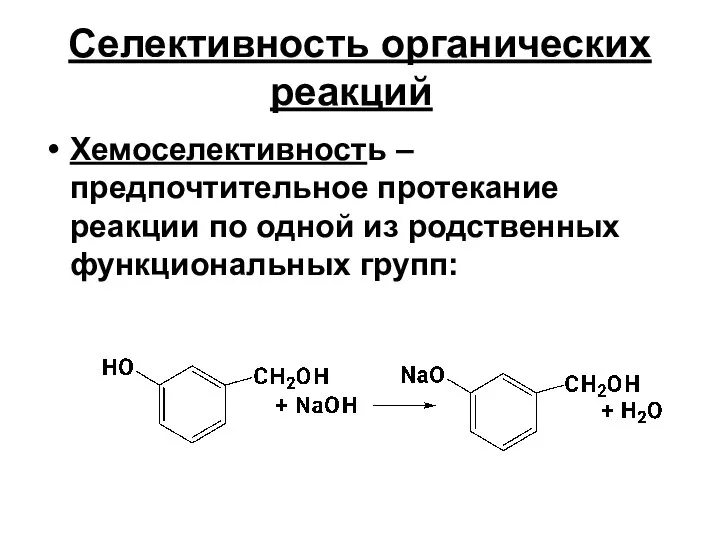
- 25. Селективность органических реакций Хемоселективность – предпочтительное протекание реакции по одной из родственных функциональных групп:
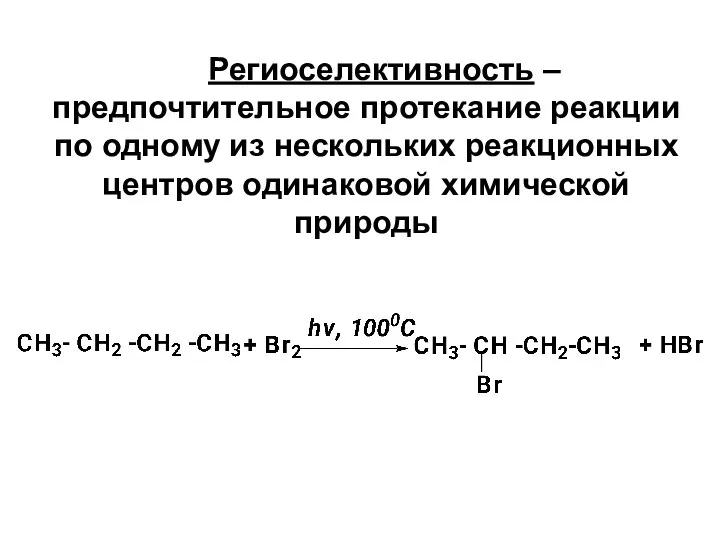
- 26. Региоселективность – предпочтительное протекание реакции по одному из нескольких реакционных центров одинаковой химической природы
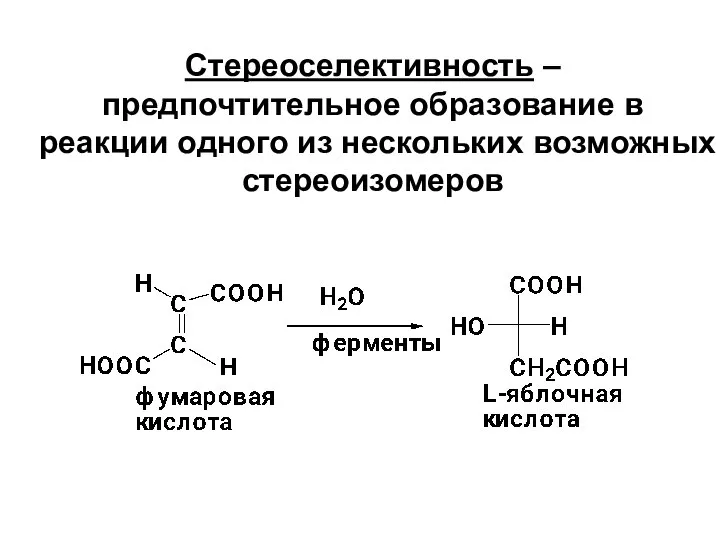
- 27. Стереоселективность – предпочтительное образование в реакции одного из нескольких возможных стереоизомеров
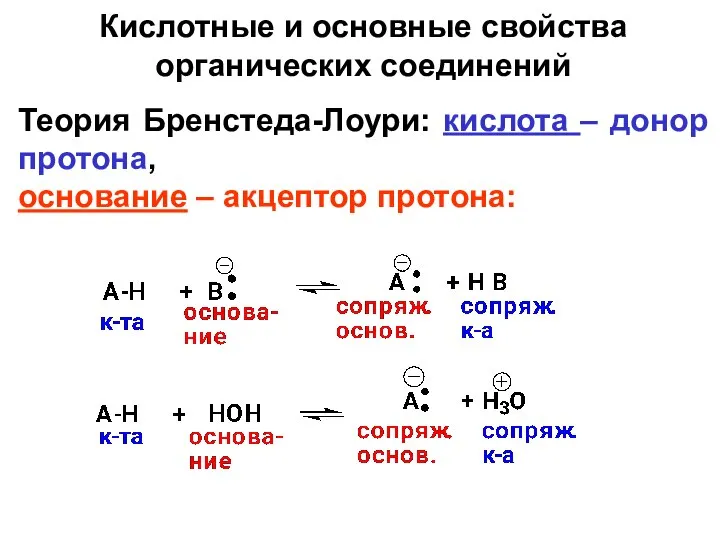
- 28. Кислотные и основные свойства органических соединений Теория Бренстеда-Лоури: кислота – донор протона, основание – акцептор протона:
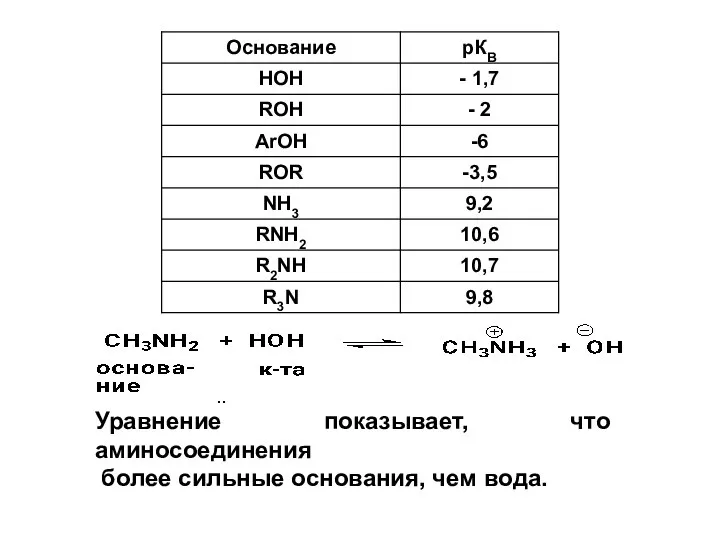
- 29. Ка –характеризует силу кислоты. Показатель кислотности рКа = – lg Ka. Чем меньше показатель кислотности, тем
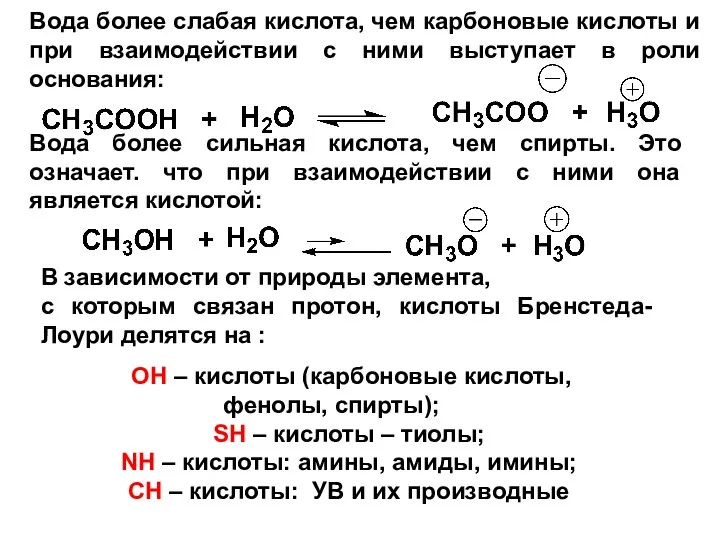
- 30. Вода более сильная кислота, чем спирты. Это означает. что при взаимодействии с ними она является кислотой:
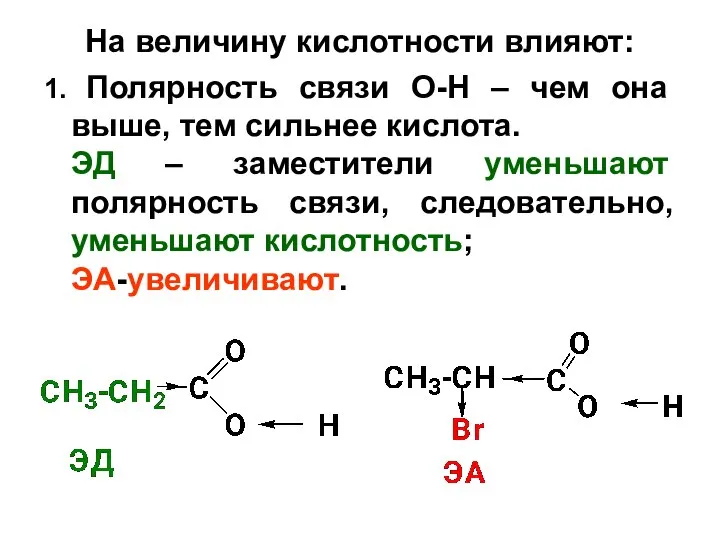
- 31. На величину кислотности влияют: 1. Полярность связи О-Н – чем она выше, тем сильнее кислота. ЭД
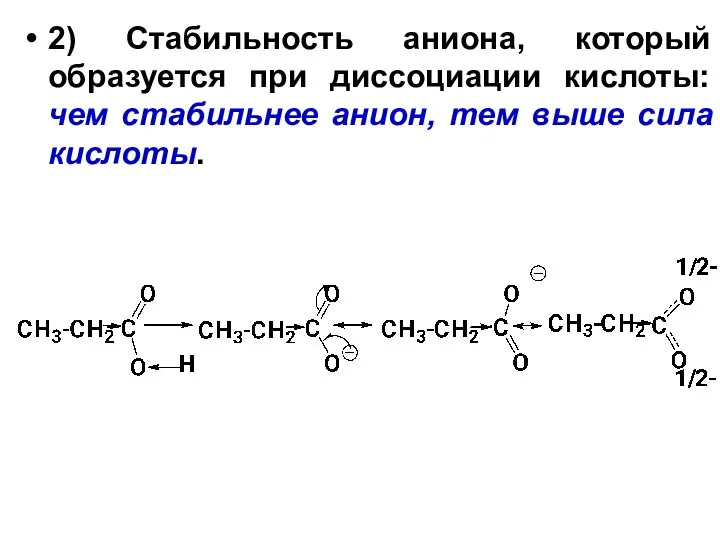
- 32. 2) Стабильность аниона, который образуется при диссоциации кислоты: чем стабильнее анион, тем выше сила кислоты.
- 33. 4) Влияние растворителя: сольватированный растворителем анион будет более стабильным, следовательно сила кислоты будет выше. 3) Тип
- 34. Основания Бренстеда-Лоури: n– основания, которые содержат неподеленную пару электронов: π– основания: алкены, алкины, алкадиены, арены. Для
- 35. Уравнение показывает, что аминосоединения более сильные основания, чем вода.
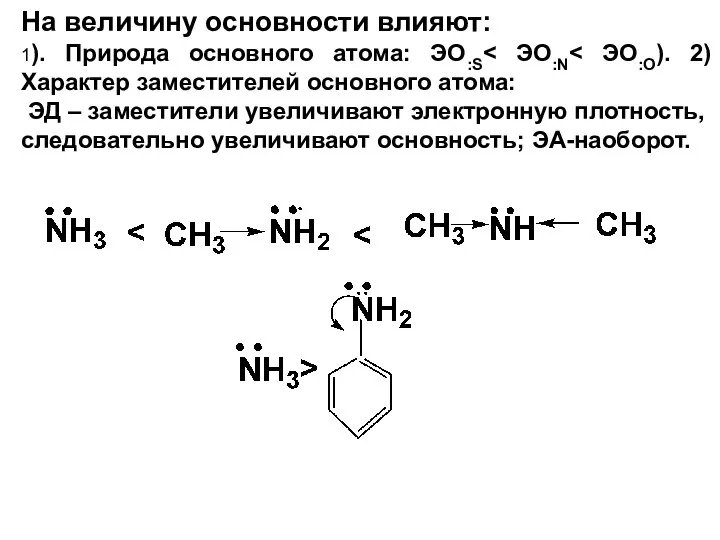
- 36. На величину основности влияют: 1). Природа основного атома: ЭО:S ЭД – заместители увеличивают электронную плотность, следовательно
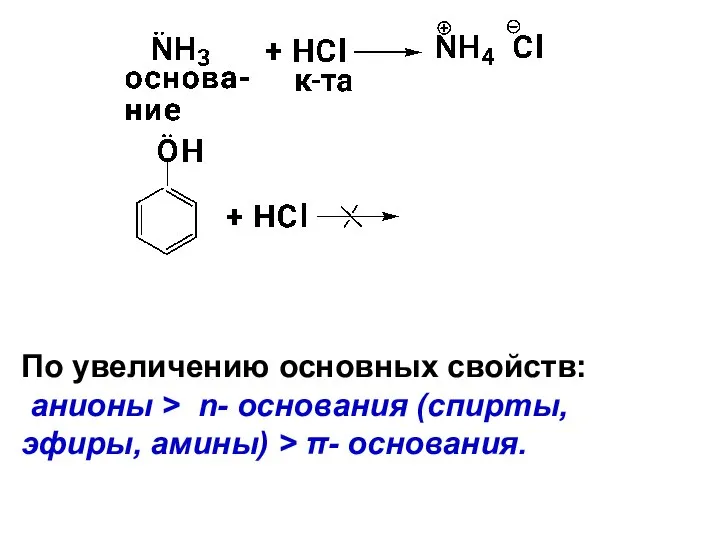
- 37. По увеличению основных свойств: анионы > n- основания (спирты, эфиры, амины) > π- основания.
- 39. Скачать презентацию

















 Ситалл – искусственный поликристаллический материал
Ситалл – искусственный поликристаллический материал Использование катионных красителей в экстракционно-флуориметрическом анализе
Использование катионных красителей в экстракционно-флуориметрическом анализе Аналитическая химия. Гомогенные растворы
Аналитическая химия. Гомогенные растворы Галогены. Положение галогенов в ПСХЭ
Галогены. Положение галогенов в ПСХЭ Арены. Химические свойства
Арены. Химические свойства Индикаторная бумага
Индикаторная бумага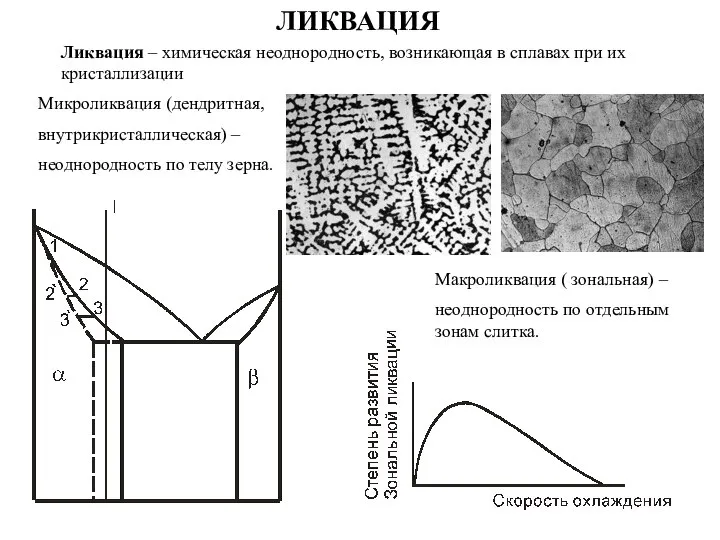 Ликвация. Микроликвация
Ликвация. Микроликвация Получение и примененипе радиоактивные изотопы
Получение и примененипе радиоактивные изотопы Химия и сельское хозяйство
Химия и сельское хозяйство Исследование влияния изменения технических параметров на производительность установки замедленного коксования
Исследование влияния изменения технических параметров на производительность установки замедленного коксования Непредельные углеводороды
Непредельные углеводороды Пластмассы
Пластмассы Тайна алмазов
Тайна алмазов Красители для волос. Первая группа
Красители для волос. Первая группа ОГЭ №1, вопрос 1-16
ОГЭ №1, вопрос 1-16 Интегративный подход к обучению на уроках химии
Интегративный подход к обучению на уроках химии Обобщение знаний об основных классах неорганических соединений
Обобщение знаний об основных классах неорганических соединений Презентация на тему Металлическая связь
Презентация на тему Металлическая связь  металлы
металлы Распределение электронов в атоме по энергетическим уровням
Распределение электронов в атоме по энергетическим уровням Строение атома. Распределение электронов
Строение атома. Распределение электронов Презентация на тему Алюминий(Al)
Презентация на тему Алюминий(Al)  Наркотики и прекурсоры
Наркотики и прекурсоры Получение галогеноалканов
Получение галогеноалканов Презентация на тему Гидролиз
Презентация на тему Гидролиз  Склероглюкан
Склероглюкан Курсовая работа: синтез 3,5-диметилпиразола
Курсовая работа: синтез 3,5-диметилпиразола Кремнийорганические каучуки
Кремнийорганические каучуки