Слайд 21. Реакции замещения.
а) Галогенирование
CH4 + Cl2 hν → CH3Cl + HCl (1 стадия)
метан хлорметан CH3Cl + Cl2 hν → CH2Cl2 + HCl (2 стадия)
дихлорметан
СH2Cl2 + Cl2 hν → CHCl3 + HCl (3 стадия);
трихлорметан
CHCl3 + Cl2 hν → CCl4 + HCl (4

стадия).
тетрахлорметан
Слайд 3CH3 – CH2 – Cl + Cl2 hν → CH3 – CHCl2 + HCl
В реакциях замещения алканов легче всего

замещаются атомы водорода у третичных атомов углерода, затем у вторичных и, в последнюю очередь, у первичных. Для хлорирования эта закономерность не соблюдается при T>400˚C.
Слайд 5б) горения
CnH2n+2 + O2 t°С → nCO2 + (n+1)H2O
Помните! Смесь метана с воздухом и кислородом взрывоопасна
V(CH4) : V(O2) = 1:

2
V(CH4) : V(воздуха) = 1 : 10
Слайд 62. Реакции отщепления (дегидрирование)
а) CnH2n+2 t˚С, Ni или Pd → CnH2n + H2
б) При нагревании до 1500 С происходит образование ацетилена

и водорода:
2CH4 1500°С → C2H2 + 3H2
Слайд 73. Реакции перегруппировки (изомеризация)
н-алкан AlCl3, t°С → изоалкан



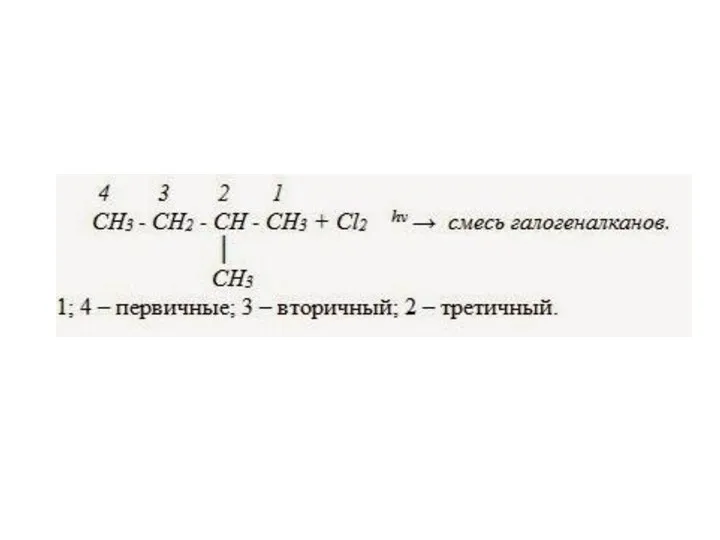



 Фуллерены (шары Бакминстера)
Фуллерены (шары Бакминстера) Алюминий и его органические производные
Алюминий и его органические производные Презентация на тему Кристаллические решетки 9 класс
Презентация на тему Кристаллические решетки 9 класс  Энергетический обмен
Энергетический обмен Ионная связь
Ионная связь Свойства солей, оксидов, оснований
Свойства солей, оксидов, оснований Генетические ряды Fe2+ и Fе3+. Качественные реакции на Fе2+ и Fе3+
Генетические ряды Fe2+ и Fе3+. Качественные реакции на Fе2+ и Fе3+ Презентация на тему Йод
Презентация на тему Йод  Роль Хеуорса, Фишера, Лемье в изучении структуры углеводов
Роль Хеуорса, Фишера, Лемье в изучении структуры углеводов Конструкционные и специальные материалы холодильной техники
Конструкционные и специальные материалы холодильной техники Перициклические реакции
Перициклические реакции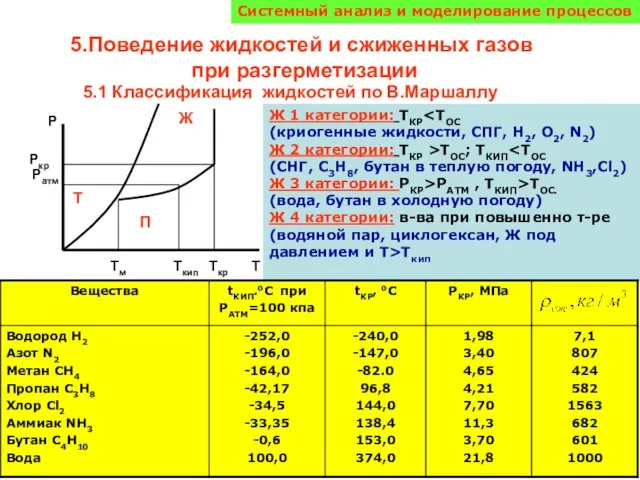 Поведение жидкостей и сжиженных газов при разгерметизации
Поведение жидкостей и сжиженных газов при разгерметизации Контроль качества лекарственных средств, производных карбоновых кислот и аминокислот
Контроль качества лекарственных средств, производных карбоновых кислот и аминокислот Получение армированных фотополимерных композиций
Получение армированных фотополимерных композиций Group 6 Cations
Group 6 Cations Русские ученые и топонимы в периодической системе химических элементов Д.И. Менделеева
Русские ученые и топонимы в периодической системе химических элементов Д.И. Менделеева Пищевые кислоты
Пищевые кислоты Предельные углеводороды. Алканы, насыщенные углеводороды, парафины, циклоалканы
Предельные углеводороды. Алканы, насыщенные углеводороды, парафины, циклоалканы Полиамиды (ПА)
Полиамиды (ПА) Окислители в пиросоставах
Окислители в пиросоставах Вебинар. Гидролиз солей
Вебинар. Гидролиз солей Совместимость материалов
Совместимость материалов Молярная масса вещества
Молярная масса вещества Композитные материалы
Композитные материалы Типы химической связи
Типы химической связи Презентация на тему Законы газового состояния вещества
Презентация на тему Законы газового состояния вещества  Development of the system of concepts on the topic redox reactions in the school course of inorganic chemistry
Development of the system of concepts on the topic redox reactions in the school course of inorganic chemistry Аммиак: состав, строение, свойства, применение
Аммиак: состав, строение, свойства, применение