Слайд 2Химическое равновесие
Реакции, которые одновременно протекают в прямом и обратном направлении, называются обратимыми
Состояние

химического обратимого процесса, при котором скорость прямой реакции равна скорости обратной реакции, называется химическим равновесием
Слайд 3Смещение химического равновесия осуществляется в соответствии с принципом Ле Шателье
Если на систему,

находящуюся в состоянии химического равновесия, оказать внешнее воздействие (изменить концентрацию, температуру, давление), то равновесие смещается в сторону той реакции, которая ослабляет это воздействие
Слайд 5Процессы, протекающие при обратимых реакциях

Слайд 6Процессы, протекающие при обратимых реакциях
прямая реакция
αА + βВ γС +

δD
обратная реакция
υ ═ k1 · [A]α · [B]β
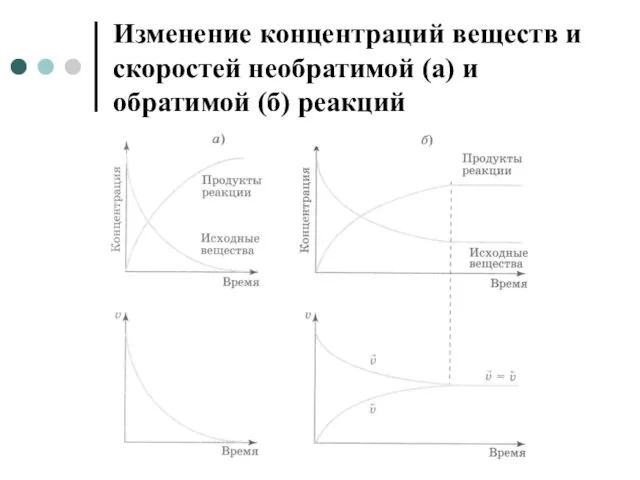
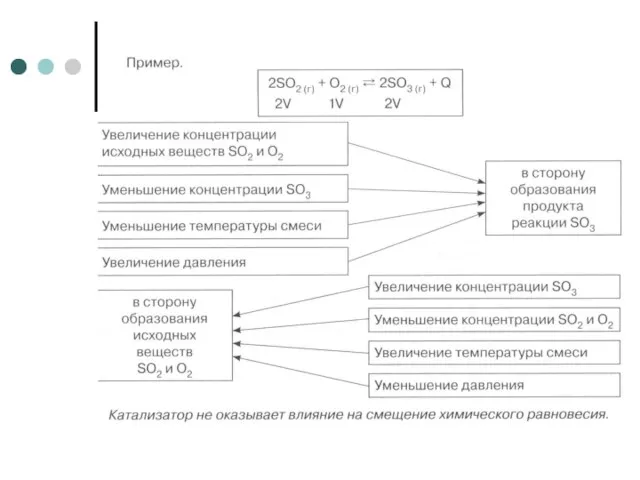
Слайд 7Изменение концентраций веществ и скоростей необратимой (а) и обратимой (б) реакций






 кулонометрия Дастан
кулонометрия Дастан Методы отбора проб воды. Оформление и подготовка к анализу, протокол исследования воды, определение рН
Методы отбора проб воды. Оформление и подготовка к анализу, протокол исследования воды, определение рН Кремнийорганическая гипотеза
Кремнийорганическая гипотеза Известняк. Разновидности известняка. Области применения
Известняк. Разновидности известняка. Области применения Строение атома
Строение атома Галогеноводородные кислоты
Галогеноводородные кислоты Сухой метод определения глюкозы. Глюкометры
Сухой метод определения глюкозы. Глюкометры Современные сплавы на основе циркония
Современные сплавы на основе циркония Комплексное задание по дисциплине основы материаловедения для группы 18
Комплексное задание по дисциплине основы материаловедения для группы 18 Соли
Соли Минералы и горные породы
Минералы и горные породы lektsia_6 (1)
lektsia_6 (1) Подготовка к контрольной работе химические реакции 8 класс
Подготовка к контрольной работе химические реакции 8 класс Азотосодержащие соединения: Амины. Аминокислоты. Белки
Азотосодержащие соединения: Амины. Аминокислоты. Белки Угольная кислота и её соли
Угольная кислота и её соли Комплексные соединения
Комплексные соединения Альдегиды, строение и свойства
Альдегиды, строение и свойства Презентация на тему Алкены. Строение. Изомерия. Химические свойства. Получение
Презентация на тему Алкены. Строение. Изомерия. Химические свойства. Получение  Распределение электронов в атомах
Распределение электронов в атомах Разработка системы подготовки лаборанта химического анализа
Разработка системы подготовки лаборанта химического анализа Пищевые добавки: вред и польза
Пищевые добавки: вред и польза Строение и функции нуклеиновых кислот. Лекция №3
Строение и функции нуклеиновых кислот. Лекция №3 Исследование биодеградации полимерных материалов методом АСМ
Исследование биодеградации полимерных материалов методом АСМ Коррозия металлов
Коррозия металлов Кислород. Физические и химические свойства. Получение
Кислород. Физические и химические свойства. Получение Классификация сложных неорганических веществ. Оксиды
Классификация сложных неорганических веществ. Оксиды Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини
Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини Стелс-материалы
Стелс-материалы