Содержание
- 2. Цели: 1. Образовательная: изучить понятие массовая доля атома химического элемента в соединении, закрепить знания об относительной
- 3. I.Актуализация знаний Повторение понятия относительная молекулярная масса вещества. Вычисление относительной молекулярной массы веществ.
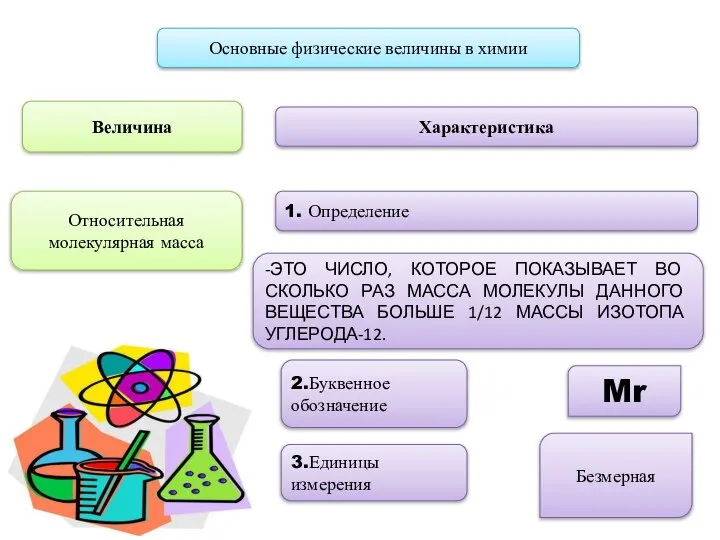
- 4. Основные физические величины в химии Величина 1. Определение Характеристика Относительная молекулярная масса -ЭТО ЧИСЛО, КОТОРОЕ ПОКАЗЫВАЕТ
- 5. Вычислить относительную молекулярную массу веществ Решение на доске Мr(Н2О)=Аr(Н)х2 Аr(О) =1х2+16 =18 Мr(СО2)= Аr(С)+ Аr(О) х2
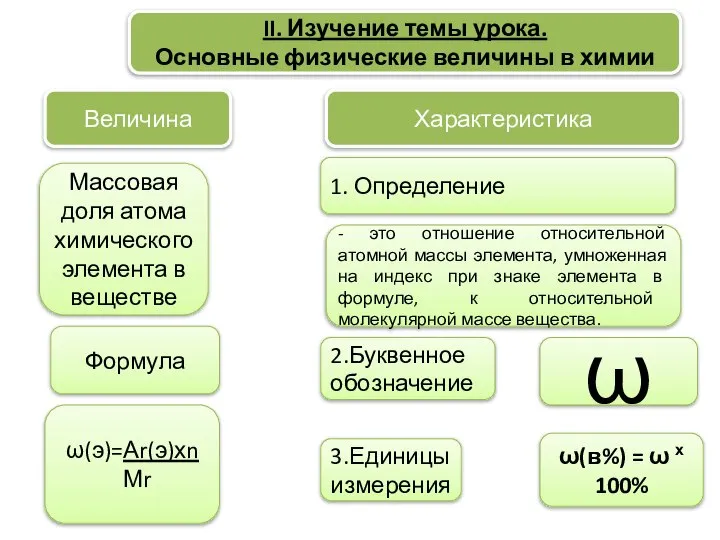
- 6. II. Изучение темы урока. Основные физические величины в химии Характеристика Величина ω(э)=Аr(э)хn Мr Формула Массовая доля
- 7. Вычисление массовой доли элемента в веществе Вычислить массовую долю кислорода в молекуле воды. ω(О)=Аr(О)хn Мr(Н2О) Мr(Н2О)
- 8. Вычисление массовой доли элемента в веществе (работа у доски) Вычислить массовую долю элементов в молекуле углекислого
- 9. Вычислить в молекуле какого вещества массовая доля кислорода больше. Н2О, СО2, К2О, СаО Мr(Н2О) = Аr(Н)х2+
- 10. ω(О)= Аr(О)хn = 16 х100% =89% Мr(Н2О) 18 ω(О)= Аr(О)х2 = 32 х100% = 72,7% Мr(СО2)
- 11. III. Закрепление изученного материала. Вычисление массовой доли элемента в веществе. Самостоятельная работа в тетради. Вычислить массовую
- 12. Домашнее задание ДИ 1. С.8-13; с.11,зад..6,7
- 14. Скачать презентацию









 Химические формулы
Химические формулы 9-8 кислоты в свете ТЭД (1)
9-8 кислоты в свете ТЭД (1) Спирты
Спирты Адсорбционно-десорбционные взаимодействия фосфатов кальция и аминокислот
Адсорбционно-десорбционные взаимодействия фосфатов кальция и аминокислот Соли как производные кислот и оснований
Соли как производные кислот и оснований Интерактивная интеллектуальная игра Юный химик
Интерактивная интеллектуальная игра Юный химик Класс оксиды
Класс оксиды Обобщение знаний об углеводородах
Обобщение знаний об углеводородах ЕГЭ по химии: документы, регламентирующие структуру и содержание контрольных измерительных материалов
ЕГЭ по химии: документы, регламентирующие структуру и содержание контрольных измерительных материалов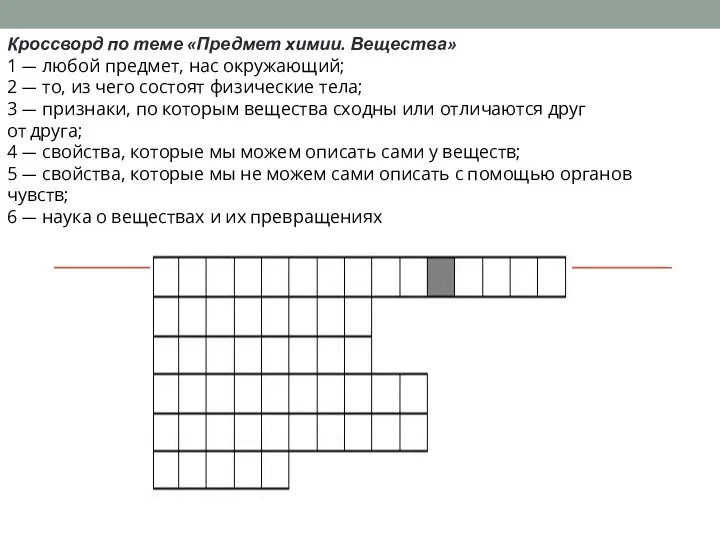 Предмет химии. Вещества
Предмет химии. Вещества 3bc28ca0711047a6880d20a6763f17db
3bc28ca0711047a6880d20a6763f17db Общая характеристика оксидов
Общая характеристика оксидов Золото
Золото Органическая химия. Ароматические углеводороды
Органическая химия. Ароматические углеводороды Методы получения нафтиридинов (всех изомеров)
Методы получения нафтиридинов (всех изомеров) Нефть и её переработка
Нефть и её переработка Оксид кремния
Оксид кремния Основания: номенклатура, классификация, применение, физические свойства
Основания: номенклатура, классификация, применение, физические свойства Алмаз. Свойства алмазов
Алмаз. Свойства алмазов Презентация на тему Соединения серы
Презентация на тему Соединения серы  Свойства солей, оксидов, оснований
Свойства солей, оксидов, оснований Модель химического образования на основе технологического подхода. Методическая система учителя химии
Модель химического образования на основе технологического подхода. Методическая система учителя химии Техника титрования и лабораторная посуда
Техника титрования и лабораторная посуда Уровень С1 в ГИА
Уровень С1 в ГИА Задачи. Периодическая система. Строение атома. Повторение
Задачи. Периодическая система. Строение атома. Повторение Азотсодержащие гетероциклические соединения пиррол
Азотсодержащие гетероциклические соединения пиррол Предельные углеводороды. Тест 19
Предельные углеводороды. Тест 19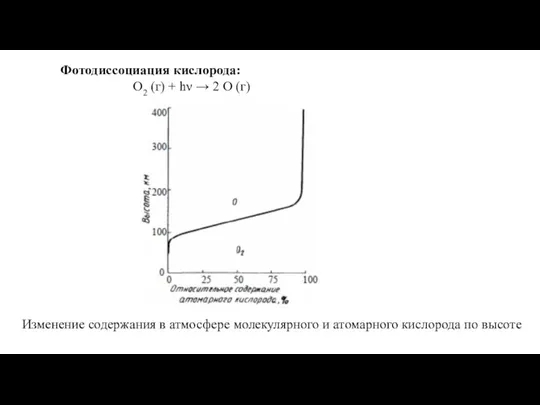 Фотодиссоциация кислорода
Фотодиссоциация кислорода