Содержание
- 2. Кислород как элемент. 1. Элемент кислород находится в VI группе, главной подгруппе, II периоде, порядковый номер
- 3. Кислород как элемент (продолжение). 4. В земной коре его 49% по массе, в гидросфере – 89%
- 4. Физические свойства Газ - без цвета, вкуса и запаха; в 100V H2O растворяется 3V O2 (н.у.);
- 5. Химические свойства С неметаллами C + O2 → CO2 S + O2 → SO2 2H2 +
- 6. Способы получения Промышленный способ (перегонка жидкого воздуха). Лабораторный способ (разложение некоторых кислородосодержащих веществ) 2KClO3 –t°;MnO2→ 2KCl
- 7. Способы получения кислорода (продолжение). перманганата калия при нагревании: 2KMnO4 –t°→ K2MnO4 + MnO2 + O2↑ Разложение
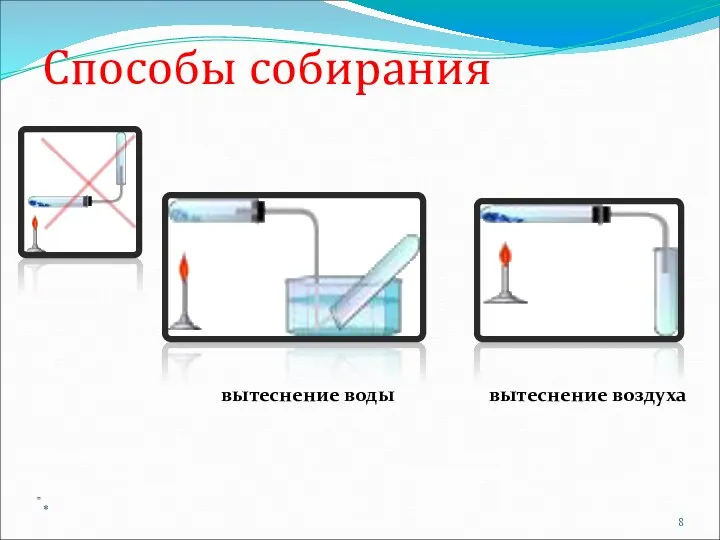
- 8. Способы собирания вытеснение воды вытеснение воздуха = *
- 10. Скачать презентацию






 Химические средства защиты растений
Химические средства защиты растений Степень окисления
Степень окисления Презентация на тему Стронций
Презентация на тему Стронций  углеводы (1)
углеводы (1) Протолитические буферные системы. Буферные системы организма, их взаимодействие
Протолитические буферные системы. Буферные системы организма, их взаимодействие Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства
Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства Коферменты. Промышленное получение и применение ферментов
Коферменты. Промышленное получение и применение ферментов Лиофильные и лиофобные дисперсные системы. Свойства лиофильных систем. Лекция 12
Лиофильные и лиофобные дисперсные системы. Свойства лиофильных систем. Лекция 12 Презентация на тему Альдегиды
Презентация на тему Альдегиды  Кислород
Кислород Классификация химических реакций
Классификация химических реакций Dereglarea metabolismului
Dereglarea metabolismului Окислительно-восстановительные реакции. Типы химических реакций
Окислительно-восстановительные реакции. Типы химических реакций Термокаталитические процессы переработки нефтяных фракций
Термокаталитические процессы переработки нефтяных фракций 175 – летию со дня рождения Дмитрия Ивановича Менделеева посвящается… АВТОР ПРЕЗЕНТАЦИИ: учитель химии МОУ СОШ №2 города Ртищево Саратовской области ПОПКОВА Е.Г.
175 – летию со дня рождения Дмитрия Ивановича Менделеева посвящается… АВТОР ПРЕЗЕНТАЦИИ: учитель химии МОУ СОШ №2 города Ртищево Саратовской области ПОПКОВА Е.Г. SHOT.шампуни. Состав. Компоненты
SHOT.шампуни. Состав. Компоненты Презентация на тему Количество вещества. Молярная масса
Презентация на тему Количество вещества. Молярная масса  Органическая химия. Теория строения органических соединений
Органическая химия. Теория строения органических соединений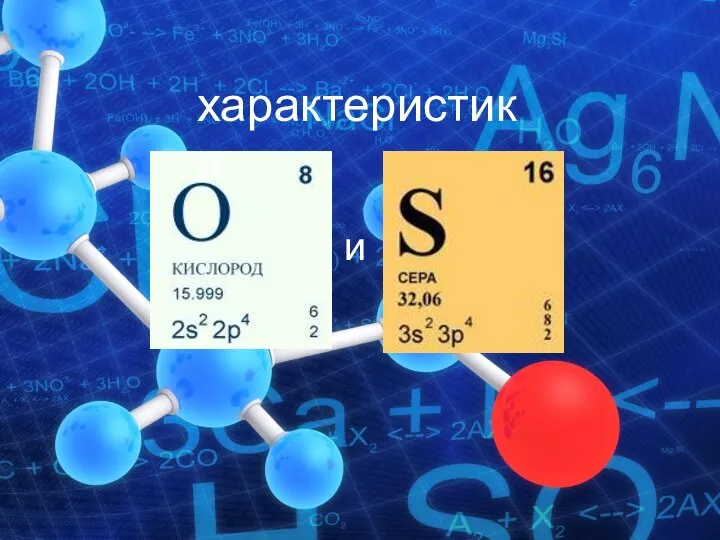 Характеристика кислорода и серы
Характеристика кислорода и серы Reactivi444
Reactivi444 Процессы в растворах: электролитическая диссоциация (ЭД)
Процессы в растворах: электролитическая диссоциация (ЭД) (Bu4N)2[Mo6I8(OOCCH3)6]. Синтез
(Bu4N)2[Mo6I8(OOCCH3)6]. Синтез Общая характеристика элементов главной подгруппы VI группы (подгруппы кислорода)
Общая характеристика элементов главной подгруппы VI группы (подгруппы кислорода) Классификация органических соединений. Предельные углеводороды (УВ)
Классификация органических соединений. Предельные углеводороды (УВ) Расчеты по химическим уравнениям
Расчеты по химическим уравнениям Закон сохранения массы веществ
Закон сохранения массы веществ Молярная масса вещества
Молярная масса вещества Свойства кислорода. Оксиды
Свойства кислорода. Оксиды