Содержание
- 2. Вспомни… Какие соединения называют оксидами? СаО, SО2, ВаО , Nа2О, Сl2О7, Al2O3 Какие соединения относят к
- 3. Работа с карточками Из предложенного списка веществ выпишите оксиды и щёлочи: CaO, CI2O7, NaOH, HCI, CO2,
- 4. Правильные ответы: Оксиды: CaO, CI2O7, CO2 , AL2O3, K2O, N2O5, SO3 Щёлочи: NaOH, LiOH, КОН
- 5. Тема урока: «КИСЛОТЫ» Цель урока: изучение строения, классификации и свойств неорганических кислот
- 6. Задачи урока: изучить строение и свойства кислот; познакомиться с классификацией кислот; узнать формулы некоторых неорганических кислот;
- 7. Кислоты в природе Муравьиная кислота Лимонная кислота Аскорбиновая кислота
- 8. Кислоты в жизни человека В медицине В кулинарии и продуктах питания В народном хозяйстве В организме
- 9. Кислотные дожди – одна из экологических проблем Н2О Н2О Н2О NО2 SО2 Н2S Н2SО3 НNО3 НNО2
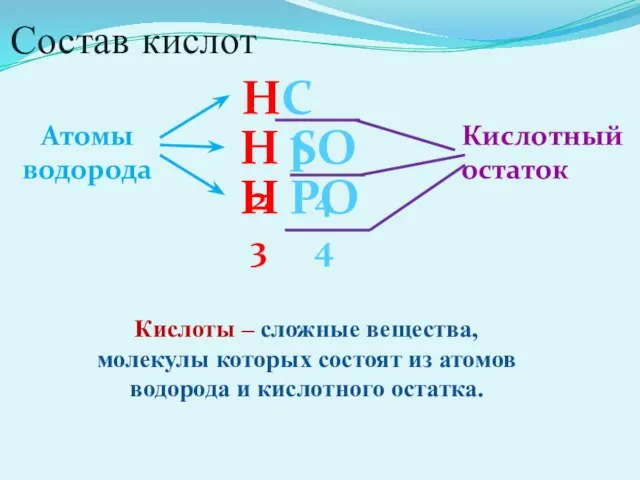
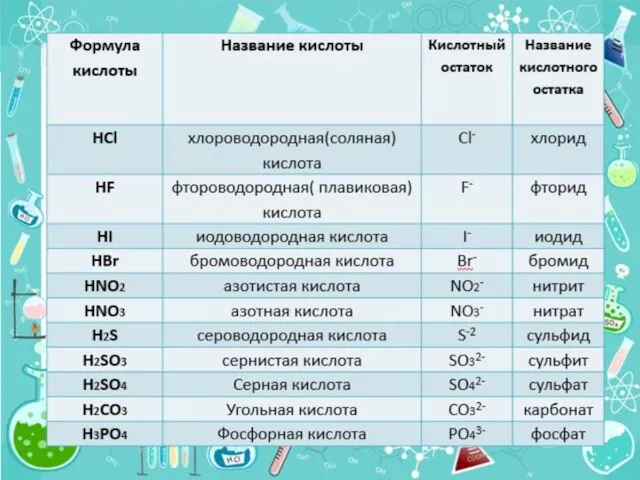
- 10. Состав кислот Н Сl Н2 SО4 Н3 РО4 Атомы водорода Кислотный остаток Кислоты – сложные вещества,
- 11. Независимо от вида кислоты, индикаторы изменяют свой цвет одинаково, а это означает, что все кислоты обладают
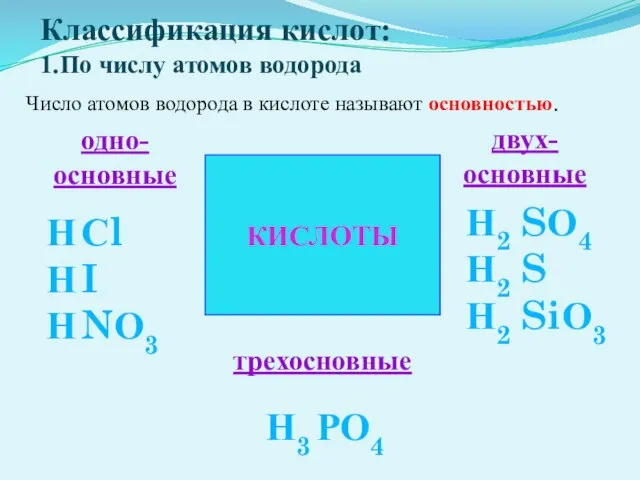
- 13. Классификация кислот: 1.По числу атомов водорода КИСЛОТЫ Сl I NО3 SО4 S SiО3 РО4 одно- основные
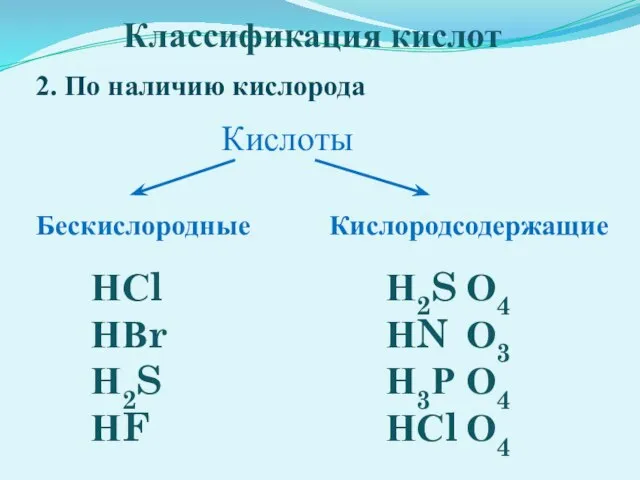
- 14. Кислоты Бескислородные Кислородсодержащие НСl НВr Н2S НF Н2S НN Н3Р НСl Классификация кислот 2. По наличию
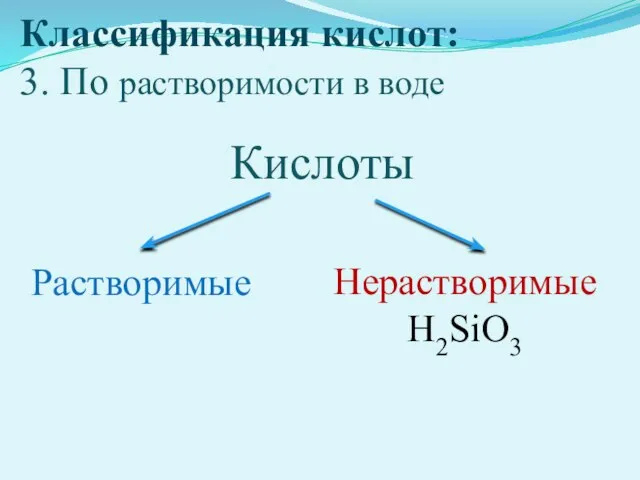
- 15. Классификация кислот: 3. По растворимости в воде Кислоты Растворимые Нерастворимые H2SiO3
- 16. Серная кислота - H2SO4
- 17. Физкультминутка Очень химию мы любим! Шеей влево, вправо крутим. Воздух – это атмосфера. Если правда -
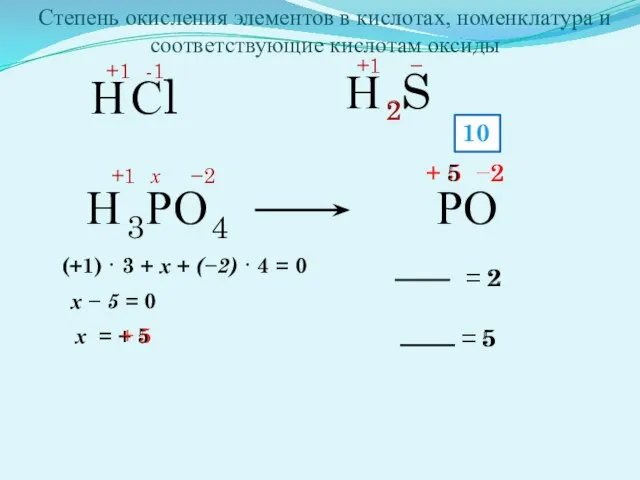
- 18. Степень окисления – это условный заряд атомов химического элемента в соединении, вычисленный из предположения, что все
- 19. Н Сl +1 -1 Н +1 − 2 S 2 Н 3 РО 4 +1 −2
- 20. Дайте характеристику кислотам по алгоритму: Название кислоты Наличие кислорода Основность Растворимость Степень окисления элементов, образующих кислоту
- 21. Кислотные оксиды CI2 O7 → CO2 → N2 O5 → S O3 →
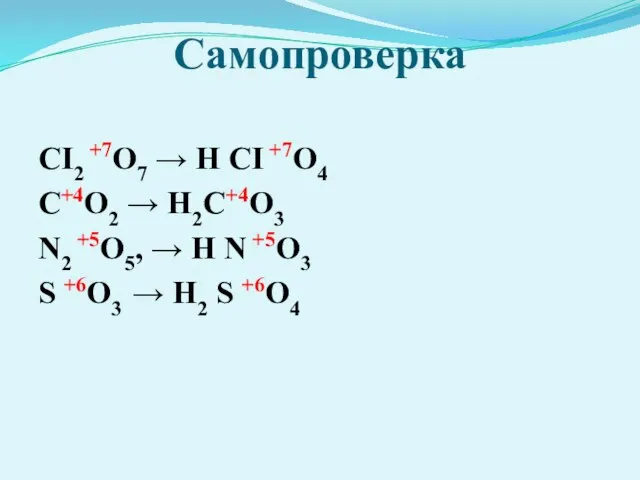
- 22. Самопроверка CI2 +7O7 → Н CI +7O4 C+4O2 → Н2С+4О3 N2 +5O5, → Н N +5O3
- 23. Домашнее задание: Выучить формулы и названия кислот § 21; Дать характеристику кремниевой кислоте по алгоритму ;
- 25. «День прожит не зря, если ты узнал что-то новое»
- 26. Спасибо за урок !
- 28. Скачать презентацию

















 Условия среды, вызывающие коррозию металла
Условия среды, вызывающие коррозию металла Комментарии к выполненным заданиям по темам Алканы и Алкены. 9 класс
Комментарии к выполненным заданиям по темам Алканы и Алкены. 9 класс ФБОУ- Раздольненская средняя общеобразовательная школа №19 Новосибирского района Новосибирской области
ФБОУ- Раздольненская средняя общеобразовательная школа №19 Новосибирского района Новосибирской области Характеристика химического элемента-неметалла на основании его положения в ПСХЭ Д.И.Менделеева. 9 класс
Характеристика химического элемента-неметалла на основании его положения в ПСХЭ Д.И.Менделеева. 9 класс Электролитическая диссоциация
Электролитическая диссоциация Классификация ХГ методов разделения
Классификация ХГ методов разделения Значение химии в медицине
Значение химии в медицине Рубидий (лат. Rubidium)
Рубидий (лат. Rubidium) Реакции соединения
Реакции соединения Кинетика химических реакций
Кинетика химических реакций Введение в органическую химию
Введение в органическую химию Пятая группа элементов
Пятая группа элементов Французский физик, химик, металловед 1850 - 1936
Французский физик, химик, металловед 1850 - 1936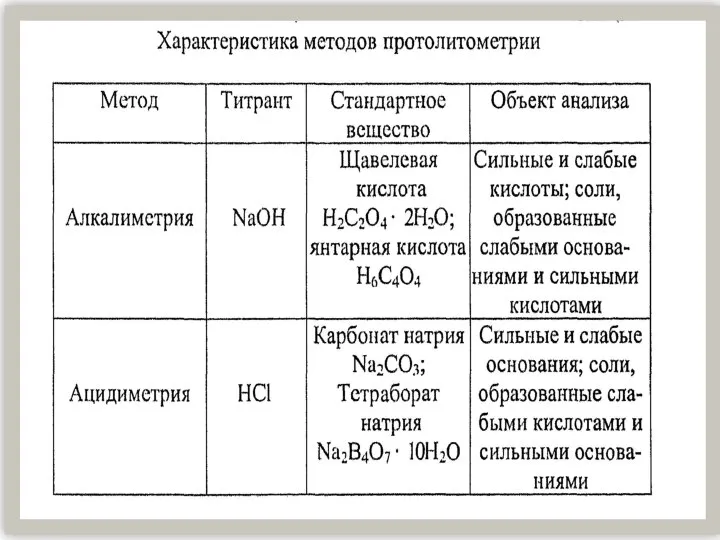 Характеристика методов протолитометрии
Характеристика методов протолитометрии Соединения серы
Соединения серы Движение молекул
Движение молекул Индиго-краситель
Индиго-краситель Селективность (реакторы)
Селективность (реакторы) Презентация на тему Алканолы
Презентация на тему Алканолы  Кинетика физико-химических процессов
Кинетика физико-химических процессов кремний и его соединения
кремний и его соединения Водород
Водород Закон сохранения массы
Закон сохранения массы Пиримидин (шестичленный гетероцикл с двумя атомами азота)
Пиримидин (шестичленный гетероцикл с двумя атомами азота) Типы загрязнений биосферы
Типы загрязнений биосферы Кислоты в свете теории электролитической диссоциации
Кислоты в свете теории электролитической диссоциации Поделочный камень родонит
Поделочный камень родонит Получение углекислого газа и изучение его свойств. Практическая работа
Получение углекислого газа и изучение его свойств. Практическая работа