Слайд 3 2Н2 + О2 ⇌ 2H2O + Q
N2 + O2 ? 2NO – Q
2Al(OH)3 ? Al2O3 + H2O
HCl (ж) + KOH (ж) ? KCl (ж) +
2Н2 + О2 ⇌ 2H2O + Q
N2 + O2 ? 2NO – Q
2Al(OH)3 ? Al2O3 + H2O
HCl (ж) + KOH (ж) ? KCl (ж) +
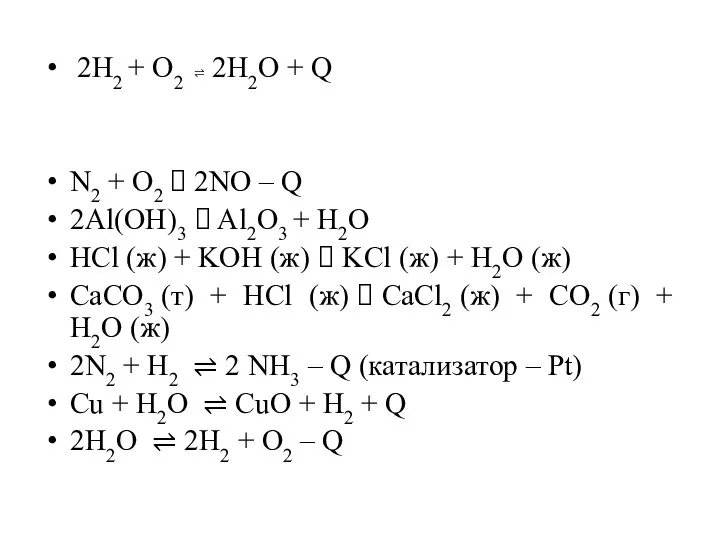
H2O (ж)
СaCO3 (т) + HCl (ж) ? CaCl2 (ж) + CO2 (г) + H2O (ж)
2N2 + H2 ⇌ 2 NH3 – Q (катализатор – Pt)
Cu + H2O ⇌ CuO + H2 + Q
2H2O ⇌ 2H2 + O2 – Q
СaCO3 (т) + HCl (ж) ? CaCl2 (ж) + CO2 (г) + H2O (ж)
2N2 + H2 ⇌ 2 NH3 – Q (катализатор – Pt)
Cu + H2O ⇌ CuO + H2 + Q
2H2O ⇌ 2H2 + O2 – Q


 Презентация на тему Химия и здоровье человека (10 класс)
Презентация на тему Химия и здоровье человека (10 класс)  Признаки реакции
Признаки реакции Нефть: история и ее применение
Нефть: история и ее применение Химические свойства спиртов и фенола
Химические свойства спиртов и фенола Диссоциация. Уравнения диссоциации
Диссоциация. Уравнения диссоциации Генетическая связь между классами неорганических соединений
Генетическая связь между классами неорганических соединений Комбинаторика в химии
Комбинаторика в химии Презентация по Химии "Ароматические углеводороды в природе. Области их применения"
Презентация по Химии "Ароматические углеводороды в природе. Области их применения" 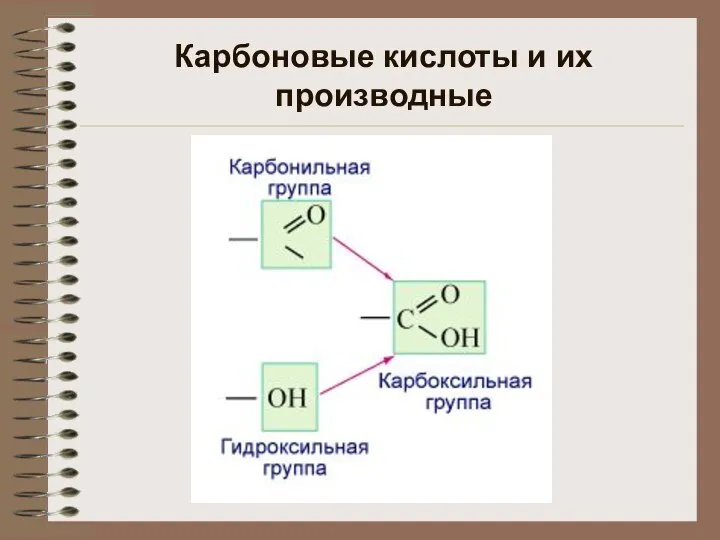 Карбоновые кислоты и их производные
Карбоновые кислоты и их производные Углеводороды в природе
Углеводороды в природе Кислоты
Кислоты Разделение смесей веществ
Разделение смесей веществ Химическая промышленность
Химическая промышленность Презентация на тему Теория строения органических соединений А.М. Бутлерова
Презентация на тему Теория строения органических соединений А.М. Бутлерова  Производство серной кислоты
Производство серной кислоты Наноматеріали. Тіт Лукрецій Кар
Наноматеріали. Тіт Лукрецій Кар Комплексные соединения
Комплексные соединения Химическая связь в органических соединениях
Химическая связь в органических соединениях Презентация на тему Щелочные и щелочноземельные металлы
Презентация на тему Щелочные и щелочноземельные металлы  ПОЛОЖЕНИЕ ВОДОРОДА В ПЕРИОДИЧЕСКОЙ СИСТЕМЕ
ПОЛОЖЕНИЕ ВОДОРОДА В ПЕРИОДИЧЕСКОЙ СИСТЕМЕ Цельное молоко: полезно или опасно для здоровья? (сравнительная характеристика качества восстановленного и цельного молока)
Цельное молоко: полезно или опасно для здоровья? (сравнительная характеристика качества восстановленного и цельного молока) История химии
История химии Презентация на тему Алмаз, графит и фуллерен
Презентация на тему Алмаз, графит и фуллерен  Увлекательный мир химии
Увлекательный мир химии Тривиальные названия веществ, наиболее часто встречаемых в ЕГЭ
Тривиальные названия веществ, наиболее часто встречаемых в ЕГЭ Взаимодействие металлов с водой, щелочами, кислотами, солями, простыми веществами
Взаимодействие металлов с водой, щелочами, кислотами, солями, простыми веществами Основы МКТ
Основы МКТ Презентация по Химии "Ковалентная химическая связь"
Презентация по Химии "Ковалентная химическая связь"