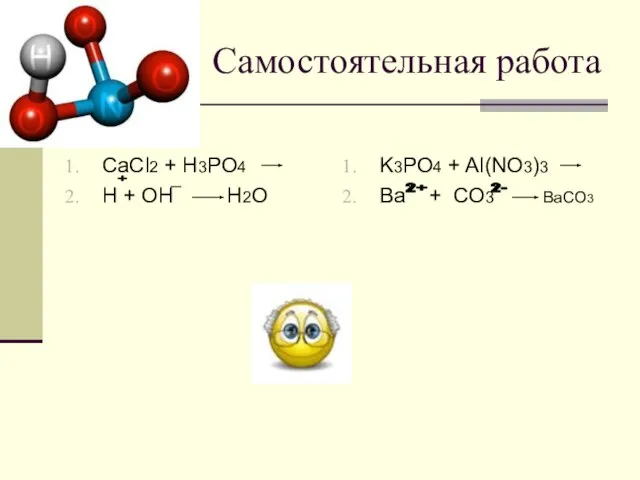
Слайд 2Самостоятельная работа
CaCl2 + H3PO4
H + OH H2O
K3PO4 + Al(NO3)3
Ba + CO3 BaCO3
+
Слайд 3Подумай
Были ли у тебя вопросы при выполнении домашнего задания?
Трудно ли составлять ионные

уравнения?
Нет ли у тебя пробелов в знаниях по химии?
Ты всегда молодец?
Слайд 5Типичные реакции
Кислота + основание = соль + вода (о)
Кислота + оксид металла
= соль + вода (о)
Кислота + металл = соль + водород (з)
Кислота + соль = новая кислота + новая соль (о)
Слайд 6Лабораторный опыт №7
Тема: Реакции характерные для растворов кислот.
Цель: Изучить свойства растворов кислот
Оборудование

и реактивы: штатив,
пробирки, NaOH, HCl, ф-ф, Al, H2SO4, CuO, BaCl2
Ход работы:
Слайд 7Реакция нейтрализации
Возьмите пробирку налейте 2-3 мл NaOH добавьте 1 каплю ф-ф, что

наблюдаете? Прилейте 2-3 мл HCl. Что вы увидели. Запишите уравнение реакции, протекающей в пробирке, его полное и сокращённое ионное уравнение.
Слайд 8Кислота + оксид металла
Возьмите 1г оксида меди (2) и прилейте к нему

2-3 мл серной кислоты. Нагрейте содержимое пробирки на спиртовке. Что вы наблюдаете? Запишите молекулярное уравнение реакции, полное и сокращённое ионное уравнение.
Слайд 9Кислота + металл
Возьмите гранулу алюминия и прилейте к ней 2-3 мл соляной

кислоты. Что наблюдаете? Запишите уравнения реакции.
Как реагируют кислоты с металлами? Какие есть особенности?
Слайд 10Кислота + соль
В пробирку налейте 2-3 мл хлорида бария и прилейте

2-3 мл серной кислоты. Что вы наблюдаете запишите уравнения реакции.
Вывод: Какие свойства кислоты проявляют в растворе?
Слайд 11Домашнее задание
§38 – «3»
№2 – «4»
№5 – «5»









 Подача питательной воды в парогенератор при запроектной аварии
Подача питательной воды в парогенератор при запроектной аварии Гетерогенные дисперсные системы
Гетерогенные дисперсные системы Смеси: гетерогенные, гомогенные
Смеси: гетерогенные, гомогенные Материаловедение. Строение металлических материалов. Металлические сплавы
Материаловедение. Строение металлических материалов. Металлические сплавы Способы получения металлов
Способы получения металлов Смолисто-асфальтеновые вещества
Смолисто-асфальтеновые вещества Перспективы использования микроволнового излучения в органической химии
Перспективы использования микроволнового излучения в органической химии Основы химической кинетики
Основы химической кинетики Общая характеристика элементов главной подгруппы VI группы (подгруппы кислорода)
Общая характеристика элементов главной подгруппы VI группы (подгруппы кислорода) Development of the system of concepts on the topic redox reactions in the school course of inorganic chemistry
Development of the system of concepts on the topic redox reactions in the school course of inorganic chemistry Биотит и тальк
Биотит и тальк Строение электронных оболочек атомов элементов
Строение электронных оболочек атомов элементов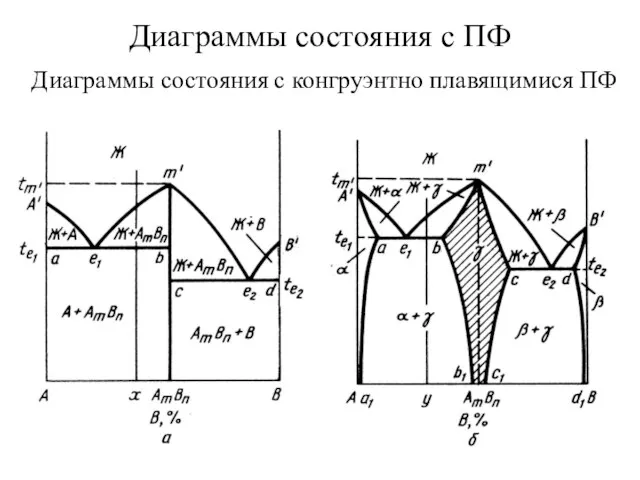 Диаграммы состояния с ПФ. Диаграммы состояния с конгруэнтно плавящимися ПФ
Диаграммы состояния с ПФ. Диаграммы состояния с конгруэнтно плавящимися ПФ Презентация на тему Йод
Презентация на тему Йод  Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Классификация органических соединений
Классификация органических соединений Химическая связь
Химическая связь 10-4 (2)
10-4 (2) Плазменное состояние вещества
Плазменное состояние вещества Презентация на тему Электролиз расплавов и растворов
Презентация на тему Электролиз расплавов и растворов  Важнейшие классы неорганических соединений
Важнейшие классы неорганических соединений Турнир знатоков химии. Химическая лихорадка
Турнир знатоков химии. Химическая лихорадка Ministry of Education and Science of the Russian Federation
Ministry of Education and Science of the Russian Federation Получение металлов
Получение металлов Строение, свойства и функции аминокислот и белков
Строение, свойства и функции аминокислот и белков Свойства растворов электролитов
Свойства растворов электролитов Кислоты. Классификация. Номенклатура
Кислоты. Классификация. Номенклатура Изомерия. Упрощенная классификация органических соединений
Изомерия. Упрощенная классификация органических соединений