Содержание
- 3. км
- 4. вещество молекула
- 5. Необходимо взять столько граммов вещества, какова относительная атомная или относительная молекулярная масса этого вещества. Как отмерить
- 6. молекула воды 1 моль воды = 18 г Mr(H2O) = 18
- 7. молекула кислорода 1 моль кислорода = 32 г Mr(O2) = 32
- 9. Лоренцо Авогадро (1776 – 1856 гг.) При одинаковых температуре и давлении в равных объёмах идеальных газов
- 13. Число молекул (N)
- 14. Число молекул (N)
- 15. М — молярная масса M = 1 г/моль М (Н2) = 2 г/моль М (FeS) =
- 16. М — молярная масса M = 1 г/моль М (Н2) = 2 г/моль М (FeS) =
- 17. Количество вещества (n)
- 18. Молярная масса — физическая величина, которая равна отношению массы вещества к его количеству.
- 19. Задача 1. Сколько молекул содержит углекислый газ количеством вещества 2,5 моль?
- 20. Задача 1. Сколько молекул содержит углекислый газ количеством вещества 2,5 моль? Дано:
- 21. Задача 1. Сколько молекул содержит углекислый газ количеством вещества 2,5 моль? Дано:
- 22. Задача 1. Сколько молекул содержит углекислый газ количеством вещества 2,5 моль? Дано: Решение.
- 23. Задача 1. Сколько молекул содержит углекислый газ количеством вещества 2,5 моль? Дано: Решение.
- 24. Задача 2. Какова масса железа (в граммах), соответствующая количеству вещества 0,25 моль?
- 25. Задача 2. Какова масса железа (в граммах), соответствующая количеству вещества 0,25 моль? Дано:
- 26. Задача 2. Какова масса железа (в граммах), соответствующая количеству вещества 0,25 моль? Дано: m(Fe) – ?
- 27. Задача 2. Какова масса железа (в граммах), соответствующая количеству вещества 0,25 моль? Дано: m(Fe) – ?
- 28. Задача 2. Какова масса железа (в граммах), соответствующая количеству вещества 0,25 моль? Дано: m(Fe) – ?
- 29. Задача 3. Определите массу хлора (Cl), содержащегося в 29,25 г поваренной соли (NaCl).
- 30. Задача 3. Определите массу хлора (Cl), содержащегося в 29,25 г поваренной соли (NaCl). Дано: M(Na) =
- 31. Задача 3. Определите массу хлора (Cl), содержащегося в 29,25 г поваренной соли (NaCl). Дано: M(Na) =
- 33. Скачать презентацию


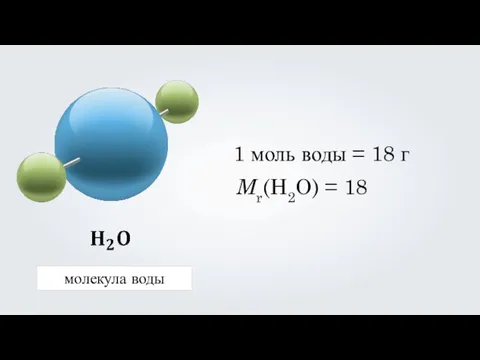
























 Атом
Атом Презентация 1
Презентация 1 Виды нагрева и материалы резистивных нагревателей, их стойкость к температуре, ростовой атмосфере и расплаву
Виды нагрева и материалы резистивных нагревателей, их стойкость к температуре, ростовой атмосфере и расплаву Получение аминов
Получение аминов Расчеты по уравнениям химических реакций
Расчеты по уравнениям химических реакций Оксиды, их классификация и химические свойства. 8 класс
Оксиды, их классификация и химические свойства. 8 класс Строение вещества
Строение вещества Виды химической связи. Обобщение и систематизация знаний
Виды химической связи. Обобщение и систематизация знаний Химические реакции
Химические реакции Морфологогия минералов
Морфологогия минералов Природа и типы химических связей
Природа и типы химических связей Презентация на тему Вещества и их свойства
Презентация на тему Вещества и их свойства  ВКР: Определение показателей качества мясной и колбасной продукции различных производителей
ВКР: Определение показателей качества мясной и колбасной продукции различных производителей Презентация на тему Физические и химические явления 8 класс
Презентация на тему Физические и химические явления 8 класс  Изомерия. Виды изомерии
Изомерия. Виды изомерии Презентация на тему Халькогены
Презентация на тему Халькогены  Азотная кислота
Азотная кислота Метелёва И.Е. учитель химии
Метелёва И.Е. учитель химии Решение заданий ОГЭ по химии (1 - 15)
Решение заданий ОГЭ по химии (1 - 15) Химия и производство
Химия и производство Алканы
Алканы Анализ воды природных источников посёлков Фруктовая и Красная Пойма городского округа Луховицы
Анализ воды природных источников посёлков Фруктовая и Красная Пойма городского округа Луховицы Салициловая кислота
Салициловая кислота Масляная кислота
Масляная кислота Кумарон - индендық полимерлер
Кумарон - индендық полимерлер Классификация химических реакций
Классификация химических реакций Нефть
Нефть Водородная химическая связь
Водородная химическая связь