Слайд 2План
Комплексиметрия и ее классификация. Реакции комплексообразования, которые используют в титриметрии, требования к

ним.
Комплексонометрия. Способы комплексоно-метрического титрования.
Построение кривых титрования в методе комплексонометрии.
Индикаторы метода комплексонометрии. Использование комплексонометрии в фарманализе.
Слайд 3Комплексиметрическое титрование, или комплексиметрия -
В методе комплексиметрического титрования выделяют такие методы:
меркуриметрия
фторидометрия

цианидометрия
комплексонометрия
Слайд 4Требования к реакциям в комплексиметрии:
Реакция должна протекать стехиометрически.
Реакция должна протекать количественно и

до конца, константа стойкости комплекса должна быть больше β≥108.
Реакция образования комплексного соединения должна протекать быстро.
Должна быть возможность фиксации точки эквивалентности.
В условиях проведения титрования не должны протекать конкурирующие реакции.
Слайд 5Комплексонометрия
Комплексон І: нитрилтриацетатная кислота (тетрадентатный)
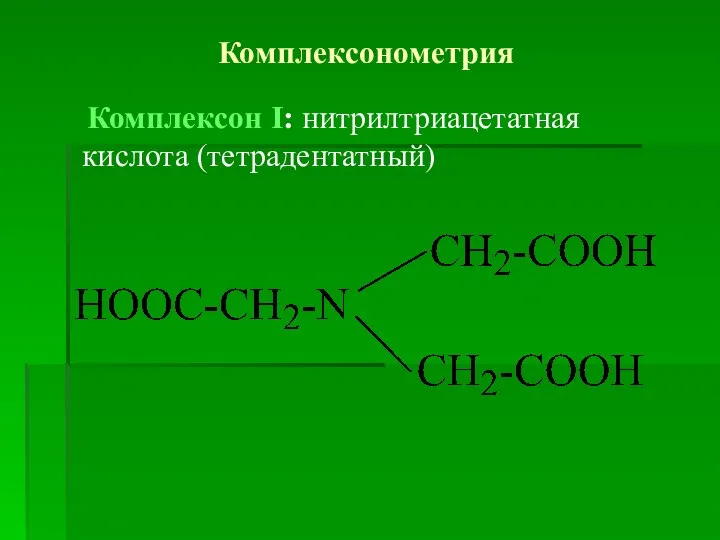
Слайд 6 Комплексон ІІ: этилендиамминтетра-ацетатная кислота (ЭДТА)
Комплексон ІІІ: этилендиамминтетраацетат натрия (Na-ЭДТА, трилон Б,
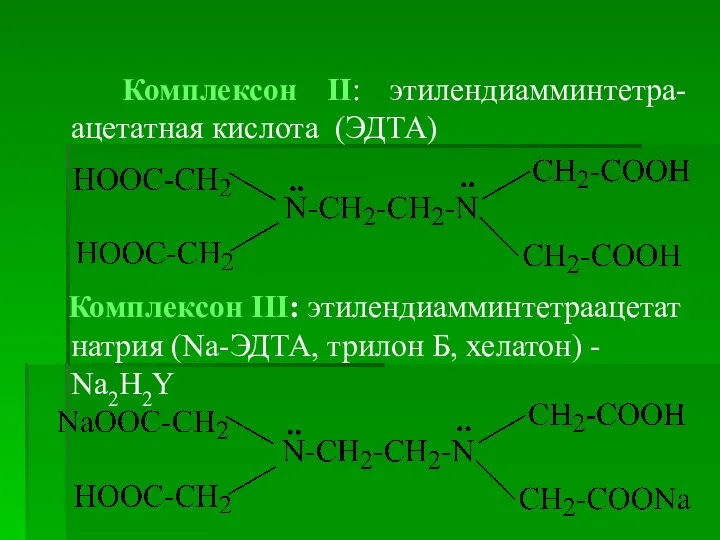
хелатон) - Na2H2Y
Слайд 7Комплексон ІV: циклогексилдиаммин-тетраацетатная кислота
Комплексоны вступают в реакции с катионами многих металлов в
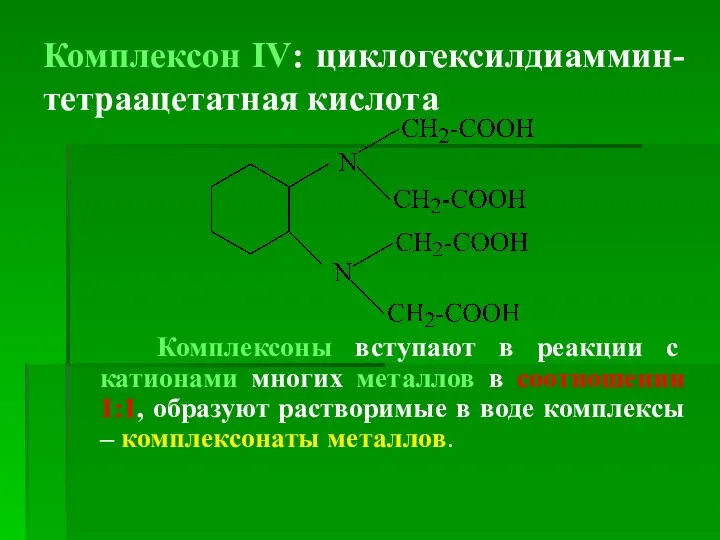
соотношении 1:1, образуют растворимые в воде комплексы – комплексонаты металлов.
Слайд 8Преимущества использования комплексонов
хорошо растворимы в воде и некоторых других органических растворителях
повышенная устойчивость

комплексов
реакции протекают стехиометрически (нет ступенчатого комплексообразования)
некоторые комплексоны являются специфическими реагентами на отдельные ионы металлов (избирательное действие)
широкое использование их как маскирующих реагентов
быстрота протекания реакции
Слайд 9Комплексонометрия
Титрант: 0,05 моль/л раствор натриевая соль эдта
Реакции метода:
Са2+ + H2Y2-

→ CaY2- + 2H+
In3+ + H2Y2- → InY- + 2H+
Th4+ + H2Y2- → ThY + 2H+
Слайд 10Комплексонометрия
Индикаторы: металлохромные
Общая реакция метода:
Men+ + H2Y2- → MeYn-4 + 2H+
Men+ +

Y4- → MeY(n-4)+
На концентрацию ионов металла влияет рН – образуются гидроксокомплексы
На концентрацию Y4- влияет рН среды
Слайд 11Условия комплексонометрического титрования
высокая устойчивость комплексонатов металлов (βст.)
придерживание конкретного значения кислотности среды
использование буферных

растворов (для связывания ионов Н+, которые выделяются)
только отдельные катионы (Fе3+, In3+, Sc3+, ZnIV, ТhIV), которые образуют очень устойчивые комплексы с комплексоном, титруются в кислой среде
Слайд 12Прямое комплексонометрическое титрование
Условия использования:
высокая скорость реакции
реакция проходит количественно, стехиометрически, до конца
есть индикатор,

который позволяет надежно фиксировать к.т.т.
можно титровать смесь катионов
Определяемые ионы: большинство катионов металлов
Слайд 13Способы повышения селективности прямого титрования:
Регулирование рН среды
ионы Fе3+, Ga3+, In3+, Tl3+, Ві3+,

при рН~2
при рН = 5 – Аl3+, Co3+, Ni2+, Cu2+, Zn2+, Cd2+
при рН = 9 – щелочноземельные металлы
2. Использование маскирующих реагентов:
ионы F-, P2O72-, CN-, Н2С4Н4О6 и др.
ионы Со(II), Ni(II), Zn(II), Cd(II) и Hg(II) могут быть замаскированы цианид-ионами
3. Изменение степени окисления
Fe3+ маскируют восстановлением до Fe2+
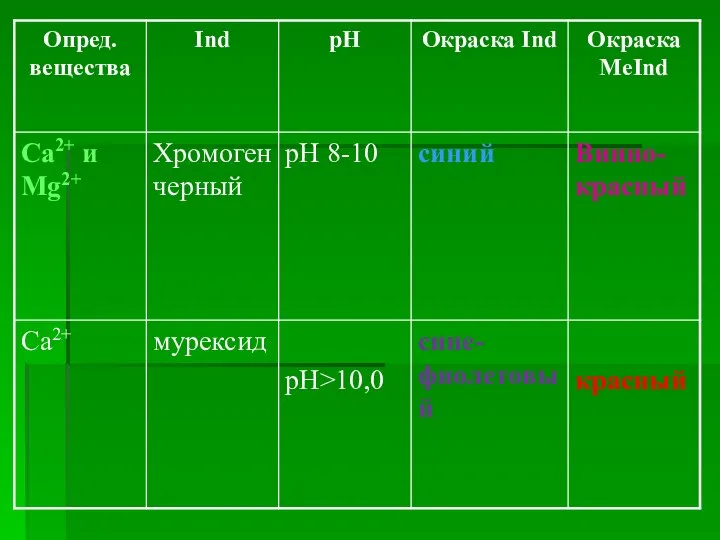
Слайд 14Требования к индикаторам в комплексонометрии
металл и индикатор должны давать комплекс в соотношении

1:1
окраска индикатора должна отличаться от окраски комплекса MeInd
комплекс MeInd должен быть достаточно устойчивым
устойчивость комплекса MeInd должна быть меньше устойчивости комплексоната металла MeY, который является продуктом титрования (разница в 10-100 раз)
комплекс MeІnd должен быть лабильным
изменение окраски при титровании должно быть контрастным
Слайд 15Металлоиндикаторы
сами не окрашены металлохромные
специфические:
Fe3+ - сульфосалициловая сами окрашены, поскольку
кислота (красная
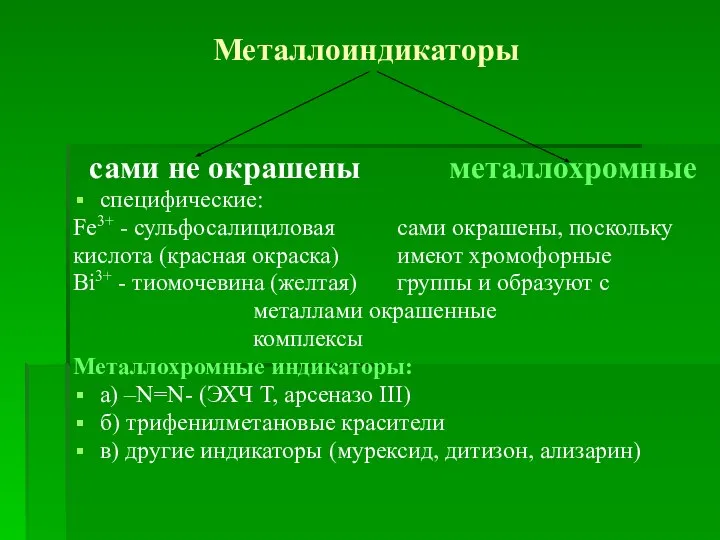
окраска) имеют хромофорные
Ві3+ - тиомочевина (желтая) группы и образуют с
металлами окрашенные
комплексы
Металлохромные индикаторы:
а) –N=N- (ЭХЧ Т, арсеназо ІІІ)
б) трифенилметановые красители
в) другие индикаторы (мурексид, дитизон, ализарин)
Слайд 16Механизм изменения окраски
металлохромных индикаторов
Me2+ + Іnd ⇔ MeІnd-
синий красный
MeІnd +

H2Y2- ⇔ MeY2- + H2Іnd
красный бесцветный синий















 Алкины (Ацетиленовые углеводороды)
Алкины (Ацетиленовые углеводороды) Соли как производные кислот и оснований
Соли как производные кислот и оснований Диссоциация. Уравнения диссоциации
Диссоциация. Уравнения диссоциации Состав и значение воздуха
Состав и значение воздуха Решение задач на нахождение молекулярной формулы газообразного алкана
Решение задач на нахождение молекулярной формулы газообразного алкана Реакционная система. Схема химической реакции. Закон сохранения массы веществ в химической реакции
Реакционная система. Схема химической реакции. Закон сохранения массы веществ в химической реакции Образование раствора
Образование раствора Горные породы
Горные породы Структура и функции нуклеиновых кислот
Структура и функции нуклеиновых кислот Органическая химия. Пищевые добавки
Органическая химия. Пищевые добавки Строение и химические свойства галогенов
Строение и химические свойства галогенов Жиры. Классификация жиров
Жиры. Классификация жиров Хлор. Распространение хлора в природе
Хлор. Распространение хлора в природе Свойства воды
Свойства воды Презентация на тему Глюкоза (10 класс)
Презентация на тему Глюкоза (10 класс)  Инструкция по самостоятельной подготовке к ЕГЭ (ЕРЭ) по химии 2022
Инструкция по самостоятельной подготовке к ЕГЭ (ЕРЭ) по химии 2022 Бер нигезле чикле карбон кислоталары
Бер нигезле чикле карбон кислоталары Составление уравнений окислительно-восстановительных реакций
Составление уравнений окислительно-восстановительных реакций Алкадиены
Алкадиены Аминокислоты. Пептиды. Белки. Тема 2
Аминокислоты. Пептиды. Белки. Тема 2 Презентация по Химии "Строении атомов. Химическая связь"
Презентация по Химии "Строении атомов. Химическая связь"  Периодическая система Д.И.Менделеева
Периодическая система Д.И.Менделеева Электролитическая диссоциация
Электролитическая диссоциация Получение и свойства полиэтилена
Получение и свойства полиэтилена Строение атома
Строение атома Прогнозирование возможности и направления протекания самопроизвольных процессов
Прогнозирование возможности и направления протекания самопроизвольных процессов rastvory_-_kopia
rastvory_-_kopia Технологические процессы получения кислорода
Технологические процессы получения кислорода