Содержание
- 2. CH3COOH ↔ CH3COO- + H+ Kдисс = [CH3COO-][H+] / [CH3COOH] C0 = [CH3COO-] + [CH3COOH] α
- 3. Сильные: α > 0.3 Ka>10-1 Средние: 0.03 Слабые: α Сила электролитов Активность — «эффективная» концентрация a
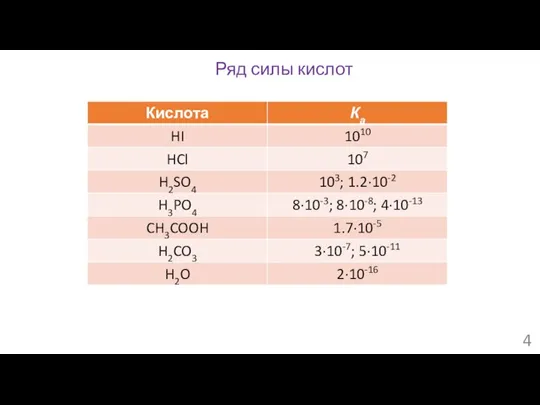
- 4. Ряд силы кислот
- 5. Кислотность воды и растворов H2O ↔ OH- + H+ Kдисс = [OH-]∙[H+] / [H2O] Ионное произведение
- 6. Задача Рассчитать рН 0.1М раствора масляной (одноосновной) кислоты, если её степень диссоциации равна 1.5%.
- 7. Задача Рассчитать рН 0.1М раствора масляной (одноосновной) кислоты, если её степень диссоциации равна 1.5%. НА ↔
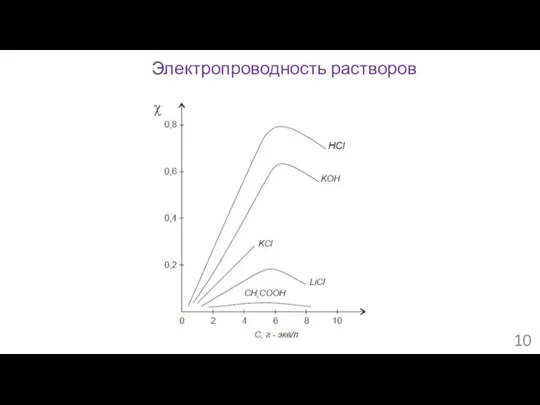
- 9. Электропроводность растворов Закон Ома: I = U/R Сопротивление проводника: R = ρ∙L/S Проводимость 1/R = 1/ρ
- 10. Электропроводность растворов
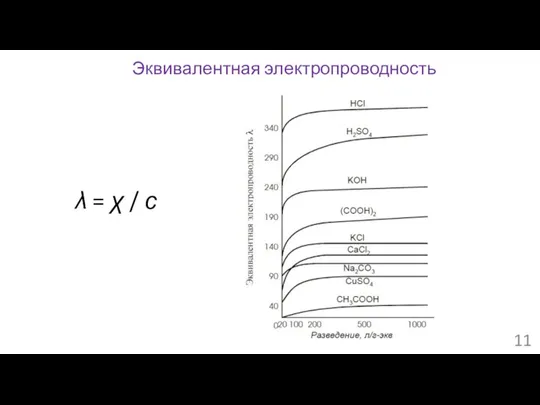
- 11. Эквивалентная электропроводность λ = χ / с
- 12. λ∞ = λ+ + λ- α = λ/ λ∞ Эквивалентная электропроводность и подвижность ионов
- 13. Аномальная подвижность H+ и OH- эстафетный механизм
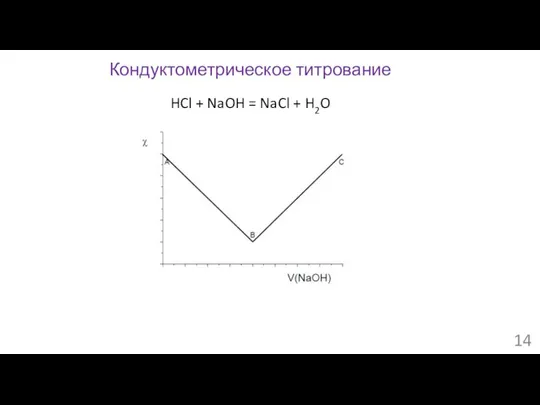
- 14. Кондуктометрическое титрование HCl + NaOH = NaCl + H2O
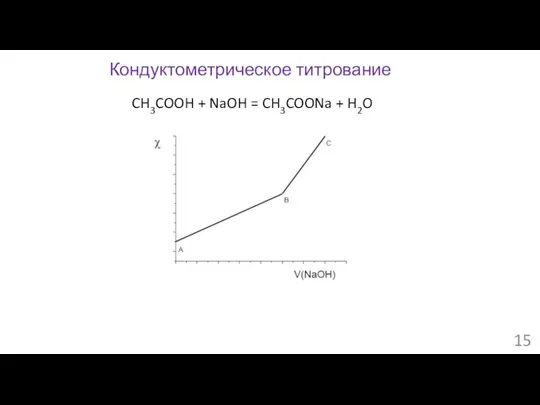
- 15. Кондуктометрическое титрование CH3COOH + NaOH = CH3COONa + H2O
- 16. Гальванический элемент
- 17. Гальванический элемент
- 18. Гальванический элемент
- 19. Стандартные потенциалы Е0
- 20. ЕХC = ЕAg,0 + (0.059/1)∙log(aAg+) = 0.222 В Хлорсеребряный электрод Ag | AgCl | KClнасыщ. AgCl
- 21. ЕХГ = ЕХГ,0 + (0.059/2)∙log(aх∙а2Н2/агх) = = ЕХГ,0 - 0.059∙pH Определение рН
- 22. Задача ЭДС гальванического элемента, состоящего из хлорсеребряного и хингидронного электродов, равна 0.32 Вольт. Найти рН хингидронного
- 24. Скачать презентацию
![CH3COOH ↔ CH3COO- + H+ Kдисс = [CH3COO-][H+] / [CH3COOH] C0 =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1110452/slide-1.jpg)

![Кислотность воды и растворов H2O ↔ OH- + H+ Kдисс = [OH-]∙[H+]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1110452/slide-4.jpg)













 Вымораживание воды
Вымораживание воды Галогены. Свойства фтора, брома, йода
Галогены. Свойства фтора, брома, йода Железо как химический элемент
Железо как химический элемент Углеводы
Углеводы Презентация на тему Электролитическая диссоциация (8 класс)
Презентация на тему Электролитическая диссоциация (8 класс)  Алюминий и сплавы алюминия
Алюминий и сплавы алюминия Периодический закон Д.И. Менделеева
Периодический закон Д.И. Менделеева Презентация на тему Палладий
Презентация на тему Палладий  Коллоидно-химическая теория схватывания и твердения вяжущих веществ
Коллоидно-химическая теория схватывания и твердения вяжущих веществ Новейшие достижения в области высокомолекулярных соединений
Новейшие достижения в области высокомолекулярных соединений Углерод и его свойства
Углерод и его свойства Презентация на тему Химические волокна
Презентация на тему Химические волокна  Соединения алюминия
Соединения алюминия Ресурс Лови оксиды для систематизации знаний, умений, навыков по теме Оксиды
Ресурс Лови оксиды для систематизации знаний, умений, навыков по теме Оксиды Электролиз
Электролиз Превращения веществ
Превращения веществ Периодическая система химических элементов. Периоды. Группы
Периодическая система химических элементов. Периоды. Группы Знаки химических элементов
Знаки химических элементов Химическая кинетика. Экзаменационные вопросы
Химическая кинетика. Экзаменационные вопросы СПИРТЫ, ФЕНОЛЫ
СПИРТЫ, ФЕНОЛЫ Презентация на тему Общая характеристика неметаллов
Презентация на тему Общая характеристика неметаллов  Методы защиты металлов от электрохимической коррозии. Классификация методов защиты
Методы защиты металлов от электрохимической коррозии. Классификация методов защиты Презентация на тему Спирты (9 класс)
Презентация на тему Спирты (9 класс)  Процесс образования неметаллических включений в стали
Процесс образования неметаллических включений в стали Многообразие веществ
Многообразие веществ Биосинтез пиримидиновых нуклеотидов
Биосинтез пиримидиновых нуклеотидов Химические свойства основных оксидов. 9 класс
Химические свойства основных оксидов. 9 класс Предельные углеводороды (алканы)
Предельные углеводороды (алканы)