Содержание
- 2. Повторение: Состав высшего оксида, его характер (основный, кислотный, амфотерный). Какая химическая связь в оксиде и тип
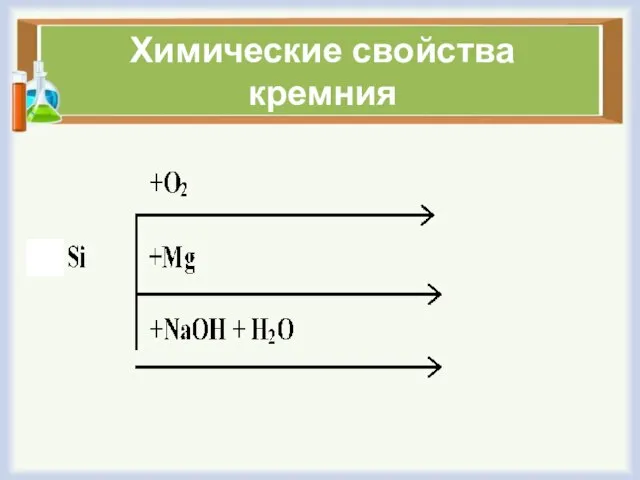
- 3. Химические свойства кремния
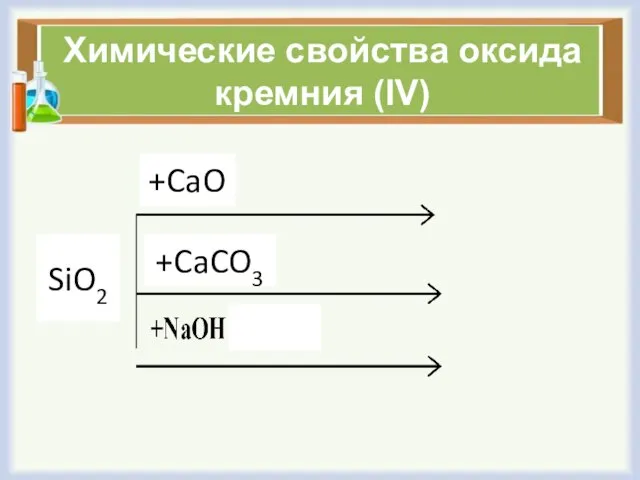
- 4. Химические свойства оксида кремния (IV) SiO2 +CaO +CaCO3
- 5. Жила в стране химии чудная дева. В семействе кислот прослыла неумелой. Была она, в общем, на
- 6. Жила в стране химии чудная дева. В семействе кислот прослыла неумелой. Была она, в общем, на
- 7. Кремневая кислота и ее соли 9 класс
- 8. Кремниевая кислота Дайте характеристику кислоте по плану: Формула Кислородсодержащая или бескислородная Сильная или слабая Одноосновная, двухосновная
- 9. Кремниевая кислота Дайте характеристику кислоте по плану: Формула H2SiO3 Кислородсодержащая или бескислородная Сильная или слабая Одноосновная,
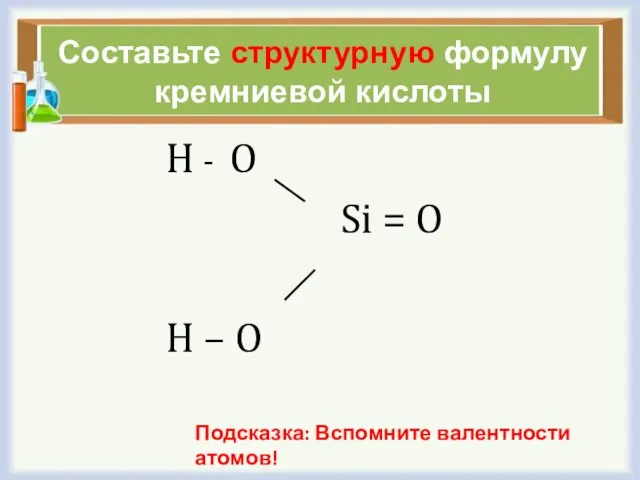
- 10. Составьте структурную формулу кремниевой кислоты H - O Si = O H – O Подсказка: Вспомните
- 11. Получение Нельзя получить реакцией оксида кремния с водой! Предложите способ получения кремниевой кислоты.
- 12. Получение Na2Si03 + H2S04 = Na2S04 + H2Si03↓ Запишите сокращенное ионное уравнение. Сделайте вывод. ВЫВОД: кремниевую
- 13. Свойства Физические в воде нерастворима прозрачное студневидное вещество ( другое название - гель.) Химические свойства характерные
- 14. Химические свойства: H2SiO3 => H2O + SiO2 H2SiO3 + 2NaOH => Na2SiO3 + 2H2O
- 15. Применение: Гель кремниевой кислоты можно высушить, он при этом приобретает пористое строение с большой внутренней поверхностью,
- 16. Силикаты - соли кремниевой кислоты Исследуем растворимость солей по таблице растворимости К растворимым относятся K2Si03 и
- 17. Свойства солей: Запишите уравнения реакций, характеризующие химические свойства силикатов. Укажите качественную реакцию для силикатов.
- 18. Нахождение в природе Силикаты широко распространены в природе. Как было отмечено ранее, земная кора в основном
- 19. Силикат натрия Силикат меди Топаз Силикат марганца Силикат алюминия
- 20. Первичное закрепление: 1.Кремниевая кислота обладает следующими свойствами а) Изменяет окраску индикаторов, взаимодействует с металлами б) Не
- 22. Скачать презентацию
















 Полезные ископаемые
Полезные ископаемые Альдегиды
Альдегиды Неметаллы. Обобщение и систематизация знаний
Неметаллы. Обобщение и систематизация знаний Презентация на тему Сахароза
Презентация на тему Сахароза  Скорость химических реакций
Скорость химических реакций Алканы. Зачетная работа
Алканы. Зачетная работа Презентация на тему Химия в криминалистике
Презентация на тему Химия в криминалистике  Алкены. Олефины, этиленовые углеводороды. (Лекция 5)
Алкены. Олефины, этиленовые углеводороды. (Лекция 5) 897386 (2)
897386 (2) Презентация по Химии "Биотрансформация чужеродных соединений в организме"
Презентация по Химии "Биотрансформация чужеродных соединений в организме"  Химические равновесия в растворах. Лекция 2. Часть 1
Химические равновесия в растворах. Лекция 2. Часть 1 Соляная кислота
Соляная кислота Химическое равновесие
Химическое равновесие Методология пробoотбора с использованием ТЧЭ
Методология пробoотбора с использованием ТЧЭ Аргументы к апелляции на ЕГЭ по химии 2021
Аргументы к апелляции на ЕГЭ по химии 2021 Метаморфизм
Метаморфизм Химия и география. Викторина
Химия и география. Викторина Алканы и алкены
Алканы и алкены Комментарии к выполненным заданиям по темам растворы и электролитическая диссоциация. 8 класс
Комментарии к выполненным заданиям по темам растворы и электролитическая диссоциация. 8 класс Алканы. Строение. Изомерия и номенклатура
Алканы. Строение. Изомерия и номенклатура Окислительно-восстановительные реакции (ОВР)
Окислительно-восстановительные реакции (ОВР) Природные источники углеводородов
Природные источники углеводородов Строение и физические свойства металлов
Строение и физические свойства металлов Физические свойства металлов
Физические свойства металлов Презентация на тему Викторина "Узнай химический элемент"
Презентация на тему Викторина "Узнай химический элемент"  Нитраты
Нитраты Прикладная геохимия
Прикладная геохимия Классификация силикатов
Классификация силикатов