Содержание
- 2. Задачи: Обучающая: опираясь на знания учащихся об основных классах неорганических веществ, подвести их к понятию «связь
- 3. Металлы Металлический блеск Ковкость Высокая теплопроводность Высокая электропроводность Образуют основные оксиды
- 4. Неметаллы Разноцветные Изоляторы Три агрегатных состояния Образуют кислотные оксиды
- 5. Распределить данные вещества по классам: MgO, SO2 , S, H2SO3, SO3, Mg, MgCl2, Mg(OH)2, NaOH, Na2SO4,
- 6. Химические элементы: S, Mg Оксиды: SO2, SO3,MgO Кислоты: H2SO3, HCl Основания: Mg(OH)2, NaOH Соли: MgCl2, Na2SO3
- 7. Практическая работа Цель: закрепить теоретические знания практическими навыками
- 8. 1. Ca CaO Ca(OH)2 CaSO4 2. Mg MgO Mg(OH)2 MgCl2 3. S SO2 H2SO3 Na2SO3 4.
- 9. Возможны ли обратные цепочки превращений?
- 10. 1 вариант: С какими из перечисленных веществ вступает в реакцию соляная кислота: оксид серы (6), оксид
- 11. Домашнее задание: параграф 42, напишите уравнения реакций получения хлорида железа (2) с помощью 4-5 различных реакций.
- 13. Скачать презентацию










 Презентация на тему Спирты (9 класс)
Презентация на тему Спирты (9 класс)  Гетерогенные дисперсные системы
Гетерогенные дисперсные системы Наука Химия на Великой Отечественной войне
Наука Химия на Великой Отечественной войне Электрохимическая коррозия
Электрохимическая коррозия Презентация на тему Общая характеристика металлов главных подгрупп I-III
Презентация на тему Общая характеристика металлов главных подгрупп I-III  Принципы строения молекулы дезоксирибонуклеиновой кислоты: комплементарность нуклеотидов
Принципы строения молекулы дезоксирибонуклеиновой кислоты: комплементарность нуклеотидов Оценка возможности повышения эффективности процесса гидрирования бутилен- бутадиеновой фракции
Оценка возможности повышения эффективности процесса гидрирования бутилен- бутадиеновой фракции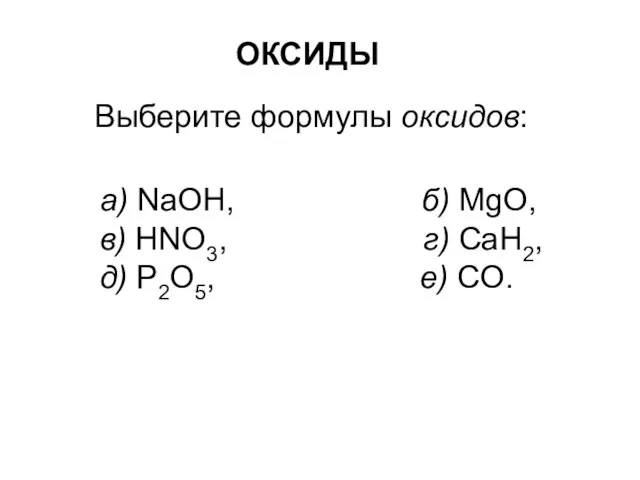 Оксиды
Оксиды Классификация и номенклатура ОС
Классификация и номенклатура ОС Значимые личности в химии
Значимые личности в химии Презентация на тему Факторы, влияющие на скорость химической реакции
Презентация на тему Факторы, влияющие на скорость химической реакции  Железо в организме человека. Функции железа в организме
Железо в организме человека. Функции железа в организме Окислительно- восстановительные реакции
Окислительно- восстановительные реакции Условия хранения и подготовка скоропортящихся грузов к перевозкам
Условия хранения и подготовка скоропортящихся грузов к перевозкам 4_10.1С Аммиак, производство и применение_Презентация
4_10.1С Аммиак, производство и применение_Презентация Валентность
Валентность Каучук негізіндегі материалдар
Каучук негізіндегі материалдар ИКТ как средство реализации проблемного обучения на уроках химии
ИКТ как средство реализации проблемного обучения на уроках химии Полисахариды. Крахмал и целлюлоза
Полисахариды. Крахмал и целлюлоза Dereglarea metabolismului
Dereglarea metabolismului Физическая химия, термодинамика
Физическая химия, термодинамика Пусть имя Д.И. Менделеева будет нашей путеводной звездой
Пусть имя Д.И. Менделеева будет нашей путеводной звездой Подготовка к контрольной работе. 8 класс
Подготовка к контрольной работе. 8 класс Электролитическая диссоциация. 8 класс
Электролитическая диссоциация. 8 класс Открытый урок на тему: Степень окисления
Открытый урок на тему: Степень окисления Амины. Номенклатура аминов
Амины. Номенклатура аминов Химический алфавит. Алфавит
Химический алфавит. Алфавит Органические вещества
Органические вещества