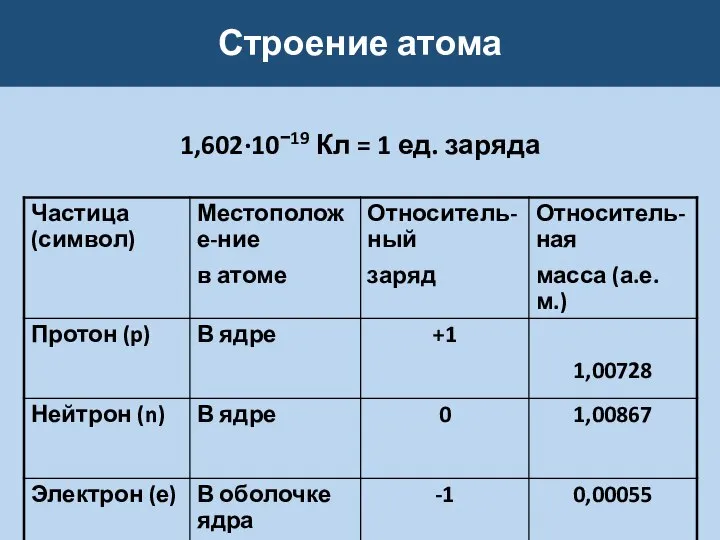
Слайд 2Строение атома
1,602·10−19 Кл = 1 ед. заряда
Слайд 3Строение атома
Атомы одного и того же элемента, имеющие одинаковый заряд ядра, но

различное число нейтронов в ядре (N), называются изотопами.
Например, изотопами элемента кальция являются 4020Ca (20p + 20n), 4220Ca (20p+22n) и 4320Ca (20p+23 n).
Слайд 4Строение атома
Сумму протонов (Z) и нейтронов (N), содержащихся в ядре атома, называют

массовым числом (А).
Нижний индекс обозначает число протонов (Z), а разность между ними равна числу нейтронов
N = A − Z.
Слайд 5Строение атома
В основе квантовой теории электронного строения атома лежат следующие экспериментальные данные.
1.

Спектры атомов.
Атомные спектры многих элементов имеют очень сложную структуру. Атом может находиться в нескольких (многих) энергетических состояниях, но они не непрерывны, а прерывисты, то есть квантованы.
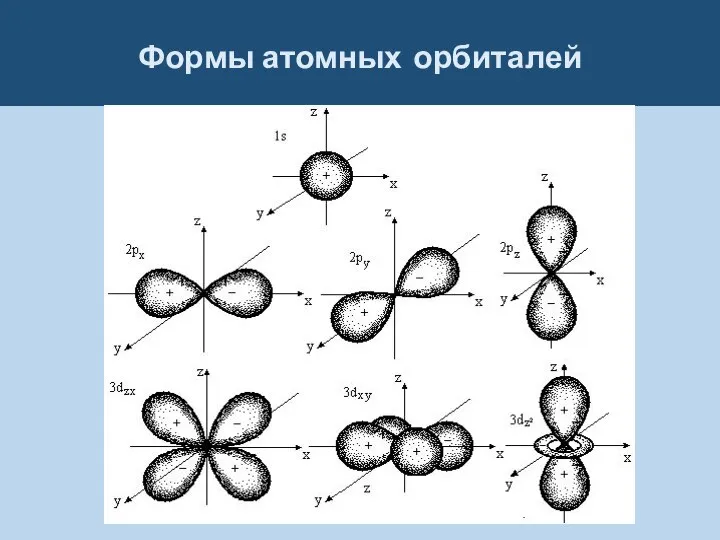
Атомная орбиталь (АО) – область атомного пространства, в которой движется электрон. Форму АО характеризуют линиями и поверхностями с одинаковым значением ψ2, которую называют плотностью электронного облака.
Слайд 6Строение атома
2. Квантовые числа
Главное квантовое число (n) характеризует энергию электрона на данном

энергетическом уровне, определяет размеры атомной орбитали, используется как номер энергетического уровня
Главное квантовое число имеет значения от 1 до ∞ (n = 1, 2, 3, 4... ∞). Иногда энергетические уровни обозначают буквами K, L, M, N.., которые соответствуют численным значениям 1, 2, 3, 4….
Чем меньше n, тем больше энергия взаимодействия электрона с ядром.
Слайд 7Строение атома
Орбитальное квантовое число (l) определяет форму атомной орбитали и принимает значения

от 0 до (n-1), то есть n значений.
Орбитальное квантовое число принято обозначать буквенными символами:
l = 0 1 2 3 4
s p d f g
Каждому значению l соответствует орбиталь определенной формы.
Слайд 9Строение атома
Магнитное квантовое число (m) − характеризует пространственную ориентацию орбитали. Оно зависит

от орбитального квантового числа и принимает значения от –l до нуля и от нуля до +l.
Например, если орбитальное квантовое число равно 0 (s-орбиталь), то магнитное квантовое число имеет одно значение (0), если орбитальное квантовое число равно 1 (р-орбиталь), то магнитное квантовое число имеет три значения: –1, 0 и +1, а если орбитальное квантовое число равно 2 (d-орбиталь), то магнитное квантовое число имеет пять значений: –2, –1, 0, +1 и +2 и т.д. Таким образом, для каждого значения l имеется (2l + 1) значений m.
Слайд 10Строение атома
Дополнительное четвертое квантовое число − спиновое (s) ("spin" − вращение, веретено)

− характеризует собственный механический момент движения электрона, которое условно представляют как вращение вокруг собственной оси.
Оно может происходить в двух взаимно противоположных направлениях.
Поэтому спиновое квантовое число имеет только два значения: +1/2 и − 1/2.
Слайд 11Заполнение атомных орбиталей электронами в многоэлектронном атоме
Принцип наименьшей энергии.
Электроны в атоме распределяются

по орбиталям таким образом, что энергия атома оказывается наименьшей.
Первое правило Клечковского:
1) энергия электрона в основном определяется значениями главного (n) и орбитального (l) квантовых чисел, поэтому сначала электронами заполняются те подуровни, для которых сумма (n + l) меньше.
Слайд 12Заполнение атомных орбиталей электронами в многоэлектронном атоме
Второе правило Клечковского:
В случае, если сумма

(n + l) для двух подуровней одинакова (например, для 3d- и 4p-подуровней эта сумма равна 5), сначала заполняется электронами уровень с меньшим n.
С учетом правил Клечковского энергия атомных орбиталей возрастает согласно ряду
1s < 2s < 2p < 3 < 3p < 4s ≤ 3d < 4p < 5s ≤ 4d < 5p < 6s ≤ 4f ≤ 5d < 6p < 7s ≤ 5f ≤ 6d < 7p
Слайд 13Заполнение атомных орбиталей электронами в многоэлектронном атоме
Принцип Паули определяет емкость АО: в

атоме не может быть двух электронов с одинаковым набором всех четырех квантовых чисел.
Таким образом, на одной АО, характеризуемой тремя квантовыми числами, может разместиться только два электрона с противоположными спинами
Слайд 14Заполнение атомных орбиталей электронами в многоэлектронном атоме
Принцип Паули и взаимозависимость между значениями

n, l, и m определяют максимально возможное количество электронов на орбитали, подуровне и уровне (табл. 2.4):
− на одной АО − 2 электрона;
− на подуровне l − 2(2l+1) электрона;
− на уровне n − 2n2 электронов.
Слайд 15Заполнение атомных орбиталей электронами в многоэлектронном атоме
Два правила Хунда описывают порядок заполнения

электронами АО одного подуровня:
Первое правило Хунда: в данном подуровне электроны стремятся заполнять энергетические состояния (АО) таким образом, чтобы сумма их спинов по абсолютной величине была максимальна. При этом энергия системы минимальна.
Слайд 16Заполнение атомных орбиталей электронами в многоэлектронном атоме
Электронная конфигурация атома углерода.
Атомный номер
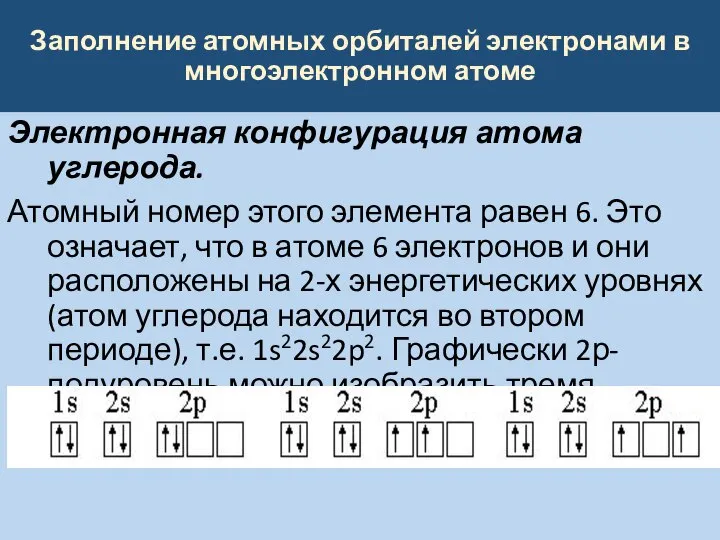
этого элемента равен 6. Это означает, что в атоме 6 электронов и они расположены на 2-х энергетических уровнях (атом углерода находится во втором периоде), т.е. 1s22s22p2. Графически 2р-подуровень можно изобразить тремя способами:
Слайд 17Заполнение атомных орбиталей электронами в многоэлектронном атоме
Второе правило Хунда:
минимальной энергией

обладает состояние с максимальной (по абсолютной величине) суммой магнитных квантовых чисел.
В соответствии с правилом Хунда, преимуществом обладает вариант б (сумма |1+ 0| равна 1) , так как в варианте в сумма |+1–1| равна 0.
Слайд 18Заполнение атомных орбиталей электронами в многоэлектронном атоме
Определим электронную формулу элемента ванадия (V).

Так как его атомный номер Z = 23, то нужно разместить на подуровнях и уровнях (их четыре, так как ванадий находится в четвертом периоде) 23 электрона. Последовательно заполняем: 1s22s22p63s23p64s23d3 (подчеркнуты незаконченные уровни и подуровни).
Для селена (Z = 34) полная электронная формула: 1s22s22p63s23p63d104s24p4, незаконченным является четвёртый уровень.
Слайд 19Периодическая система и изменение свойств элементов
Свойства элементов, а также формы и

свойства соединений элементов находятся в периодической зависимости от заряда ядра. (1869 г)
Слайд 20Периодическая система и изменение свойств элементов
Период соответствует постепенному заполнению электронами электронного уровня,

характеризуемого главным квантовым числом n (равным номеру периода).
Периоды состоят из семейств s-, р-, d-, f-элементов.
Периоды располагают в параллельных строках так, чтобы элементы с одинаковым строением (одинаковые l и число электронов внешних подуровней nвэ) располагались друг под другом, образуя группы и подгруппы.
Слайд 21Периодическая система и изменение свойств элементов
В соответствии с числом электронов на внешнем

уровне элементы подразделяются на группы.
Группы состоят из главных и побочных подгрупп. Отличие элементов главных и побочных подгрупп состоит в том, что в главных подгруппах элементы имеют валентные s- и р-электроны, а в побочных − d - и f-электроны.
Соответственно, элементы, имеющие в качестве валентных электронов только s-электроны, называют s-элементами (например, Li − ...2s1, Ca − ...4s2).
Слайд 22Устойчивость орбитальных электронных конфигураций
Нарушения заполнения электронов в атоме объясняются особой устойчивостью некоторых

электронных конфигураций. Качественно можно сформулировать следующие закономерности:
1) при заполнении уровня и подуровня устойчивость электронной конфигурации возрастает и
2) особой устойчивостью обладают заполненные (s2, p6, d10, f14) и наполовину заполненные (p3, d5, f7) конфигурации.
Слайд 23Устойчивость орбитальных электронных конфигураций
Такие отклонения имеют место во многих случаях:
для d-элементов: Cr,

Cu, Nb, Mo, Ru, Rh, Pd, Ag, Pt, Au;
для f-элементов: La, Gd, Ac, Th, Pa, U, Cm.
Слайд 24Изменение свойств элементов в Периодической системе
Орбитальные конфигурации и первые энергии ионизации атомов.

Энергия, необходимая для отрыва электрона от атома называется энергией ионизации (I)
Э + I1 → Э+ + ē.
Отрыву первого электрона соответствует первая энергия ионизации I1 , второго – вторая I2 и т.д.
Энергию ионизации выражают либо в кДж/моль, либо в электронвольтах (эВ).
Слайд 25Изменение свойств элементов в Периодической системе
Сродство к электрону и электроотрицательность.
Энергия, которая

выделяется при присоединении электрона к атому, называется сродством к электрону (Eср) (кДж/моль или эВ).
Э0 + е = Э− + Еср .
Величина Еср ,очевидно, равна по величине и обратна по знаку энергии ионизации отрицательно заряженного атома
Слайд 26Изменение свойств элементов в Периодической системе
Электроотрицательность (ЭО).
Согласно Полингу, "электроотрицательность есть способность

атома в молекуле или сложном ионе притягивать к себе электроны, участвующие в образовании связи".
Слайд 27Изменение свойств элементов в Периодической системе
Атомные и ионные радиусы
Эффективные радиусы -

условные величины, определяемые в соответствии с каким-либо принципом или условием. Так, например, в качестве орбитальных радиусов атомов принимают расстояние от ядра до последнего максимума электронной плотности.
Размеры ионов (ионные радиусы) находят делением в определенной пропорции расстояния между ионами в ионных соединениях.
Слайд 29Основные характеристики химической связи
Химическая связь − это понижение энергии атомов при образовании

молекулы или СЕ.
Энергия химической связи может быть определена как энергия, необходимая для разрыва этой связи.
Для двухатомной молекулы она равна энергии (энтальпии) диссоциации, например:
Н2 = 2Н, ΔН0 = Ен-н = 432 кДж.
Слайд 30Свойства химической связи
Насыщаемость – это особое свойство химической связи: атом в молекуле

или структурной единице (СЕ) обладает определенной валентностью и он может иметь небольшое число валентностей.
Вещества обладают определенными оптическими (цвет, спектры), электрическими (дипольный момент, заряды на атомах) и магнитными свойствами, которые должны быть объяснены с точки зрения их строения.
Слайд 31В случае многоатомных молекул энергия связи зависит от состояния реагентов и продуктов.

Поэтому энергии последовательного разрыва одинаковых связей не равны между собой.
Химические связи между одними и теми же атомами в разных молекулах примерно одинаковы, если атомы находятся в одинаковых валентных состояниях.
Под валентным состоянием атома понимают количество и вид химических связей, образуемых им в рассматриваемом соединении.
Слайд 32Кратность связи
Энергии химических связей между одними и теми же двумя атомами могут

различаться примерно в 2 и 3 раза. Это привело к введению представлений об ординарных (одиночных), двойных и тройных связях
Е с-с ≈ 350,
Е с=с ≈ 600,
Е с≡с ≈ 820 кДж/моль
Слайд 33Длина связи
Длина связи равна расстоянию между центрами соседних атомов в молекуле.
Длину

связи можно приближенно определять путем сложения соответствующих радиусов атомов или ионов:
d A-B ≈ rA + rB ≈ (dA-A + dB-B ) /2
Длины связей зависят от валентного состояния атомов, то есть, например, от кратности связи: d c−c ≈ 154 пм, d c=c ≈ 134 пм и d с≡с ≈ 120 пм.
Сравнение длин связей с их энергиями показывает, что между ними существует обратная зависимость: чем больше длина, тем меньше энергия связи
Слайд 34Валентные углы
Валентные углы − углы между связями, образуемыми одним атомом в молекуле

или СЕ. Они зависят от природы атомов и характера химической связи.
Молекулы состава AB2 могут быть линейными (CO2) или угловыми (H2O), AB3 − треугольными (BF3) и пирамидальными (NH3), AB4 − тетраэдрическими (CH4), или квадратными (PtCl4)−, или пирамидальными (SbCl4)−, AB5 − тригонально-бипирамидальными (PCl5), или тетрагонально-пирамидальными (BrF5), AB6 − октаэдрическими (AlF6)3− и т.д.
Слайд 35Спектры молекул
Спектры молекул обычно представляют собой зависимость интенсивности (I) поглощения или излучения

веществом энергии (в виде фотонов, электронов или ионов) от энергии внешнего воздействия на вещество.
Слайд 36Магнитные свойства
Существует два основных типа взаимодействия вещества с магнитным полем.
1. Парамагнитное взаимодействие

− атомы и молекулы вещества имеют неспаренные электроны, вещество намагничивается в магнитном поле и втягивается между полюсами магнита.
2. Диамагнитное взаимодействие − в атомах и молекулах вещества все электроны спарены, магнитные моменты скомпенсированы, вещество не намагничивается, но испытывает слабое отталкивание из межполюсного пространства.
Слайд 37Магнитные свойства
К парамагнитным веществам относятся все атомы (Li, B, N, F и

т.д.), а также молекулы (NO, NO2, CO+, N2+, [Fe(H2O)6]3+) с нечетным числом электронов.
Некоторые молекулы и вещества, имеющие четное число электронов, также парамагнитны (O2, F22+, [Fe(H2O)6]2+ и т.д.)
Слайд 38Современные теории химических связей.
Общие принципы квантово-механических теорий
Применяют два подхода к анализу химических

связей.
1) В методе валентных связей (ВС) вначале рассматриваются взаимодействия только между парами атомов. Химические связи в молекуле представляются как совокупность локализованных связей.
2) В методе молекулярных орбиталей (МО) рассматривается распределение электронной плотности между всеми ядрами, а молекулярные орбитали охватывают все ядра, то есть в методе МО связи изначально делокализованы
Слайд 39Теория валентных связей
Химическая связь, образованная путем обобществления пары электронов двумя атомами,

называется ковалентной.
По мере сближения атомов, их электроны начинают притягиваться не только ядром своего атома, но и ядром другого атома. Атомные орбитали начинают перекрываться, и появляется вероятность одновременного появления обоих электронов в области перекрывания.
Слайд 40Представление о донорно-акцепторной связи
В случае молекулы СО донорно-акцепторная связь образуется за счет

электронной пары валентной оболочки атома кислорода и пустой АО атома углерода. Атом кислорода при этом называют донором, а углерода − акцептором электронной пары.
Слайд 41Основные свойства ковалентной связи – насыщаемость и направленность
Из рассмотренных выше механизмов

образования связи следует, что с точки зрения метода ВС максимально возможное число ковалентных связей (максимальная ковалентность) определяется не только числом валентных электронов, но и общим числом валентных орбиталей.
Ограничение числа химических связей атома, вызванное ограниченным числом валентных электронов и орбиталей, называют насыщаемостью ковалентной химической связи.
Слайд 42Основные свойства ковалентной связи – насыщаемость и направленность
Направленность химической связи определяется направленностью

в пространстве всех АО с l > 0.
Так как лепестки р-орбиталей расположены под углом 1800, а сами px-, py- и pz-АО расположены под углами 900, то следует ожидать, что такие углы будут и в молекулах.
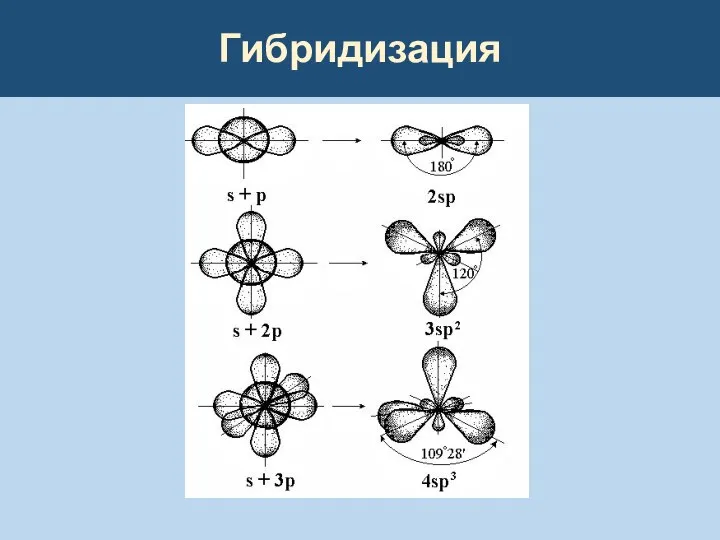
Для объяснения углов между связями введено представление о гибридизации атомных орбиталей, то есть о перемешивании орбиталей с различными орбитальными квантовыми числами с получением гибридных (смешанных) АО.
Слайд 43Гибридизация
sp − линейная (1800),
sp2 − треугольная (1200),
sp3 − тетраэдрическая

(109028').
sp3d2 − октаэдрическая (900),
sp3d − треугольно-бипирамидальная (90 и 1200),
sp2d − квадратная ( 90 и 1800)
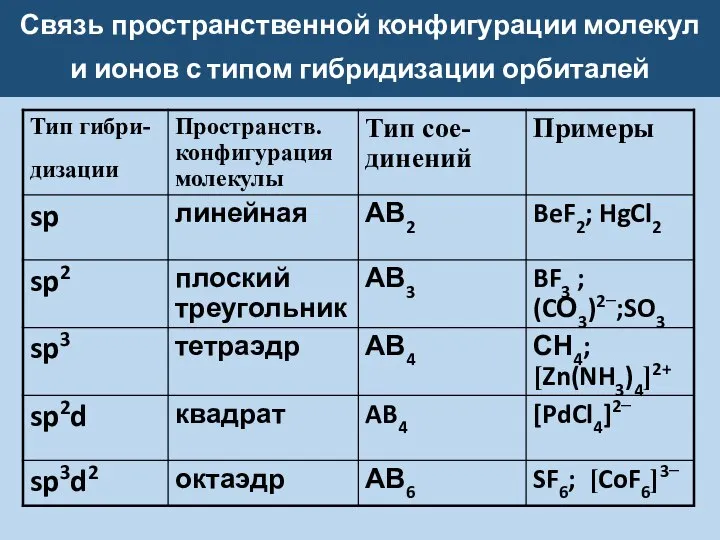
Слайд 45Связь пространственной конфигурации молекул
и ионов с типом гибридизации орбиталей
Слайд 46σ-связями (перекрыванием) называют связи (перекрывание), образующиеся при перекрывании АО, имеющих цилиндрическую симметрию
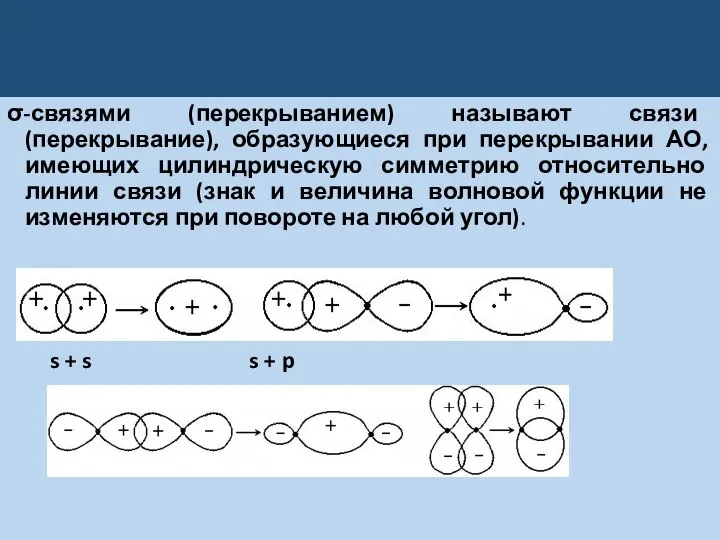
относительно линии связи (знак и величина волновой функции не изменяются при повороте на любой угол).
s + s s + p
Слайд 47Между двумя атомами, в соответствие с рассматриваемым методом ВС, может быть только

одна связь σ-типа.
π-связью (перекрыванием) называют связь, образующуюся при перекрывании облаков, имеющих плоскость симметрии, но не имеющих цилиндрической симметрии. В этом случае электронные плотности располагаются вне линии связи с двух ее сторон; таких связей между двумя атомами может быть несколько.
Слайд 48Энергия, кратность и длина связи
Чем больше кратность, тем меньше длина и больше

энергия связи; при одинаковой кратности − чем меньше длина, тем больше энергия связи.













































 Типы химических реакций
Типы химических реакций Переваривание и всасывание жиров
Переваривание и всасывание жиров Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Вода – самое удивительное вещество на Земле
Вода – самое удивительное вещество на Земле Химия природная или синтетическая. За и против
Химия природная или синтетическая. За и против Основные классы неорганических соединений
Основные классы неорганических соединений Химия в космосе Автор: Гриб Яна ученица 8а класса школа №484. Научный руководитель: Бирюкова Зоя Владимировна.
Химия в космосе Автор: Гриб Яна ученица 8а класса школа №484. Научный руководитель: Бирюкова Зоя Владимировна. Электролиз (катод)
Электролиз (катод) Строение углеводородов
Строение углеводородов Общая характеристика элементов группы, главной подгруппы
Общая характеристика элементов группы, главной подгруппы Урок-путешествие по теме «Первоначальные химические понятия»
Урок-путешествие по теме «Первоначальные химические понятия» Аминокислоты. Пептиды. Белки
Аминокислоты. Пептиды. Белки Виды аккумулирования энергии
Виды аккумулирования энергии Химические методы анализа. Аналитические методы контроля в техносферной безопасности. Лекция 6
Химические методы анализа. Аналитические методы контроля в техносферной безопасности. Лекция 6 Алканы. Химические свойства, получение и особенности
Алканы. Химические свойства, получение и особенности Природные смолы: канифоль, янтарь, сандарак (2)
Природные смолы: канифоль, янтарь, сандарак (2)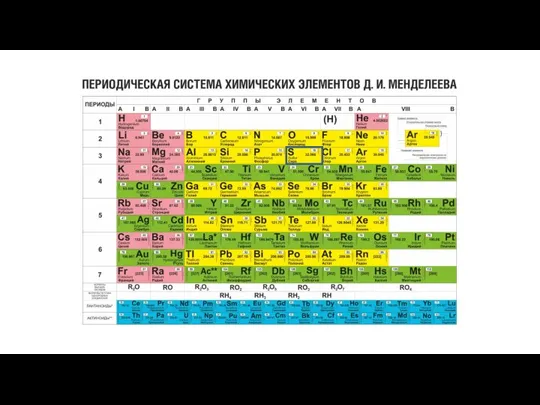 Периодическая система химических элементов Д.И. Меделеева
Периодическая система химических элементов Д.И. Меделеева Разбор 25 задания. Вебинариум
Разбор 25 задания. Вебинариум Металлы. Контрольная работа
Металлы. Контрольная работа Использование ИКТ в преподавании химии
Использование ИКТ в преподавании химии Презентация на тему Органическая химия. Жиры
Презентация на тему Органическая химия. Жиры  Гидроксикарбоновые кислоты
Гидроксикарбоновые кислоты Презентация на тему Неорганические полимеры
Презентация на тему Неорганические полимеры  Презентация на тему Теория А. М. Бутлерова
Презентация на тему Теория А. М. Бутлерова  Поляризуемость. Эллипсоид поляризуемости и симметрия молекулы
Поляризуемость. Эллипсоид поляризуемости и симметрия молекулы Галогеноводородные кислоты
Галогеноводородные кислоты Техника безопасности на уроках химии
Техника безопасности на уроках химии Презентация на тему Неметаллы. Мышьяк
Презентация на тему Неметаллы. Мышьяк