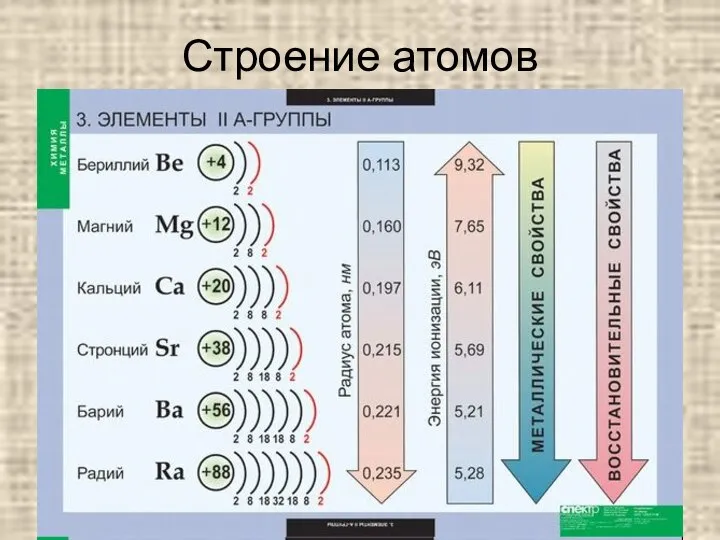
Слайд 2Строение атомов
Общая электронная формула ns2
Валентность II
Степень окисления +2
Восстановительные свойства
Менее реакционно-способны, чем щелочные

металлы
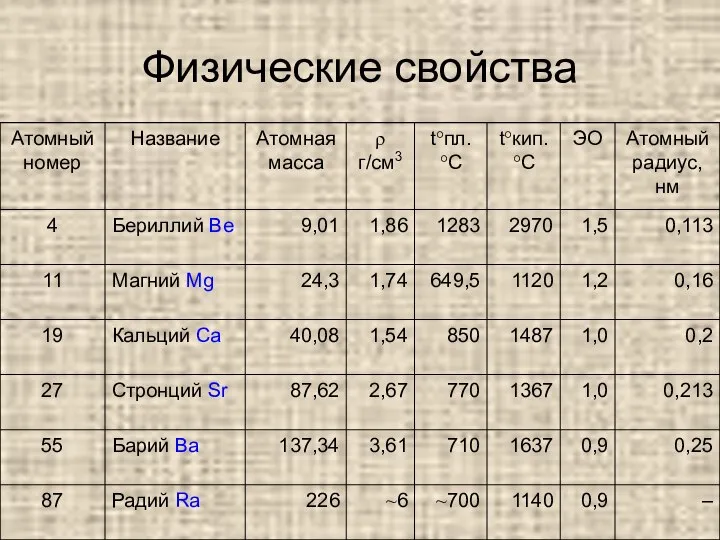
Слайд 5Физические свойства
серебристо-белые блестящие металлы, твердость значительно выше, чем у щелочных металлов.

Слайд 6Be
3BeO • Al2O3 • 6SiO2 –
берилл

Слайд 7Mg
MgCO3 – магнезит
CaCO3 • MgCO3 – доломит
KCl • MgSO4 • 3H2O –

каинит
KCl • MgCl2 • 6H2O – карналлит
Слайд 8Ca
CaCO3 – кальцит
(известняк, мрамор и др.)
Ca3(PO4)2 – апатит, фосфорит
CaSO4 • 2H2O

– гипс
CaSO4 – ангидрит
CaF2 – плавиковый шпат
(флюорит)
Слайд 9
SrSO4 – целестин
SrCO3 – стронцианит
BaSO4 – барит
BaCO3 – витерит
во всём мире удалось
добыть

всего 1,5 кг
чистого радия
Sr, Ba и Ra
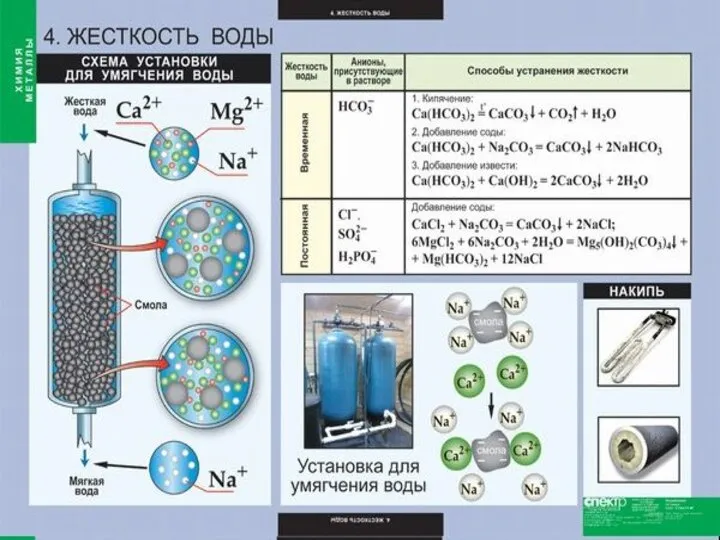
Слайд 10Химические свойства
1. Все металлы образуют оксиды RO, барий-пероксид – BaO2
2Me

+O2 → 2MeO
2. Бериллий и магний сравнительно медленно реагируют с неметаллами
Me +H2 → MeH2
Me +Cl2 → MeCl2
Me +S → MeS
Слайд 11Химические свойства
3. Растворяются в кислотах:
Me +2HCl → MeCl2 + H2

Бериллий растворяется в водных растворах щелочей
4. В обычных условиях поверхность Be и Mg покрыта инертной оксидной пленкой, поэтому они устойчивы по отношению к воде.
Ca, Sr и Ba растворяются в воде с образованием гидроксидов Me +2HOH → Me(OH)2 +Н2
Слайд 12Качественная реакция на катионы щелочноземельных металлов – окрашивание пламени в следующие цвета:
Ca2+

- темно-оранжевый
Sr2+- темно-красный
Ba2+ - светло-зеленый
Слайд 14Проверка знаний
Сравните атомы элементов, поставив знаки <, > или = вместо

*:
а) заряд ядра: Mg * Ca, Na *Mg, Ca * К;
б) число электронных слоев: Mg * Ca, Na * Mg,
Ca * К;
в) число электронов на внешнем уровне: Mg * Ca, Na *Mg, Ca * К;
г) радиус атома: Mg * Ca, Na * Mg, Ca * K;
д) восстановительные свойства: Mg * Ca,
Na * Mg, Ca * K.
Слайд 15Допишите уравнения реакций:
а) Са + H2O→ ……………………….
б) Mg + НСl→……………………….

в) Ва + О2→………………………..
Осуществить превращения по схеме:
Ме → МеО → Ме(ОН)2 → МеSО4











 Органическая химия
Органическая химия Трансляция. Активирование аминокислоты
Трансляция. Активирование аминокислоты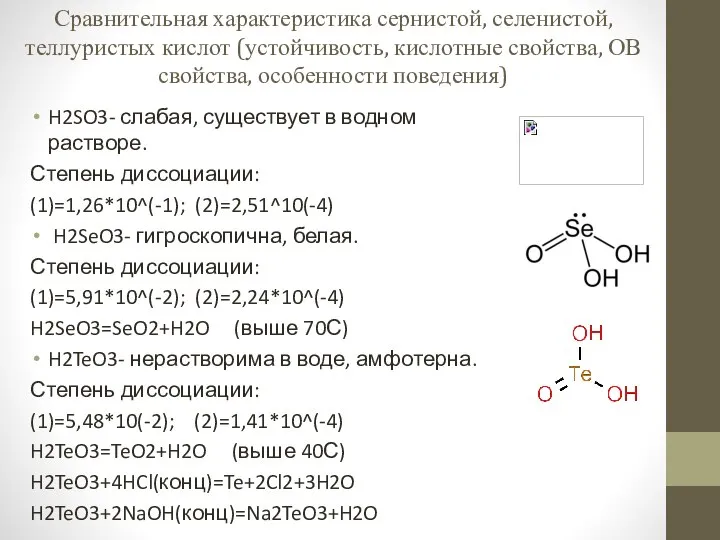 Сравнительная характеристика сернистой, селенистой, теллуристых кислот
Сравнительная характеристика сернистой, селенистой, теллуристых кислот Химические реакции
Химические реакции Кинетика и равновесие. Лекция №3
Кинетика и равновесие. Лекция №3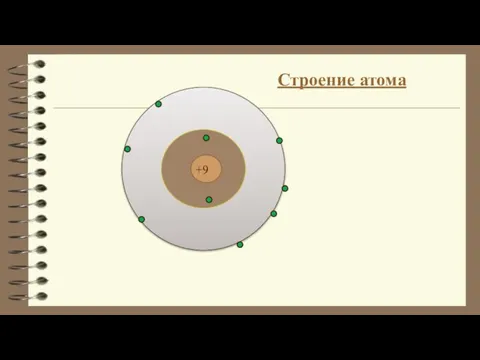 Строение атома
Строение атома Химия элементов
Химия элементов Химик белемнәрне тормышта куллану
Химик белемнәрне тормышта куллану Ацетиленди гидратациялау
Ацетиленди гидратациялау Химический элемент азот N и его соединения
Химический элемент азот N и его соединения Презентация на тему Аллотропные видоизменения неметаллов
Презентация на тему Аллотропные видоизменения неметаллов  Химическая связь
Химическая связь Основы строения и свойства материалов
Основы строения и свойства материалов Влияние бытовой химии на здоровье человека
Влияние бытовой химии на здоровье человека Нуклеиновые кислоты
Нуклеиновые кислоты Про краски
Про краски Углеродистые стали
Углеродистые стали Реакции ионного обмена и условия их протекания
Реакции ионного обмена и условия их протекания Экстракционное разделение радионуклидов
Экстракционное разделение радионуклидов Альдегиды и кетоны
Альдегиды и кетоны Осмотическое давление
Осмотическое давление Степень окисления
Степень окисления Условия среды, вызывающие коррозию металла
Условия среды, вызывающие коррозию металла Физические и химические явления в химии. Признаки химических реакций
Физические и химические явления в химии. Признаки химических реакций Химическая связь. Ковалентная связь
Химическая связь. Ковалентная связь Замедленное коксование гудрона
Замедленное коксование гудрона Структура, свойства и термическая обработка железоуглеродистых сплавов
Структура, свойства и термическая обработка железоуглеродистых сплавов Самородные металлы
Самородные металлы