Содержание
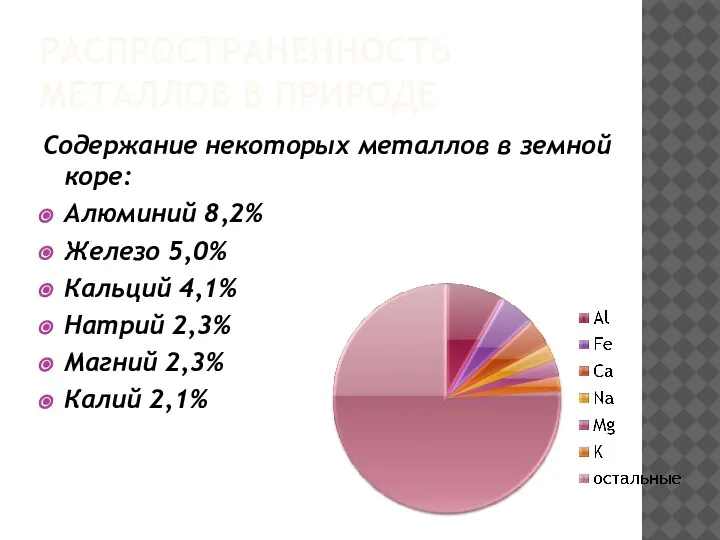
- 2. РАСПРОСТРАНЕННОСТЬ МЕТАЛЛОВ В ПРИРОДЕ Содержание некоторых металлов в земной коре: Алюминий 8,2% Железо 5,0% Кальций 4,1%
- 3. РАСПРОСТРАНЕННОСТЬ МЕТАЛЛОВ В ПРИРОДЕ Содержание некоторых металлов в морской воде: Na+ 1,05% Mg 2+ 0,12%
- 4. В ПРИРОДЕ МЕТАЛЛЫ МОГУТ ВСТРЕЧАТЬСЯ Только в свободном (самородном) виде (благородные металлы - золото, платина); В
- 10. ЧАЩЕ ВСЕГО МЕТАЛЛЫ ВСТРЕЧАЮТСЯ В ВИДЕ Солей неорганических кислот Оксидов
- 11. СУЛЬФИДЫ Галенит PbS Киноварь HgS Пирит FeS2 И др.
- 12. ХЛОРИДЫ Сильвин KCl Галит NaCl Сильвинит KCl • NaCl Карналлит KCl • MgCl2 • 6H2O И
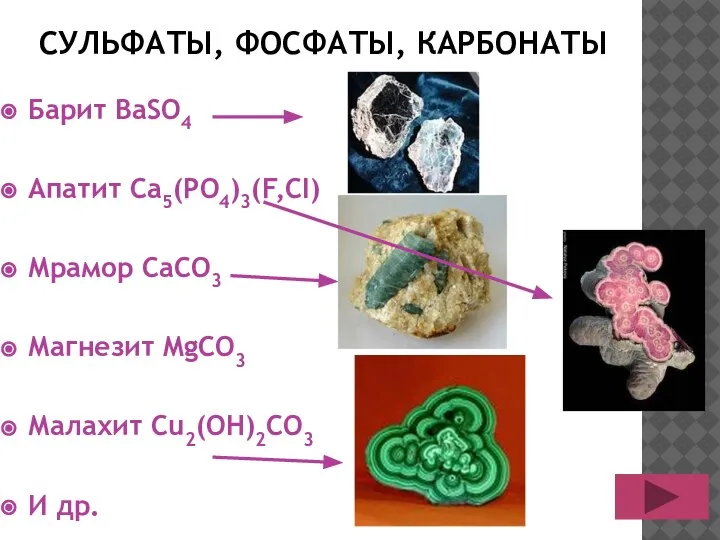
- 13. СУЛЬФАТЫ, ФОСФАТЫ, КАРБОНАТЫ Барит BaSO4 Апатит Ca5(PO4)3(F,CI) Мрамор CaCO3 Магнезит MgCO3 Малахит Cu2(OH)2CO3 И др.
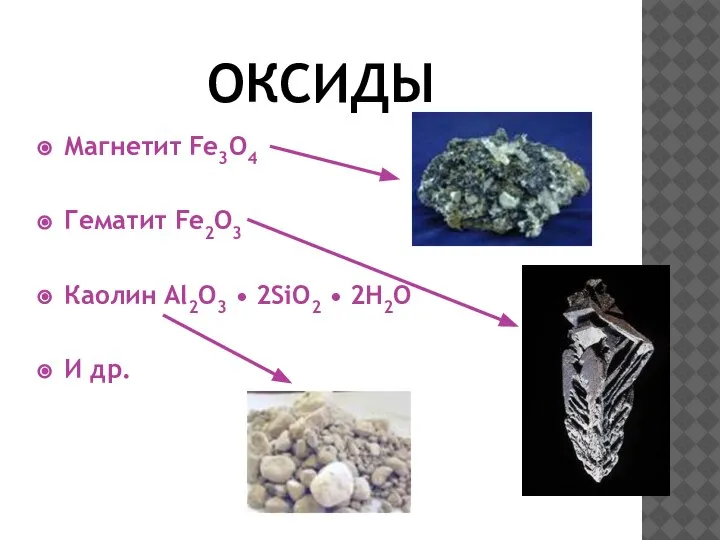
- 14. ОКСИДЫ Магнетит Fe3O4 Гематит Fe2O3 Каолин Al2O3 • 2SiO2 • 2H2O И др.
- 15. Минералы и горные породы, содержащие металлы и их соединения и пригодные для промышленного получения металлов, называются
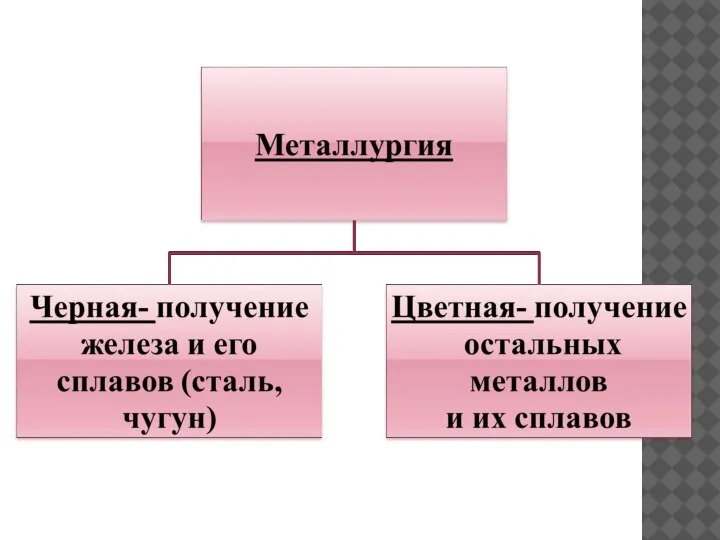
- 16. Металлургия – наука о промышленных способах получения металлов из природного сырья. Металлургия делится на три отрасли:
- 18. 1. ПИРОМЕТАЛЛУРГИЯ Восстановление металлов из руд при высоких температурах с помощью восстановителей. Соль → оксид Соли
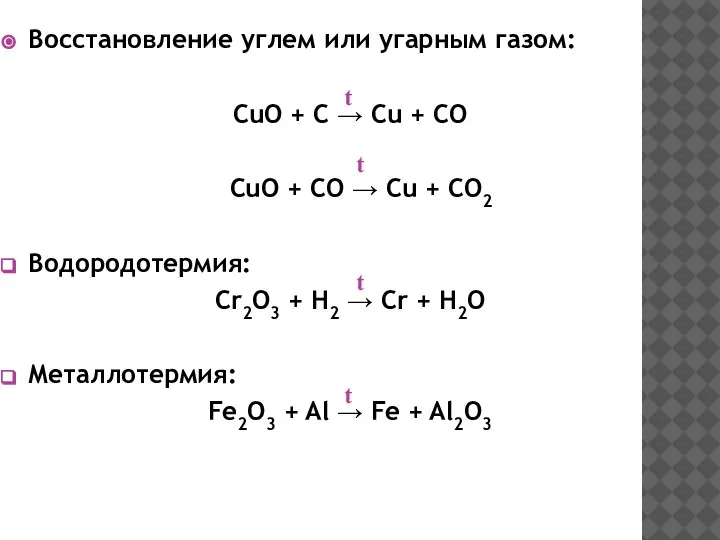
- 19. Восстановление углем или угарным газом: CuO + C → Cu + CO CuO + CO →
- 20. АЛЮМОТЕРМИЯ 3MnO2 + 4Al → 3Mn + 2Al2O3 Таким способом получают Mn, Cr, Ti, Mo, W
- 21. 2. ГИДРОМЕТАЛЛУРГИЯ Получение металлов из растворов их солей. Перевод нерастворимого соединения в раствор: CuO + H2SO4
- 23. Скачать презентацию















 ОВР. Метод электронного баланса
ОВР. Метод электронного баланса Кислоты. Общая формула кислот
Кислоты. Общая формула кислот Презентация на тему Алюминий как химический элемент и как простое вещество
Презентация на тему Алюминий как химический элемент и как простое вещество  Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу
Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу Предмет органической химии
Предмет органической химии Неметаллы
Неметаллы Химия. Соотечественники, внёсшие большой вклад в становление и развитие этой науки
Химия. Соотечественники, внёсшие большой вклад в становление и развитие этой науки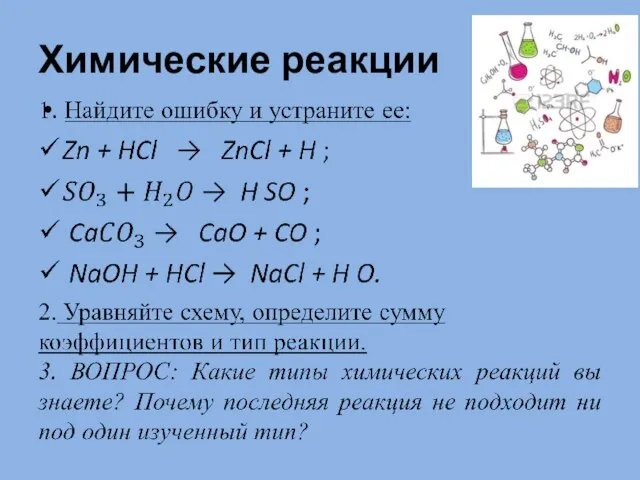 Химические реакции
Химические реакции Водородная химическая связь
Водородная химическая связь Понятие аналитической химии, её цели и задачи. Химический анализ, его задачи
Понятие аналитической химии, её цели и задачи. Химический анализ, его задачи Тепловой эффект химических реакций
Тепловой эффект химических реакций Газоанализаторы. Измерительный прибор для определения качественного и количественного состава смесей газов
Газоанализаторы. Измерительный прибор для определения качественного и количественного состава смесей газов Неметалічні елементи
Неметалічні елементи Вода. Классы неорганических соединений. 8 класс
Вода. Классы неорганических соединений. 8 класс Неметаллы. Агрегатные состояния неметаллов
Неметаллы. Агрегатные состояния неметаллов Строение атома. Связь основных характеристик атома с его положением в таблице Д.И. Менделеева. Способы изображения строения
Строение атома. Связь основных характеристик атома с его положением в таблице Д.И. Менделеева. Способы изображения строения Процессы минералообразования
Процессы минералообразования Химическая связь и строение вещества
Химическая связь и строение вещества Фотохромные биоматериалы. Применение спиропирановых систем в медицине
Фотохромные биоматериалы. Применение спиропирановых систем в медицине Аналитическая химия
Аналитическая химия Неорганические вещества клетки. 10 класс
Неорганические вещества клетки. 10 класс Типы химических реакций. Решение примеров
Типы химических реакций. Решение примеров Основы радиохимии и радиологии
Основы радиохимии и радиологии Кислород и сера. Их положение в ПСХЭ. Значение и применение
Кислород и сера. Их положение в ПСХЭ. Значение и применение Основания
Основания Презентация на тему Самородки 9 класс
Презентация на тему Самородки 9 класс  Алкадиены. Строение. Гомологический ряд. Изомерия. Номенклатура
Алкадиены. Строение. Гомологический ряд. Изомерия. Номенклатура Окислительно-восстановительные реакции
Окислительно-восстановительные реакции