Содержание
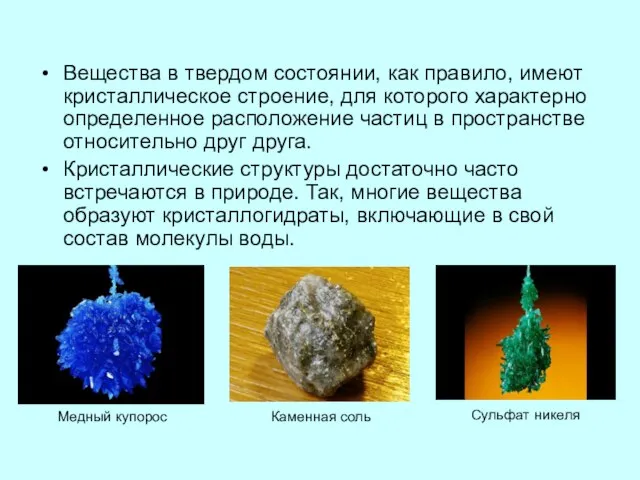
- 2. Вещества в твердом состоянии, как правило, имеют кристаллическое строение, для которого характерно определенное расположение частиц в
- 3. Если присмотреться, то можно разглядеть кубическое строение кристаллов поваренной соли
- 4. Если обозначить все частицы в виде точек и соединить их пересекающимися прямыми линиями, то образуется пространственный
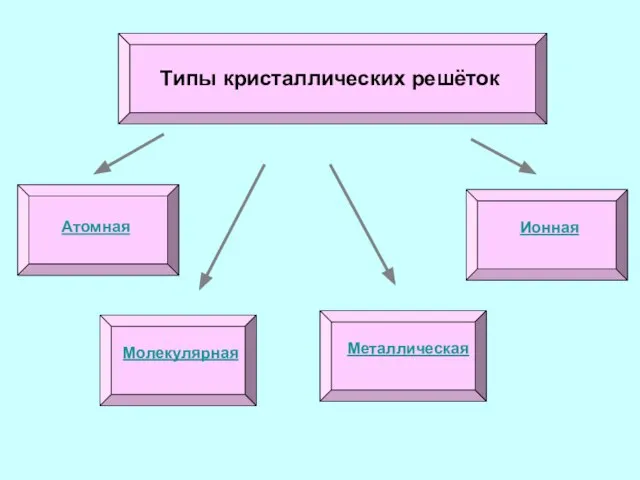
- 5. Типы кристаллических решёток Атомная Ионная Молекулярная Металлическая
- 6. Атомной кристаллической решеткой называется решетка, в узлах которой располагаются атомы, соединенные между собой прочными ковалентными связями
- 7. Например, в кристалле алмаза атомы углерода соединены в форме тетраэдра (каркасная структура, рис.а). У кристаллической решетки
- 8. Бриллиант – ограненный алмаз
- 9. Ионными называют кристаллические решетки, в узлах которых находятся положительно и отрицательно заряженные ионы, между которыми существуют
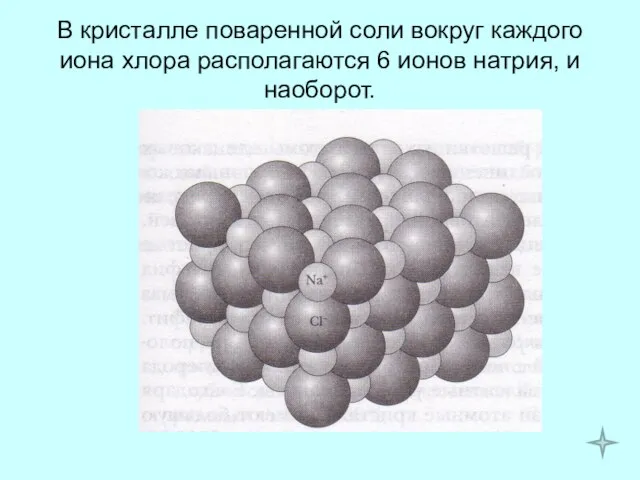
- 10. В кристалле поваренной соли вокруг каждого иона хлора располагаются 6 ионов натрия, и наоборот.
- 11. Молекулярными называют кристаллические решетки, в узлах которых находятся отдельные молекулы, между которыми образуется ковалентная связь. Молекулярными
- 12. Наличие водородных связей (частный случай ковалентной полярной связи) в воде приводит к образованию причудливой формы снежинок.
- 13. Металлическими называют кристаллические решетки, в узлах которых находятся отдельные атомы или ионы металлов, между которыми движутся
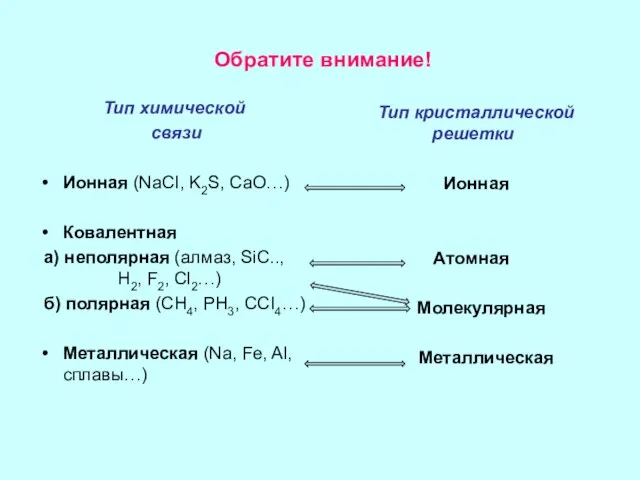
- 14. Обратите внимание! Тип химической связи Ионная (NaCI, K2S, CaO…) Ковалентная а) неполярная (алмаз, SiC.., H2, F2,
- 16. Скачать презентацию









 Введение в общую теорию поверхностных явлений. Лекция 1
Введение в общую теорию поверхностных явлений. Лекция 1 Презентация на тему Все о спиртах
Презентация на тему Все о спиртах  Щелочные металлы
Щелочные металлы Циклоалканы. Строение, изомерия, получение и свойства
Циклоалканы. Строение, изомерия, получение и свойства Основания
Основания Железо как химический элемент
Железо как химический элемент Характеристика углерода
Характеристика углерода Презентация на тему Типы изомерии
Презентация на тему Типы изомерии  Кроссворд Интересные факты в химии
Кроссворд Интересные факты в химии Великий кислород
Великий кислород Чистые вещества и смеси
Чистые вещества и смеси Кислотність бджолиного обніжжя
Кислотність бджолиного обніжжя Нобелевские лауреаты и их достижения
Нобелевские лауреаты и их достижения Химическое равновесие. Экзаменационные вопросы
Химическое равновесие. Экзаменационные вопросы Физическая и коллоидная химия
Физическая и коллоидная химия Валентность, классы и номенклатура неорганических веществ
Валентность, классы и номенклатура неорганических веществ Гетероциклические соединения. Пятичленные гетероциклы с одним гетероатомом
Гетероциклические соединения. Пятичленные гетероциклы с одним гетероатомом Химическая посуда и лабораторное оборудование
Химическая посуда и лабораторное оборудование Бериллий, магний и щелочноземельные металлы
Бериллий, магний и щелочноземельные металлы Строение вещества
Строение вещества Ацетиленовые углеводороды. Алкины
Ацетиленовые углеводороды. Алкины Особенности формирования естественно-научной картины мира на уроках географии и химии
Особенности формирования естественно-научной картины мира на уроках географии и химии Моделирование деформаций углеродных слоёв при функционализации технического углерода
Моделирование деформаций углеродных слоёв при функционализации технического углерода prezentatsiya-po-fizike-7-klass-tri-agregatnyh-sostoyaniya-veshchestva
prezentatsiya-po-fizike-7-klass-tri-agregatnyh-sostoyaniya-veshchestva 11_PERMANGANATOMETRIYa_JODOMETRIYa_1
11_PERMANGANATOMETRIYa_JODOMETRIYa_1 Химический канцерогенез
Химический канцерогенез Силикатная промышленность
Силикатная промышленность Расчеты по химическим уравнениям
Расчеты по химическим уравнениям