Содержание
- 2. 1. До групи лужних металів належать: Літій, Натрій, Рубідій, Цезій Гра «Так» чи «Ні» Так 2.
- 3. 5. Хімічна активність галогенів спадає із збільшенням відносної атомної маси Так 6. Оксиди лужних металів виявляють
- 4. 10. Галогени взаємодіють з металами, утворюючи солі Так 11. Інертні елементи – типові неметали Ні 12.
- 5. В основу класифікації Д. І. Менделєєв поклав значення відносної атомної маси. На кожний елемент із 63
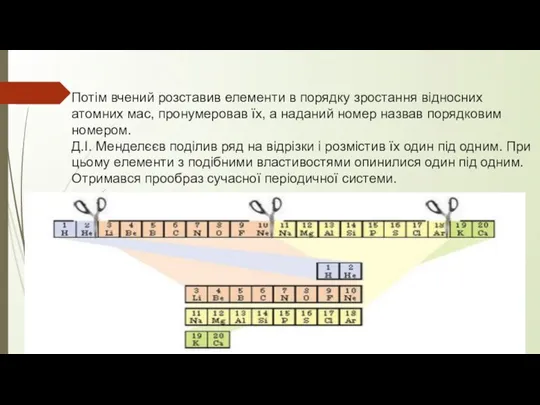
- 6. Потім вчений розставив елементи в порядку зростання відносних атомних мас, пронумеровав їх, а наданий номер назвав
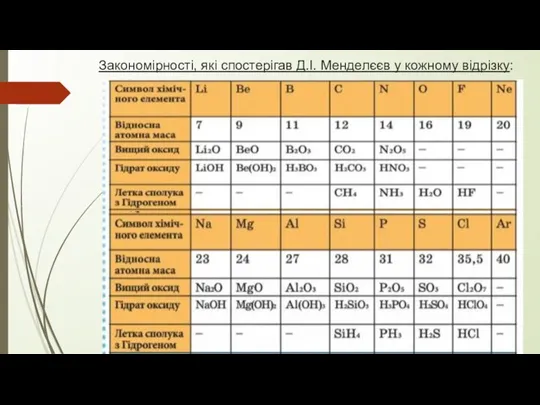
- 7. Закономірності, які спостерігав Д.І. Менделєєв у кожному відрізку:
- 8. 1) Металічні властивості спадають, неметалічні – зростають; 2) Валентність в сполуках з Оксигеном зростає; 3) Характер
- 9. У 1869р. Д.І. Менделєєв сформулював періодичний закон: Властивості елементів і властивості утворених ними простих і складних
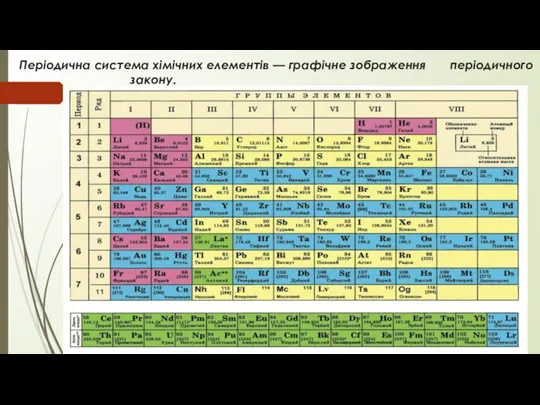
- 10. Періодична система хімічних елементів — графічне зображення періодичного закону.
- 11. Елементи, розташовані в періодичній системі утворюють 7 періодів. Будова періодичної системи Період – це горизонтальний ряд
- 12. Елементи, розташовані в періодичній системі, утворюють 8 груп. Будова періодичної системи Група – це вертикальний стовпчик,
- 13. Вниз таблиці винесено загальні формули вищих оксидів і летких сполук з Гідрогеном Будова періодичної системи Елементи
- 14. 1). Скільки періодів містить періодична система? 2). Які бувають періоди? 3).Чим відрізняються між собою періоди? 4).
- 15. Охарактеризуйте положенням елемента в періодичній системі за планом
- 16. Як змінюються властивості елементів в періодах і групах
- 18. Скачать презентацию












 Физические свойства спиртов
Физические свойства спиртов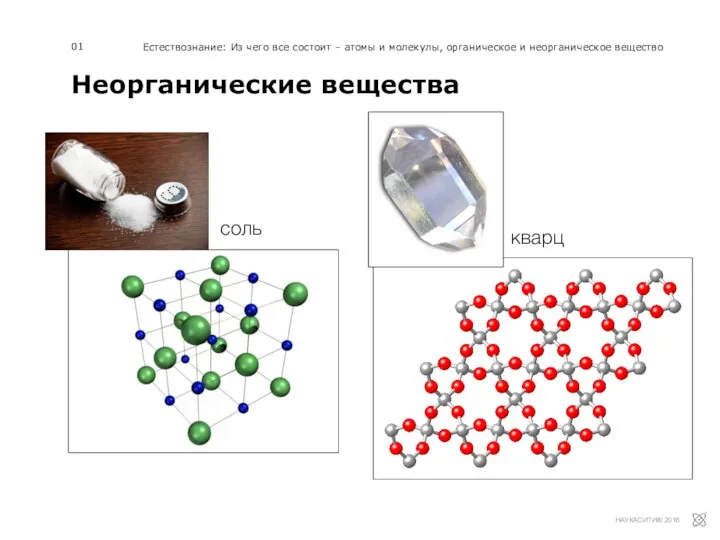 Неорганические вещества
Неорганические вещества Презентация на тему Неорганічні речовини живих організмів
Презентация на тему Неорганічні речовини живих організмів  Проект в сфере экологического волонтерства преподавателя химии первой квалификационной категории
Проект в сфере экологического волонтерства преподавателя химии первой квалификационной категории Л-1-4
Л-1-4 Способы получения веществ 14 (IVА) группы элементов
Способы получения веществ 14 (IVА) группы элементов Получение металлов
Получение металлов Термохимия
Термохимия Органическая химия. Подготовка к экзамену
Органическая химия. Подготовка к экзамену Химическая связь. 11 класс
Химическая связь. 11 класс Хром (Cr)
Хром (Cr) 热塑性复合材料的分类及特性
热塑性复合材料的分类及特性 10_kl_klas-ya
10_kl_klas-ya Общая химия. Основные понятия
Общая химия. Основные понятия Сколько нужно чистого белка
Сколько нужно чистого белка Основные классы неорганических соединений
Основные классы неорганических соединений Презентация на тему: Изомерия
Презентация на тему: Изомерия Азот и его свойства
Азот и его свойства Анализ лекарственных форм с витаминами и использование физико-химических и химических методов анализа. Вопросы стабилизации
Анализ лекарственных форм с витаминами и использование физико-химических и химических методов анализа. Вопросы стабилизации Роль элементов 5 группы
Роль элементов 5 группы Растворы
Растворы Теория химического строения органических веществ А.М. Бутлерова
Теория химического строения органических веществ А.М. Бутлерова Полимерные материалы
Полимерные материалы Нітратна кислота Презентація вчителя хімії Смілянської загальноосвітньої школи І-ІІІ ст. № 11 Л.В.Заруби
Нітратна кислота Презентація вчителя хімії Смілянської загальноосвітньої школи І-ІІІ ст. № 11 Л.В.Заруби Круговорот серы в природе
Круговорот серы в природе Харктеристика металлов
Харктеристика металлов Катаболизм пуриновых нуклеотидов
Катаболизм пуриновых нуклеотидов Быстрорастущие кристаллы
Быстрорастущие кристаллы