Слайд 2Цель работы:
Провести количественное определение Fe и Ca,
содержащихся в модельном растворе образца доломита.
Задачи:
Изучить

примерный состав природного доломита
Составить схему качественного анализа на основе изученной литературы
Провести качественный анализ модельного раствора
На основе полученных данных, составить схему количественного анализа раствора
Определить концентрацию Fe и Ca, оценить суммарную погрешность определения
Проверить правильность результата для железа путем сравнения равноточности двух методов
Слайд 3Доломит.
Доломи́т — минерал из класса карбонатов, а также осадочная карбонатная горная порода, состоящая из этого

минерала на 95 % и более. Получил название вчесть французского инженера и геолога Деода де Доломьё (1750—1801), описавшего признакидоломитовых пород.
Используется в стекольной промышленности, в производстве флюсов, огнеупорных материалов, облицовочных материалов, в агропромышленности (для раскисления и удобрения почв)
Слайд 4Состав породы:
CaCO3*MgCO3
CaO – 30.4%
MgO – 21.7%
CO2 – 47.9%
В качестве примесей входит Fe

и Mn,
реже Sr, Zn, Ni
Слайд 5Отбор средней пробы
Отбор проб кускового доломита производят от штабелей до погрузки

или после выгрузки его из транспортных средств не менее чем из 30 равномерно удаленных друг от друга участков штабеля. Точечную пробу массой не менее 0.5 кг на каждом участке отбирают от 10 соприкасающихся друг с другом кусков доломита откалыванием молотком кусочков массой не менее 50 г. Все отобранные точечные пробы соединяют в объединенную пробу, тщательно перемешивают и методом квартования сокращают до массы не менее 4 кг. Полученную пробу измельчают на лабораторных бегунах или валковой дробилке до крупности не более 1 мм, сокращают методом квартования до массы 1 кг и тем же методом делят на две равные части, которые помещают в полиэтиленовые пакеты или стеклянные банки и снабжают этикетками с указанием соответствующих параметров.
Слайд 6Пробоподготовка
Согласно методикам ГОСТ 23673.1-79, навеску молотого доломита предлагается смочить водой, а затем

осторожно прилить некоторое количество кислоты (4 мл.). После частичного растворения добавляют еще 50 мл воды, перемешивают, кипятят, периодически разминая материал стеклянной палочкой. По окончанию выделения пузырьков при наличии нерастворенного остатка его фильтруют, промывают 8-10 раз горячей водой, собирая промывные воды в ту же колбу. Фильтрат охлаждают, доводят до метки и перемешивают.
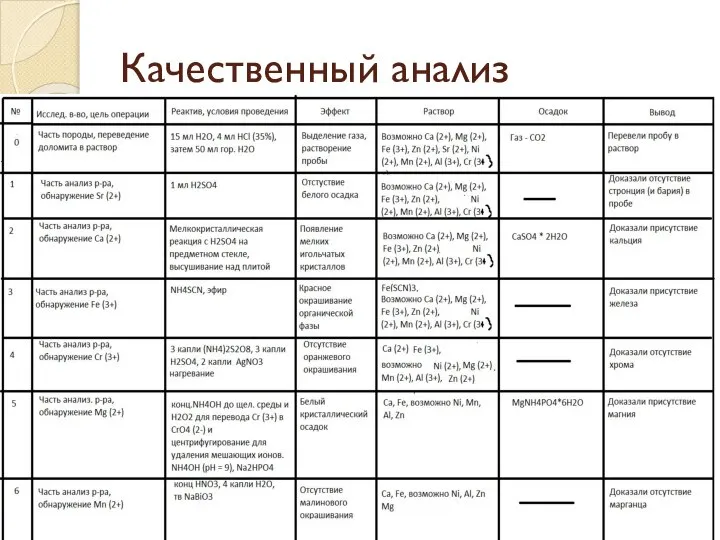
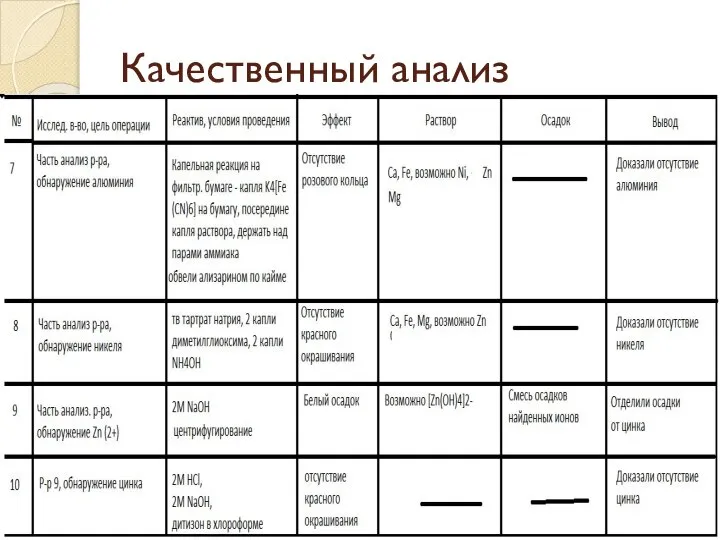
Слайд 9Итог качественного анализа
Было доказано присутствие Fe (3+), Ca, Mg
Было доказано отсутствие Cr

(3+), Sr, Ba, Al, Ni, Mn, Zn
Слайд 10Количественный анализ
Исходя из полученных данных, была предложена следующая схема количественного анализа:
Определение железа
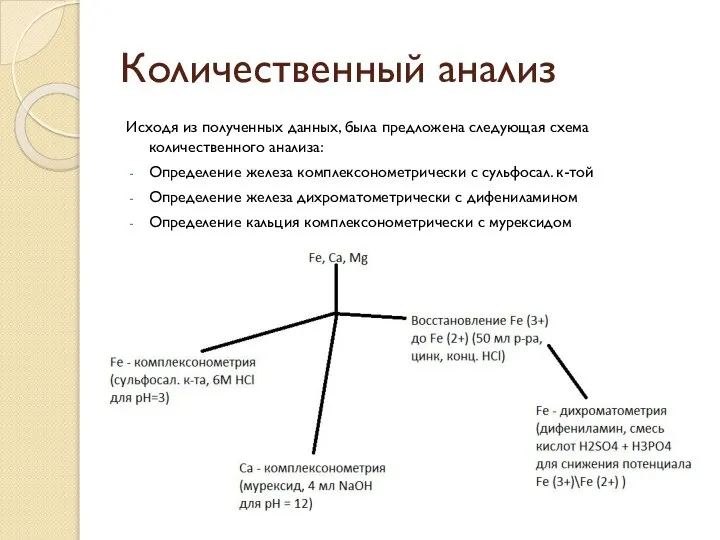
комплексонометрически с сульфосал. к-той
Определение железа дихроматометрически с дифениламином
Определение кальция комплексонометрически с мурексидом
Слайд 11Определение кальция
К 10 мл анализируемого раствора прилили 3 мл триэтаноламина и 4.5

мл NaOH. Затем прибавили пару шпателей мурексида, наблюдали интенсивное фиолетовое окрашивание. Титровали раствором ЭДТА до устойчивого перехода цвета раствора в синий.
Ca (2+) + Y (4-) => CaY (2-)
Слайд 13Определение железа комплексонометрически
К 10 мл аликвоты добавляют NH4OH до появления мути, растворяют

ее несколькими каплями 6М HCl, затем добавляют 4 мл 4М HCl, что сопровождалось изменением цвета на ярко-зеленый (Соли Fe(3+)) добавляют примерно 10-15 мл H2O, несколько капель сульфосалициловой кислоты, перемешивают и доводят до кипения. При этом раствор принял фиолетовую окраску. После этого раствору дали остыть и провели титрование комплексоном III, наблюдали переход окраски из фиолетовой в желтую
Слайд 14Определение железа комплексонометрически

Слайд 15Определение железа дихроматометрически
Для восстановления было отобрано 50 мл анализируемого раствора, к которому

прибавили около 20 гранул цинка и 30 мл конц HCL. Полученный раствор поставили на плиту, колбу накрыли воронкой, наблюдали выделение газа и постепенное обесцвечивание раствора. Проверяли окончание восстановления качественной реакцией с тиоционатом, когда раствор не дал красную окраску, колбу сняли с плиты, остудили. Раствор был профильтрован через вату и количественно перенесен в мерную колбу на 100 мл, доведен до метки водой, перемешан. Затем аликвоты полученного раствора объемом 10 мл были перенесены в колбы для титрования, к ним добавили смесь кислот (H2SO4+H3PO4) и 5 капель дифениламина. При титровании наблюдали переход окраски со светло- до темно-зеленого, а при достижении ктт в фиолетовый.
Fe(3+) + e = Fe(2+), E = 0,771 B
Fe(3+) + 2H2SO4 => Fe(SO4)2 (-), E (Fe(SO4)2 (-)\FeSO4) = 0,68 B
Fe(3+) + H2PO4(-) => FeH2PO4(2+), Eитог (Fe(3+)\Fe(2+)) = 0,60 B
2Fe(3+)+Zn => 2Fe(2+) +Zn(2+)
Fe(3+) +3SCN(-) => Fe(SCN)3
6Fe(2+) +Cr2O7(2-)+14H(+) =>6Fe(3+) + 2Cr(3+) +7H2O
Cr2O7(2-) + 6e +14H(+)=> 2Cr(3+) +7H2O, E = 1,33 B
Слайд 16Определение железа дихроматометрически
Fe(3+) + e = Fe(2+), E = 0,771 B
Fe(3+) +

2H2SO4 =>
Fe(SO4)2 (-), E (Fe(SO4)2 (-)\
\FeSO4) = 0,68 B
Fe(3+) + H2PO4(-) =>
FeH2PO4(2+),
Eитог (Fe(3+)\Fe(2+)) = 0,60 B
2Fe(3+)+Zn => 2Fe(2+) +Zn(2+)
Fe(3+) +3SCN(-) => Fe(SCN)3
6Fe(2+) +Cr2O7(2-)+14H(+) =>
6Fe(3+) + 2Cr(3+) +7H2O
Cr2O7(2-) + 6e +14H(+)=>
=> 2Cr(3+) +7H2O
Слайд 17Проведение проверки правильности

Слайд 18Выводы
Мы изучили состав модельного раствора доломита с использование методик качественного и количественного

анализа. Предложенный раствор содержал Fe, Ca и Mg. Среднее содержание железа можно выразить как (0,337±0,005) грамм в 200 мл раствора (или 1.6234 гр. теор. навески), в то время как содержание оксида кальция можно оценить как (0.4935±0.0039) грамм на 200 мл раствора.
Слайд 19Вывод
Мы изучили методику определения содержания ионов магния комплексонометрическим титрованием.

















 Природні сполуки алюмінію і методи одержання
Природні сполуки алюмінію і методи одержання Презентация на тему Обобщение по типам химических реакций
Презентация на тему Обобщение по типам химических реакций  Многоядерные Арены
Многоядерные Арены 8. Изотопы. Ядерные реакции
8. Изотопы. Ядерные реакции Вязкость жидкости
Вязкость жидкости Металлургия в химии
Металлургия в химии Химические процессы на кухне (урок №7)
Химические процессы на кухне (урок №7) Основания: номенклатура, классификация, применение, физические свойства
Основания: номенклатура, классификация, применение, физические свойства Кислоты
Кислоты Потенциометрические анализаторы Поверка рН - метра
Потенциометрические анализаторы Поверка рН - метра Алканы. Задания
Алканы. Задания Закон сохранения массы и химические уравнения
Закон сохранения массы и химические уравнения Щелочные металлы
Щелочные металлы Характеристика кислорода и серы
Характеристика кислорода и серы Кремний – химический элемент или природный дар
Кремний – химический элемент или природный дар Нефть. Способы переработки нефти
Нефть. Способы переработки нефти Косметические средства и бытовая химия
Косметические средства и бытовая химия Классификация неорганических веществ. Оксиды
Классификация неорганических веществ. Оксиды Химическая реакция
Химическая реакция Аммиак. Строение молекулы. Водородная связь
Аммиак. Строение молекулы. Водородная связь Число химических связей, способных образовать данный атом
Число химических связей, способных образовать данный атом Основные законы и понятия химии. Основные классы неорганических соединений. Химический эквивалент. Закон эквивалентов
Основные законы и понятия химии. Основные классы неорганических соединений. Химический эквивалент. Закон эквивалентов Резиновые материалы и клеи. Тема 7.5
Резиновые материалы и клеи. Тема 7.5 Мило. Його склад. Мийна дія
Мило. Його склад. Мийна дія Ювелирные камни
Ювелирные камни Нефть. Свойства нефти
Нефть. Свойства нефти Занимательная химия в 8 классе
Занимательная химия в 8 классе Углеводороды
Углеводороды