Слайд 2Валенттілік, (лат. valentіa — күш) — атомның басқа атомдарды немесе атомдар тобын қосып

алып химиялық байланыс құру қасиеті.
Химияға валенттілік ұғымын 1853 ж. ағылшын химигі Э.Франкленд (1825 — 1899) енгізген.
А.М. Бутлеровтың қосылыстардың химиялық құрылысы теориясына (1861) Валенттілік негіз болды
Менделеев элементтің валенттілікінің оның периодтық жүйедегі орнымен байланыстылығын тапты, айнымалы валенттілік туралы ұғымды енгізді
Элементтердің валенттілікіне қарап химиялық формулаларды жазуға болады
Слайд 3Валенттіліктің бірлігі ретінде сутектің валенттілігі алынған, сутек қосылыстарында әркашан бір валентті деп

есептеледі. Өзімізге белгілі судың формуласы Н20 (аш екі о), ол молекуланың сутектің 2 атомы мен оттектің бір атомынан тұратынын көрсетеді. Судың кұрамында оттектің бір атомына сутектің екі атомы сөйкес келеді екен. Оны былай көрсетсек Н-О-Н оттектің валенттілігі екіге тең екенін байқаймыз. Өйткені сутек бір жағымен байланысса, оттек екі жағымен де байланысады.
Слайд 5Валенттілік рим цифрларымен белгіленеді, формулаларда элмент таңбасының үстіне жазылады, мәні I-VIII-гe дейін

өзгереді. Валенттілік бойынша формула құру үшін элементтердің валенттіліктерінің ең кіші ортак еселігін тауып, әр элементтін валенттілігіне бөліп, индекс етіп жазамыз. Егер элемент қосылыстарында айнымалы валенттілік көрсетсе, онын, атауында элементтің валенттілігі рим цифрымен жақшаның ішінде көрсетіледі.
Слайд 6МОЛЕКУЛА КҰРАМЫ ЕКІ ЭЛЕМЕНТ АТОМЫНАН ТҰРАТЫН ҚОСЫЛЫСТАР БИНАРЛЫ ҚОСЫЛЫСТАР ДЕП АТАЛАДЫ.
Н20
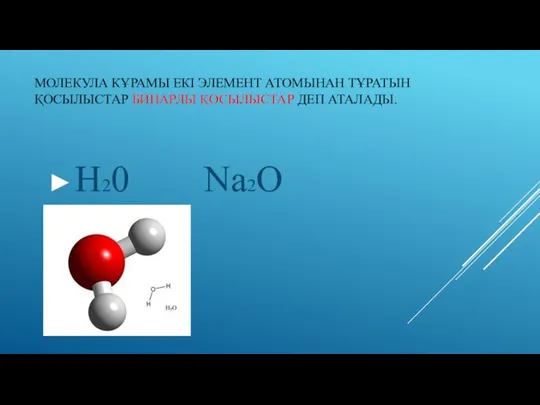
Na2О
Слайд 8АТОМ-МОЛЕКУЛАЛЫҚ ІЛІМ
Атом-молекулалық ілім — жаратылыстану және зат бөлшектері туралы теориялардың жинағы.
Атом-молекулалық ілімнің

қалыптасып дамуына өз заманында М. В. Ломоносов, Дж. Дальтон, А. Лавуазье, Ж. Пруст, А. Авогадро, Й. Берцелиус, Д. И. Менделеев, А. М. Бутлеров секілді зор үлес қосқан.






 Полисахариды
Полисахариды Особенные свойства муравьиной кислоты
Особенные свойства муравьиной кислоты Замедленное коксование нефтяного сырья
Замедленное коксование нефтяного сырья Водные растворы электролитов
Водные растворы электролитов Посвящение в химики
Посвящение в химики Открытый урок на тему: Степень окисления
Открытый урок на тему: Степень окисления Презентация на тему Скорость химических реакций
Презентация на тему Скорость химических реакций  Задача на химическое равновесие
Задача на химическое равновесие Спирты. Классификация спиртов
Спирты. Классификация спиртов Порох: из грязи в князи
Порох: из грязи в князи Alkalické kovy
Alkalické kovy Превращения серосодержащих соединений
Превращения серосодержащих соединений Понятие аналитической химии, её цели и задачи. Химический анализ, его задачи
Понятие аналитической химии, её цели и задачи. Химический анализ, его задачи получение Ме презентация
получение Ме презентация Органика из аптеки
Органика из аптеки Азот
Азот Презентация на тему Решение задач на смеси, сплавы, растворы
Презентация на тему Решение задач на смеси, сплавы, растворы  Металл XXI века титан
Металл XXI века титан Всё о нефти. Часть 5
Всё о нефти. Часть 5 Закон сохранения массы и энергии
Закон сохранения массы и энергии Предельные углеводороды. Тест 19
Предельные углеводороды. Тест 19 Фізика гірських порід і процесів. Хімічні зв'язки в мінералах. Іонний зв'язок
Фізика гірських порід і процесів. Хімічні зв'язки в мінералах. Іонний зв'язок Презентация на тему Подгруппа углерода
Презентация на тему Подгруппа углерода  Получение и химические свойства металлов
Получение и химические свойства металлов Синтез олигомеров этиленгликоля и терефталевой кислоты
Синтез олигомеров этиленгликоля и терефталевой кислоты Презентация на тему Признаки реакций
Презентация на тему Признаки реакций  Косметические средства. Виды, состав и влияние на организм
Косметические средства. Виды, состав и влияние на организм Каучук. История открытия каучука
Каучук. История открытия каучука