Слайд 13Степень окисления –
Это условный заряд атомов химического элемента в соединении, вычисленный

на основе предположения, что все соединения (и ионные и ковалентно-полярные) состоят только из ионов.
Слайд 14Правила определения степени окисления:
Степень окисления свободных атомов и простых веществ равна 0:

( Mg0, N20, K0)
Степень окисления водорода в соединениях с неметаллами равна +1, а с металлами равна -1: (NaH-1, H+1Cl).
Степень окисления фтора в соединениях всегда равна -1: (HF-1, CaF-12).
Степень окисления кислорода в соединениях равна -2 (NO-2, Al2O3-2), а в пероксидах -1 (H2O2-1) в соединении с фтором +2 (O+2F2)
Степень окисления металлов в соединениях всегда положительная , у металлов I-A, II-A, III-A соответственно равна +1, +2, +3 .
Суммарная степень окисления всех атомов в молекуле равна 0.
Высшая степень окисления элемента равна (+№ группы).
Низшая степень окисления: для металлов равна 0, для неметаллов равна (№ группы -8).
Слайд 15Промежуточные с.о.
Рассмотрим возможные с.о. серы – S
Максимальная +6 SO3
Минимальная -2 H2S
Сера может

проявлять с.о. 0,+2,+4 – это промежуточные с.о.
Слайд 16Как определить степень окисления элемента в соединении? (с. 88)
1) Определение степеней окисления

начинают с того элемента, у которого С.О. (Р2О-25); постоянная или известна в соответствии с правилами (см. выше);
2) Умножить эту С.О. на индекс (– 2 * 5 = – 10);
3) Полученное число разделить на индекс второго элемента (– 10 / 2 = – 5);
Записать полученную С.О. с противоположным знаком (Р+52О-25).
Слайд 17Задание :
Определите С.О. по формулам:
Cl2O7, NaH, Na2S, MgO, H3N, N2, Al2S3, Cu2O
Слайд 18Алгоритм названия бинарных соединений:
Пример: Al+32O-23 – оксид алюминия; Cu+2O-2 – оксид меди (II)
Cl-1 –

хлорид; O-2 – оксид; Н-1 – гидрид;
S-2 – сульфид; C-4 – карбид; N-3 – нитрид; P-3 — фосфид; Si-4 — силицид.
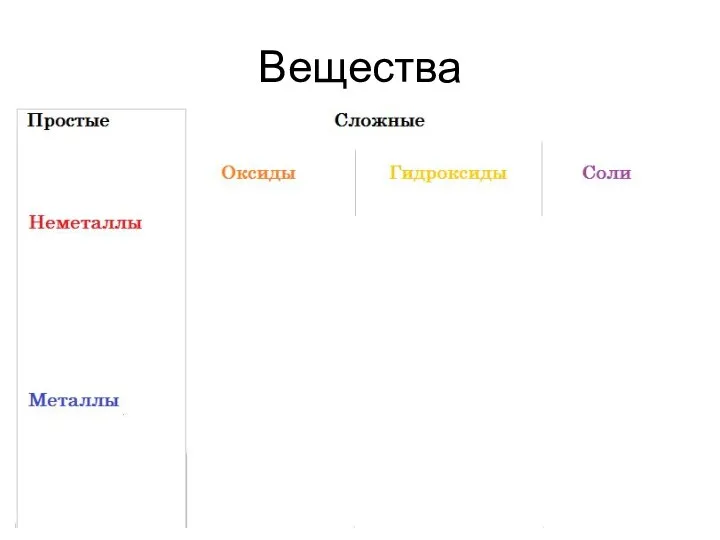
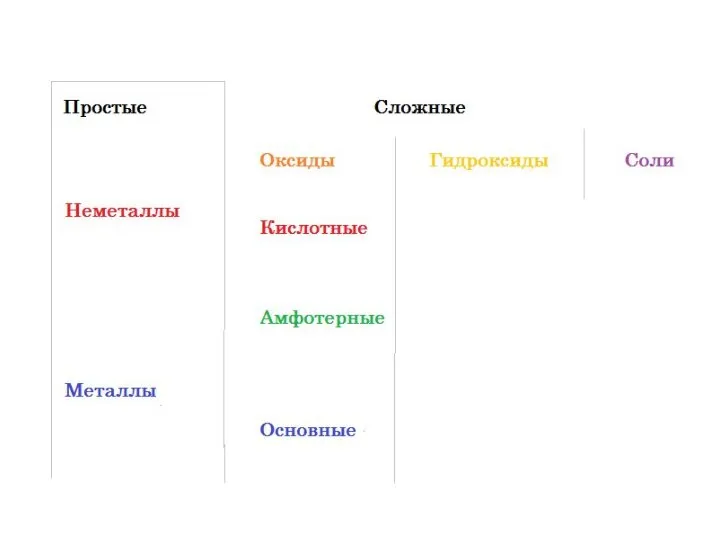
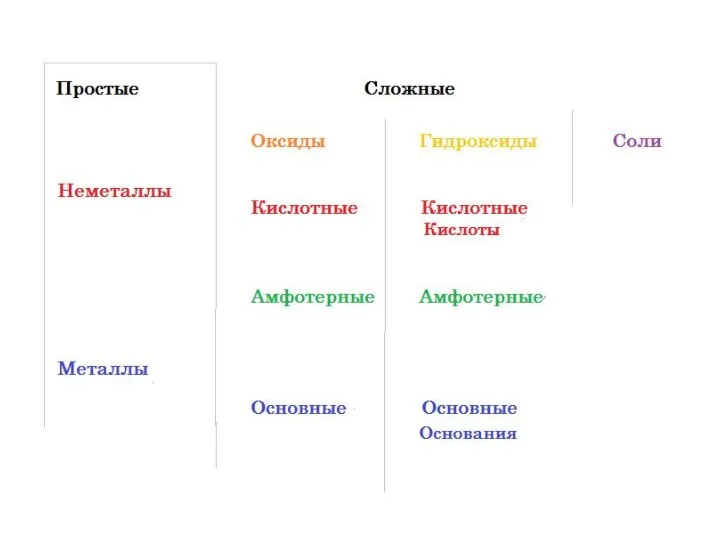
Слайд 19Алгоритм составления формул по названиям:
Записать знаки элементов (частиц) в порядке: на первом

месте – положительно заряженную, на втором – отрицательно заряженную ( Al O );
Расставить степени окисления ( Al+3 O-2);
Найти наименьшее общее кратное (НОК) между значениями степеней окисления, записать его между ними в “окошечко”;
Разделить НОК на значение степеней окисления, полученные результаты записать как индексы (6/3=2; 6/3=3 Al2O3).









 Теория-кинетика
Теория-кинетика Железо как химический элемент
Железо как химический элемент Получение серной кислоты
Получение серной кислоты Полиуретаны. Структура и строение
Полиуретаны. Структура и строение Замедленное коксование гудрона
Замедленное коксование гудрона Классификации по атомному весу
Классификации по атомному весу Кислоты
Кислоты Влияние растворителей на скорость органических реакций. (Лекция 10)
Влияние растворителей на скорость органических реакций. (Лекция 10)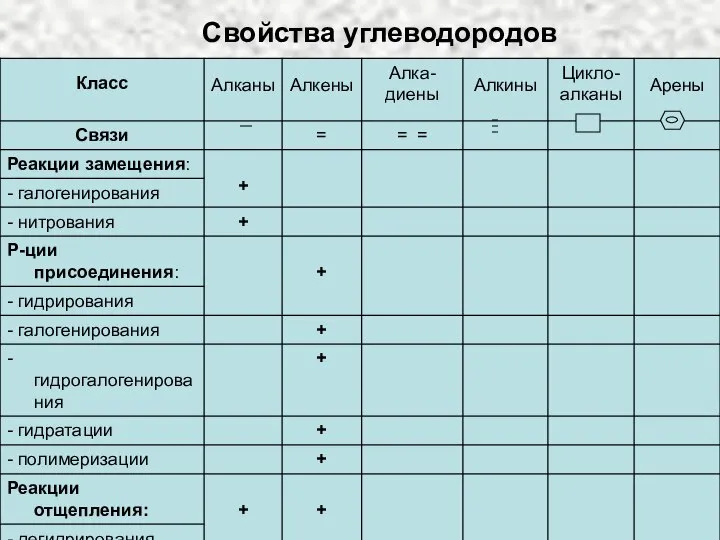 Свойства углеводородов
Свойства углеводородов Химические реакции. по фазовому составу
Химические реакции. по фазовому составу Анализ объектов окружающей среды. Сопоставление и выбор методов анализа
Анализ объектов окружающей среды. Сопоставление и выбор методов анализа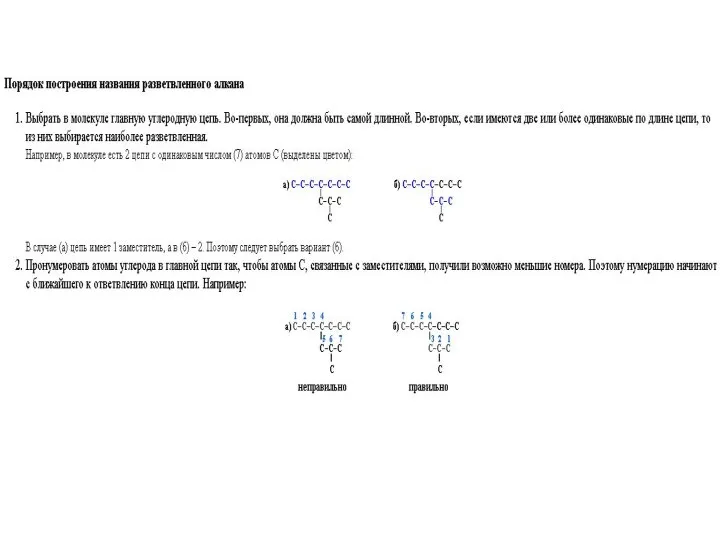 Номенклатура алканов РВЛ
Номенклатура алканов РВЛ Состояние электронов в атоме
Состояние электронов в атоме Классификация спиртов. Изомерия спиртов
Классификация спиртов. Изомерия спиртов Кинетика химических и биохимических процессов. Часть 1
Кинетика химических и биохимических процессов. Часть 1 Презентация на тему Железо и его соединения
Презентация на тему Железо и его соединения  Расчет печи кипящего слоя в производстве хлорида калия
Расчет печи кипящего слоя в производстве хлорида калия Алканы. Строение, номенклатура, изомерия, физические свойства
Алканы. Строение, номенклатура, изомерия, физические свойства Презентация на тему Водород, его общая характеристика, нахождение в природе и его свойства
Презентация на тему Водород, его общая характеристика, нахождение в природе и его свойства  Алкины. Строение.номенклатура. Изомерия. Получение
Алкины. Строение.номенклатура. Изомерия. Получение Физико-химия полимеров
Физико-химия полимеров Хлордың қолданылуы
Хлордың қолданылуы Карбоновые кислоты
Карбоновые кислоты Презентация на тему Щелочные и щелочноземельные металлы
Презентация на тему Щелочные и щелочноземельные металлы  Электрохимия. Электролиты
Электрохимия. Электролиты Галогениды, нитраты и сульфаты лантаноидов
Галогениды, нитраты и сульфаты лантаноидов Окситоцин. Сила любви и биология
Окситоцин. Сила любви и биология Chemia kosmetyczna
Chemia kosmetyczna