Содержание
- 2. Габер Фриц Синтез аммиака – процесс связывания азота, который впервые осуществил известный немецкий химик - неорганик
- 3. Карл Бош Немецкие исследователи Ф.Габер и К.Бош создали циркуляционную схему синтеза аммиака под давлением. В 1913
- 4. Условия для проведения синтеза N2 + 3H2 = 2NH3 Реакция обратимая, гомогенная и идет с уменьшением
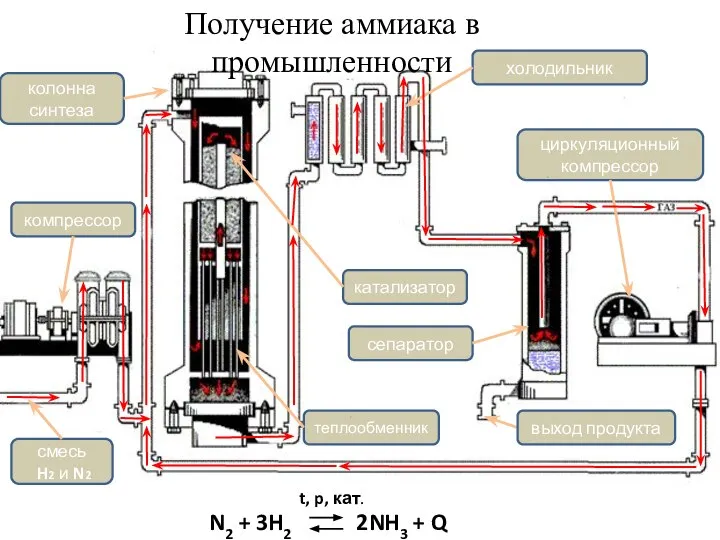
- 5. Получение аммиака в промышленности теплообменник катализатор выход продукта циркуляционный компрессор колонна синтеза
- 6. Другие способы получения аммиака: Дуговой метод Дуговой метод основан на прямом окислении азота атмосферным воздухом при
- 7. Применение аммиака удобрения пищевая промышленность (хладагент) -аммиачная вода -мочевина -сода HNO3
- 8. Действие аммиака на организм Аммиак сильно раздражает слизистые оболочки уже при 0,5%-ном содержании его в воздухе.
- 10. Скачать презентацию






 Основания. Получение оснований
Основания. Получение оснований Кремнийорганические каучуки
Кремнийорганические каучуки Химическая связь
Химическая связь Типы химических связей
Типы химических связей Металлы p-семейства
Металлы p-семейства Азотосодержащие соединения: Амины. Аминокислоты. Белки
Азотосодержащие соединения: Амины. Аминокислоты. Белки Аминокислоты. Белки. Лекция 2
Аминокислоты. Белки. Лекция 2 Алкены. Строение, номенклатура, изомерия, физические свойства
Алкены. Строение, номенклатура, изомерия, физические свойства относительная атомная масса
относительная атомная масса Примеры реакций в жизни и в быту
Примеры реакций в жизни и в быту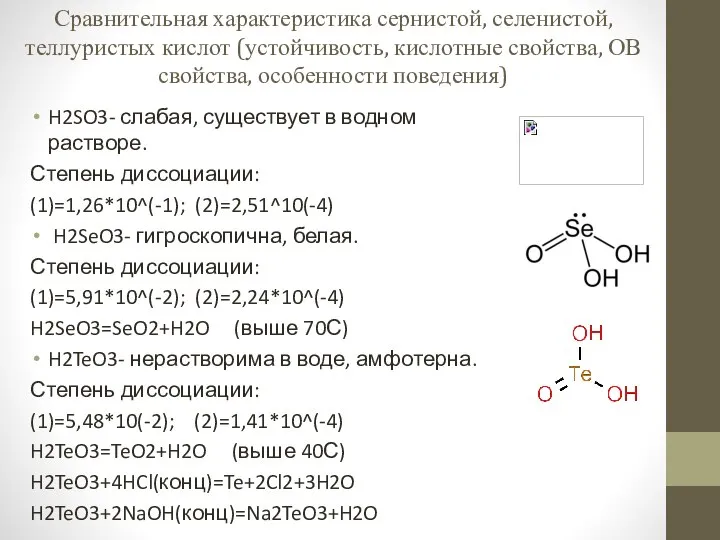 Сравнительная характеристика сернистой, селенистой, теллуристых кислот
Сравнительная характеристика сернистой, селенистой, теллуристых кислот Полімер поліетилен
Полімер поліетилен Комплексные соединения
Комплексные соединения Презентация на тему Ковалентная химическая связь
Презентация на тему Ковалентная химическая связь  Положение металлов в периодической системе Д.И. Менделеева и особенности строения их атомов
Положение металлов в периодической системе Д.И. Менделеева и особенности строения их атомов Химические реакции. по фазовому составу
Химические реакции. по фазовому составу Презентация на тему Биотехнологии. Генная инженерия
Презентация на тему Биотехнологии. Генная инженерия  Счастливый случай
Счастливый случай Презентация Продукции Opet (3)
Презентация Продукции Opet (3) Электролитическая диссоциация
Электролитическая диссоциация Реактор гидроочистки дизельного топлива
Реактор гидроочистки дизельного топлива Арены. Бензол
Арены. Бензол Окислительно-восстаовительные реакции
Окислительно-восстаовительные реакции Карбоновые кислоты
Карбоновые кислоты Изотопная геохимия. Лекция 4-5
Изотопная геохимия. Лекция 4-5 Неметаллы в ПСХЭ
Неметаллы в ПСХЭ Ионная связь
Ионная связь მეტალები
მეტალები